|
تضامنًا مع حق الشعب الفلسطيني |
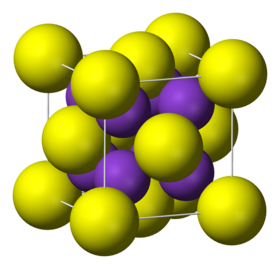
كبريتيد البوتاسيوم
اذهب إلى التنقل
اذهب إلى البحث
| كبريتيد البوتاسيوم | |
|---|---|
| الاسم النظامي (IUPAC) | |
كبريتيد البوتاسيوم |
|
| أسماء أخرى | |
سلفيد البوتاسيوم |
|
| المعرفات | |
| رقم CAS | 1312-73-8 |
| الخواص | |
| الصيغة الجزيئية | K2S |
| الكتلة المولية | 110.262 غ/مول |
| المظهر | بلورات عديمة اللون |
| الكثافة | 1,805 غ/سم3 |
| نقطة الانصهار | 840 °س |
| الذوبانية في الماء | يتحلمه إلى KOH وKSH |
| المخاطر | |
| ترميز المخاطر | |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
كبريتيد البوتاسيوم مركب كيميائي له الصيغة K2S، ويكون على شكل بلورات عديمة اللون.
التحضير
يحضر مركب كبريتيد البوتاسيوم بأنقى شكل من إضافة فلز الكبريت إلى محلول فلز البوتاسيوم في الأمونياك السائل.
يحضر تقنياً من اختزال كبريتات البوتاسيوم بالفحم حسب المعادلة:
- K2SO4 + 2C → K2S + 2CO2
أما مخبرياً يستحصل عليه من تمرير غاز كبريتيد الهيدروجين في البوتاس الكاوي، حيث يتشكل كبريتيد البوتاسيوم الحمضي أولا، والذي يتحول بإضافة كميات ستوكيومترية من هيدروكسيد البوتاسيوم إلى كبريتيد البوتاسيوم.
- KOH + H2S → KHS + H2O
- KHS + KOH → K2S + H2O
الخواص
- لمركب كبريتيد البوتاسيوم خاصية استرطاب كبيرة، كما أنه حساس للرطوبة، حيث يؤدي تماسه مع الماء إلى حلمهته وتحوله إلى كل من هيدروكسيد البوتاسيوم وكبريتيد البوتاسيوم الحمضي كما تظهر المعادلة:
- K2S + H2O → KOH + KSH
مراجع
- Taschenbuch chemische Substanzen, Willmes, Verlag Harri Deutsch, ISBN 3-8171-1662-4
| في كومنز صور وملفات عن: كبريتيد البوتاسيوم |