|
تضامنًا مع حق الشعب الفلسطيني |
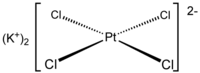
رباعي كلوروبلاتينات البوتاسيوم
| رباعي كلوروبلاتينات البوتاسيوم | |
|---|---|
| الاسم النظامي (IUPAC) | |
Potassium tetrachloroplatinate |
|
| أسماء أخرى | |
Potassium chloroplatinite |
|
| الخواص | |
| الصيغة الجزيئية | K2PtCl4 |
| الكتلة المولية | 415.09 غ/مول |
| المظهر | صلب أحمر |
| الكثافة | 3.4 غ/سم3 |
| نقطة الانصهار | 500 °س |
| الذوبانية في الماء | 0.93 غ/100 مل ماء (عند 16 °س) |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
رباعي كلوروبلاتينات البوتاسيوم مركب كيميائي صيغته K2PtCl4، ويوجد في الشروط القياسية على شكل صلب بلوري أحمر اللون.
التحضير
يحضر المركب من تفاعل سداسي كلوروبلاتينات البوتاسيوم مع أملاح الهيدرازين (مثل ثنائي كلوريد الهيدرازين).[1]
الخواص
يوجد المركب في الشروط القياسية على شكل صلب بلوري أحمر اللون، ينحل بشكل ضعيف في الماء. للبلورات بنية وفق نظام بلوري رباعي، وتتبع الزمرة الفراغية P4/mmm.
يمكن لأيونات الكلوريد في رباعي كلوروبلاتينات البوتاسيوم أن تستبدل بعدة ربيطات في تفاعلات تبادل، كما هو الحال مثلاً في تفاعل تحضير سيسبلاتين.[2]
الاستخدامات
يؤدي اختزال رباعي كلوروبلاتينات البوتاسيوم بطرق مناسبة إلى الحصول على فلز البوتاسيوم بحالة غروانية ذات أهمية محتملة في التحفيز الكيميائي.[3]
مراجع
- ^ Georg Brauer: Handbuch der präparativen anorganischen Chemie. 3., umgearb. Auflage. Band III. Enke, Stuttgart 1981, ISBN 3-432-87823-0, S. 1712 (بالألمانية)
- ^ Keller, R. N.؛ Moeller, T. (1963). "Potassium Tetrachloroplatinate(II)". Inorg. Synth. Inorganic Syntheses. ج. 7: 247–250. DOI:10.1002/9780470132333.ch79. ISBN:9780470132333.
- ^ Ahmadi, T. S.؛ Wang، Z. L.؛ Green، T. C.؛ Henglein، A.؛ El-Sayed، M. A. (1996). "Shape-Controlled Synthesis of Colloidal Platinum Nanoparticles". ساينس. ج. 272 ع. 5270: 1924ff. DOI:10.1126/science.272.5270.1924. PMID:8662492.
| رباعي كلوروبلاتينات البوتاسيوم في المشاريع الشقيقة: | |