تليف رئوي
المزيد من اللغات
المزيد من الإجراءات
| تليف رئوي | |
|---|---|
| Pulmonary fibrosis | |
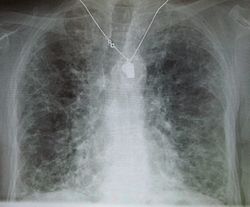
صورة للصدر بالأشعة السينية تظهر التليف الرئوي.
| |
| تسميات أخرى | تليف رئوي خلالي |
| معلومات عامة | |
| الاختصاص | طب الرئة |
| تعديل مصدري - تعديل | |
التليف الرئوي[1] (بالإنجليزية: Pulmonary fibrosis) هو مرض تنفسي تتشكل فيه ندبات في أنسجة الرئة، مما يؤدي إلى مشاكل خطيرة في التنفس. إن تكوين هذه الندبة عن طريق تراكم النسيج الضام الليفي الزائد (فيما يُسمى بالتليف) يؤدي إلى سماكة الجدران وانخفاض كمية الأكسجين في الدم، ونتيجة لذلك يعاني المرضى من ضيق دائم في التنفس.[2]
في بعض المرضى، يمكن تشخيص السبب المحدد للمرض، ولكن في حالات أخرى لا يمكن تحديد السبب المحتمل، وهي حالة تسمى بالتليف الرئوي مجهول السبب. ولا يوجد علاج معروف للندوب والتلف في الرئة بسبب التليف الرئوي.[3]
الأعراض
أعراض التليف الرئوي الرئيسية هي:[4]
- ضيق في التنفس، لا سيما مع المجهود
- السعال الجاف المزمن
- الإجهاد والضعف
- ألم في الصدر
- فقدان الشهيه وفقدان الوزن السريع
ويشير التاريخ المرضي من الضيق التدريجي في التنفس مع بذل مجهود إلى التليف الرئوي. وفي بعض الأحيان، يمكن سماع كراكر في قواعد الرئة عند التسمع، وقد تكون الأشعة السينية على الصدر طبيعية أو غير طبيعية، ولكن التصوير المقطعي عالي الدقة سيُظهر غالبا الحالات الشاذة.[3]
الأسباب
قد يكون التليف الرئوي أثرًا ثانويًا لأمراض أخرى. وتصنف معظم هذه الأمراض على أنها أمراض رئوية خلالية. وتشمل أمثلة ذلك الأمراض المناعية الذاتية، والالتهابات الفيروسية، والعدوى البكتيرية مثل السل الذي قد يتسبب في تغيرات ليفية في كل من فصوص الرئة العليا أو السفلى وغيرها من الإصابات الميكروسكوبية في الرئة. ومع ذلك، يمكن أن يظهر التليف الرئوي أيضًا بدون أي سبب معروف وفي هذه الحالة يطلق عليه «مجهول السبب».[5] ويتم تشخيص معظم الحالات مجهولة السبب على أنها تليف رئوي مجهول السبب. وفي كلتا الحالتين، هناك مجموعة متزايدة من الأدلة التي تشير إلى وجود استعداد وراثي في مجموعة فرعية من المرضى، فعلى سبيل المثال، تم العثور على طفرة في بروتين SP-C السطحي في بعض العائلات التي لديها تاريخ من التليف الرئوي.[6] وقد تم تحديد طفرات سائدة في الجينات TERC أو TERT، والتي تشفر التيلوميراز في حوالي 15 في المئة من مرضى التليف الرئوي.[7]
تشمل الأمراض والظروف التي قد تسبب التليف الرئوي كأثر ثانوي ما يلي:[3][6]
- استنشاق الملوثات البيئية والمهنية، مثل المعادن[8] في داء الأسبست، والسحار السيليسي، والتعرض لبعض الغازات. ويعتبر عمال مناجم الفحم، وعمال السفن، ومفجرو الرمال معرضين لخطر أكبر.[5]
- التهاب فرط التحسس الرئوي، وغالبا ما ينتج عن استنشاق الغبار الملوث بالمنتجات البكتيرية أو الفطرية أو الحيوانية.
- يمكن أن يزيد تدخين السجائر من الخطر أو يجعل المرض أسوأ.[5]
- بعض أمراض النسيج الضام المعتادة،[5] مثل التهاب المفاصل الروماتويدي، والذئبة الحمامية الشاملة، وتصلب الجلد.
- الأمراض الأخرى التي تشمل النسيج الضام، مثل الساركويد، والورام الحبيبي.
- العدوى.
- بعض الأدوية، على سبيل المثال أميودارون، وبليومايسين (بينجيانجميسين)، وبوسولفان، وميثوتريكسات،[5] وآبومورفين،[9] ونيتروفورانتوين.[10]
- العلاج الإشعاعي للصدر.
طريقة تطور المرض
يتضمن التليف الرئوي تبادل تدريجي للنسيج الحشوي الطبيعي للرئة بالنسيج المتليف. ويؤدي استبدال الرئة الطبيعية بالنسيج الندبي إلى انخفاض لا رجعة فيه في قدرة انتشار الأكسجين، وتجعل الصلابة الناتجة التليف الرئوي مرضًا رئويًا مقيِدًا.[11] ويستمر تليف الرئتين عن طريق الشفاء الشاذ للجروح، بدلا من التهاب مزمن،[12] وهذا هو السبب الرئيسي لمرض الرئة التقييدي. وعلى النقيض من ذلك، يعتبر الشلل الرباعي[13] والحداب[14] أمثلة على أسباب الإصابة بأمراض الرئة المقيدة التي لا تتضمن بالضرورة تليفًا رئويًا.
التشخيص

يمكن تأكيد التشخيص عن طريق خزعة الرئة.[3] وقد يكون من الضروري الحصول على ما يكفي من الأنسجة لإجراء فحص دقيق بالحصول على خزعة وتدية الشكل باستخدام المنظار تحت التخدير العام، وينطوي ذلك النوع من الخزعة على وضع عدة أنابيب من خلال جدار الصدر، حيث تستخدم واحدة منها لقطع جزء من الرئة لإرسالها للتقييم، ويتم فحصها مجهريا لتأكيد وجود ونمط التليف بالإضافة إلى وجود خصائص أخرى قد تشير إلى سبب معين.[3]
إن التشخيص الخاطئ شائع؛ لأنه في حين أن التليف الرئوي عموما ليس نادرًا، إلا أن كل نوع من أنواعه غير شائع، كما أن تقييم المرضى الذين يعانون من هذه الأمراض معقد ويتطلب نهجًا متعدد التخصصات. وقد تم توحيد المصطلحات ولكن لا تزال هناك صعوبات في تطبيقها، حتى الخبراء قد يختلفون في تصنيف بعض الحالات.[15]
وعلى مقياس التنفس كمرض رئوي مقيد، ينخفض كل من FEV1 (حجم الزفير القسري في 1 ثانية) وFVC (السعة الحيوية القسرية) بحيث تكون نسبة FEV1 / FVC طبيعية أو حتى تزيد على النقيض من مرض الرئة الانسدادي، حيث تقل هذه النسبة، وعادة ما تنخفض قيم حجم الهواء المتبقي والقدرة الكلية للرئة في أمراض الرئة المقيدة.[16]
العلاج
يخلق التليف الرئوي ندبا في نسيج الرئة، ويكون التندب دائمًا عندما يتطور،[3] ويعتمد إبطاء التقدم والوقاية على السبب الأساسي:
- خيارات العلاج للتليف الرئوي مجهول السبب محدودة للغاية. وعلى الرغم من التجارب البحثية الجارية، لا يوجد أي دليل على أن أي أدوية يمكن أن تساعد بشكل كبير هذه الحالة، وزرع الرئة هو الخيار العلاجي الوحيد المتاح في الحالات الشديدة. وبما أن بعض أنواع التليف الرئوي يمكن أن تستجيب للكورتيكوستيرويدات (مثل بريدنيزون) و/أو الأدوية الأخرى التي تقمع جهاز المناعة في الجسم، فإن هذه الأنواع من الأدوية توصف أحيانا في محاولة لإبطاء العمليات التي تؤدي إلى التليف.
- يُعتقَد أن الجهاز المناعي يلعب دورا مركزيا في تطوير العديد من أشكال التليف الرئوي. والهدف من العلاج بالمواد المثبطة للمناعة مثل الكورتيكوستيرويدات هو تقليل التهاب الرئة والتندب لاحقا، والاستجابات للعلاج متغيرة، فأولئك الذين تحسنت حالتهم مع علاج قمع المناعة ربما لم يكن لديهم تليف رئوي مجهول السبب، حيث أن التليف الرئوي مجهول السبب ليس له علاج.
- اثنين من الأدوية التي تهدف إلى منع التندب في التليف البسيط مجهول السبب هما بيرفنيدون، الذي يقلل من معدل الانخفاض في السعة الحيوية القسرية في السنة، ويقلل أيضا من انخفاض المسافات في اختبار المشي لمدة 6 دقائق، ولكن لم يكن له أي تأثير على الأعراض التنفسية،[17] والدواء الثاني هو ناينتيدانيب، الذي يعمل بمثابة مضاد حيوي بوساطة تثبيط مجموعة متنوعة من مستقبلات كيناز التيروزين (بما في ذلك عامل النمو المشتق من الصفائح الدموية، وعامل نمو الأرومة الليفية، وعامل نمو بطانة الأوعية الدموية)،[18] وأظهرت تجربة سريرية عشوائية أنه يقلل من انخفاض وظائف الرئة والتفاقم الحاد للحالة.[19]
- الأدوية المضادة للالتهاب لها دور محدود فقط في الحد من عملية التليف. وقد تستجيب بعض الأنواع الأخرى من التليف، مثل الالتهاب الرئوي الخلالي اللانوعي للعلاج المثبط للمناعة، مثل الكورتيكوستيرويدات. ومع ذلك، لا يستجيب إلا أقلية من المرضى للكورتيكوستيرويدات وحدها؛ لذلك يمكن استخدام مثبطات إضافية للمناعة، مثل السيكلوفوسفاميد، والأزوثيوبرين، والميثوتريكسات، والبنسيلامين، والسيكلوسبورين، كما تم استخدام الكولشيسين أيضا في العلاح ولكن دوره محدود.[3] وهناك تجارب جارية مع أدوية جديدة، مثل إنترفيرون غاما.
- يتم منع التهاب فرط التحسس الرئوي، وهو شكل أقل حدة من التليف الرئوي، من أن يتفاقم عن طريق تجنب الاتصال مع المواد المسببة.
- يعمل العلاج بالأكسجين على تحسين نوعية الحياة والقدرة على التمارين الرياضية، ويمكن وضع زراعة الرئة لبعض المرضى في الاعتبار.[20]
- في المراحل الاولى من التعرض للتدخين والغبار المعدني ممكن ان تساعد عملية غسيل الرئة في ازاله الغبار من الرئة، وبالتالي منع وقوع ضرر .
توقع سير المرض
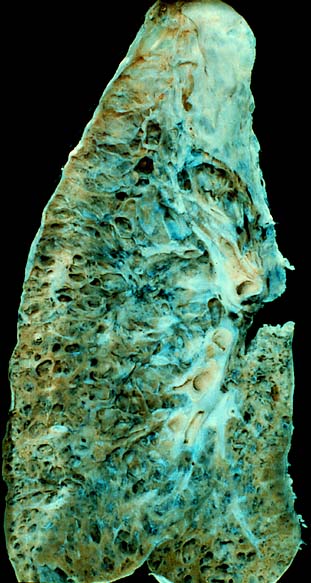
يمكن أن يؤدي نقص الأكسجة الناجم عن التليف الرئوي إلى ارتفاع ضغط الدم الرئوي، والذي بدوره يمكن أن يؤدي إلى فشل القلب في البطين الأيمن. ويمكن منع نقص الأكسجة من خلال تزويد المريض بالأكسجين.[3]
وقد يؤدي التليف الرئوي أيضًا إلى زيادة خطر الصمات الرئوية، التي يمكن منعها عن طريق مضادات التخثر.[3]
وبائيات
هناك خمسة ملايين شخص في جميع أنحاء العالم مصابون بالتليف الرئوي. وتم الإبلاغ عن مجموعة واسعة من معدلات حدوث وانتشار التليف الرئوي، والمعدلات أدناه لكل 100.000 شخص، وتعكس النطاقات معايير التضمين الضيقة والواسعة، على التوالي.
| مؤلفو الدراسة | معدل الحدوث | معدل الانتشار | السكان | السنوات التي تغطيها الدراسة | |
|---|---|---|---|---|---|
| راغو وآخرون [21] | -- | 6.8-16.3 | 14.0-42.7 | نظام معالجة المطالبات الصحية الأمريكية | 1996–2000 |
| فرنانديز بيريز وآخرون [22] | -- | 8.8-17.4 | 27.9-63.0 | مقاطعة أولمستيد، مينيسوتا | 1997–2005 |
| كولتاس وآخرون [23] | ذكور | 27.5 | 30.3 | مقاطعة برناليلو، نيو مكسيكو | 1988–1990 |
| إناث | 11.5 | 14.5 |
واستناداً إلى هذه المعدلات، يمكن أن يتراوح انتشار التليف الرئوي في الولايات المتحدة بين أكثر من 29000 إلى حوالي 132000 شخص استنادًا إلى عدد السكان في عام 2000 من عمر 18 عامًا أو أكثر. وقد تكون الأرقام الفعلية أعلى بكثير بسبب خطأ التشخيص. وعادة، يكون المرضى في الأربعينات والخمسينيات عند تشخيصهم في حين أن حالات الإصابة بالتليف الرئوي مجهول السبب تزداد بشكل كبير بعد سن الخمسين. ومع ذلك، فإن فقدان الوظيفة الرئوية يُنسب عادة إلى الشيخوخة أو أمراض القلب أو أمراض الرئة الأكثر شيوعًا.
المراجع
- ^ Q98547939، ص. 296، QID:Q98547939
- ^ Mayo Clinic Staff. "Definition [of pulmonary fibrosis]". Mayo Foundation for Medical Education and Research. مؤرشف من الأصل في 15 يوليو 2014. اطلع عليه بتاريخ 26 يوليو 2014.
- ^ أ ب ت ث ج ح خ د ذ "Pulmonary Fibrosis". MedicineNet, Inc. مؤرشف من الأصل في 19 يوليو 2014. اطلع عليه بتاريخ 26 يوليو 2014.
- ^ Mayo Clinic Staff. "Symptoms". Mayo Foundation for Medical Education and Research. مؤرشف من الأصل في 4 يوليو 2014. اطلع عليه بتاريخ 26 يوليو 2014.
- ^ أ ب ت ث ج MedlinePlus > Pulmonary Fibrosis نسخة محفوظة 5 July 2016 على موقع واي باك مشين. Date last updated: 9 February 2010
- ^ أ ب Mayo Clinic Staff. "Causes". Mayo Foundation for Medical Education and Research. مؤرشف من الأصل في 1 أكتوبر 2014. اطلع عليه بتاريخ 26 يوليو 2014.
- ^ Idiopathic pulmonary fibrosis - Genetics Home Reference - NIH نسخة محفوظة 26 سبتمبر 2018 على موقع واي باك مشين.
- ^ Hubbard R، Cooper M، Antoniak M، وآخرون (2000). "Risk of cryptogenic fibrosing alveolitis in metal workers". Lancet. ج. 355 ع. 9202: 466–467. DOI:10.1016/S0140-6736(00)82017-6. PMID:10841131.
- ^ "Not Found - BIDMC". bidmc.org. مؤرشف من الأصل في 16 مارس 2014. اطلع عليه بتاريخ 29 أبريل 2018.
- ^ Goemaere NN، Grijm K، van Hal PT، den Bakker MA (2008). "Nitrofurantoin-induced pulmonary fibrosis: a case report". J Med Case Reports. ج. 2: 169. DOI:10.1186/1752-1947-2-169. PMC:2408600. PMID:18495029. مؤرشف من الأصل في 6 مارس 2016.
- ^ Mayo Clinic Staff. "Complications". Mayo Foundation for Medical Education and Research. مؤرشف من الأصل في 4 يوليو 2014. اطلع عليه بتاريخ 26 يوليو 2014.
- ^ Gross TJ، Hunninghake GW (2001). "Idiopathic pulmonary fibrosis". N Engl J Med. ج. 345: 517–525. DOI:10.1056/NEJMra003200.
- ^ Walker J، Cooney M، Norton S (أغسطس 1989). "Improved pulmonary function in chronic quadriplegics after pulmonary therapy and arm ergometry". Paraplegia. ج. 27 ع. 4: 278–83. DOI:10.1038/sc.1989.42. PMID:2780083.
- ^ eMedicine Specialties > Pulmonology > Interstitial Lung Diseases > Restrictive Lung Disease نسخة محفوظة 5 March 2010 على موقع واي باك مشين. Author: Lalit K Kanaparthi, MD, Klaus-Dieter Lessnau, MD, Sat Sharma, MD. Updated: 27 July 2009
- ^ Mayo Clinic Staff. "Tests and diagnosis". Mayo Foundation for Medical Education and Research. مؤرشف من الأصل في 4 يوليو 2014. اطلع عليه بتاريخ 26 يوليو 2014.
- ^ "www.spirXpert.com". مؤرشف من الأصل في 28 يناير 2010.
- ^ King TE Jr؛ Bradford WZ؛ Castro-Bernardini S؛ وآخرون (مايو 2014). "A phase 3 trial of pirfenidone in patients with idiopathic pulmonary fibrosis". NEJM. ج. 370 ع. 22: 2083–2092. DOI:10.1056/NEJMoa1402582. PMID:24836312.
- ^ Richeldi L، Costabel U، Selman M، وآخرون (2011). "Efficacy of a tyrosine kinase inhibitor in idiopathic pulmonary fibrosis". N Engl J Med. ج. 365: 1079–1087. DOI:10.1056/nejmoa1103690. PMID:21992121.
- ^ Richeldi L، du Bois RM، Raghu G، وآخرون (مايو 2014). "Efficacy and Safety of Nintedanib in Idiopathic Pulmonary Fibrosis". N Engl J Med. ج. 370: 2071–2082. DOI:10.1056/NEJMoa1402584. PMID:24836310.
- ^ Mayo Clinic Staff. "Lifestyle and home remedies". Mayo Foundation for Medical Education and Research. مؤرشف من الأصل في 4 يوليو 2014. اطلع عليه بتاريخ 26 يوليو 2014.
- ^ Raghu G, Weycker D, Edelsberg J, Bradford WZ, Oster G. Incidence and Prevalence of Idiopathic Pulmonary Fibrosis. Am J Respir Crit Care Med. 2006;174:810-6.
- ^ Fernandez Perez ER, Daniels CE, Schroeder DR, St Sauver J, Hartman TE, Bartholmai BJ, Yi ES, Ryu JH. Incidence, Prevalence, and Clinical Course of Idiopathic Pulmonary Fibrosis: A Population-Based Study. Chest. Jan 2010;137:129-37.
- ^ Coultas DB, Zumwalt RE, Black WC, Sobonya RE. The Epidemiology of Interstitial Lung Diseases. Am J Respir Crit Care Med. Oct 1994;150(4):967-72. cited by Michaelson JE, Aguayo SM, Roman J. Idiopathic Pulmonary Fibrosis: A Practical Approach for Diagnosis and Management. Chest. Sept 2000;118:788-94.
| تليف رئوي في المشاريع الشقيقة: | |