|
تضامنًا مع حق الشعب الفلسطيني |
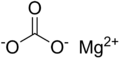
كربونات المغنيسيوم
| كربونات المغنيسيوم | |
|---|---|
| أسماء أخرى | |
Magnesite |
|
| المعرفات | |
| رقم CAS | 546-93-0 (anhydrous) 13717-00-5 (monohydrate), 5145-48-2 (dihydrate), 14457-83-1 (trihydrate), 61042-72-6 (pentahydrate) |
| بوب كيم (PubChem) | 11029 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| الخواص | |
| صيغة كيميائية | CMgO3 |
| كتلة مولية | 84.31 غ.مول−1 |
| المظهر | white solid استرطاب |
| الرائحة | odorless |
| الكثافة | 2.958 g/cm3 (anhydrous) 2.825 g/cm3 (dihydrate) 1.837 g/cm3 (trihydrate) 1.73 g/cm3 (pentahydrate) |
| نقطة الانصهار | 350 °س، 623 °ك، 662 °ف ( decomposes (anydrous) 165 °م (329 °ف؛ 438 ك) (trihydrate)) |
| الذوبانية في الماء | anhydrous: 0.0106 g/100ml (25 °C) 0.0063 g/100ml (100 °C)[2] pentahydrate: 0.375 g/100ml (20 °C)[بحاجة لمصدر] |
| حاصل الذوبانية، Ksp | 10−7.8[1] |
| الذوبانية | soluble in acid, aqueous ثنائي أكسيد الكربون insoluble in أسيتون، أمونياك |
| معامل الانكسار (nD) | 1.717 (anhydrous) 1.458 (dihydrate) 1.412 (trihydrate) |
| البنية | |
| البنية البلورية | نظام بلوري ثلاثي |
| كيمياء حرارية | |
| الحرارة القياسية للتكوين ΔfH |
-1113 kJ/mol[3] |
| إنتروبيا مولية قياسية S |
65.7 J/mol·K[2][3] |
| الحرارة النوعية، C | 75.6 J/mol·K[2] |
| المخاطر | |
| صحيفة بيانات سلامة المادة | ICSC 0969 |
| فهرس المفوضية الأوروبية | Not listed |
| NFPA 704 |
|
| نقطة الوميض | Non-flammable |
| حد التعرض المسموح به U.S | TWA 15 mg/m3 (total) TWA 5 mg/m3 (resp) ْْْْْْْ |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
كربونات المغنيسيوم هو مركب كيميائي له الصيغة MgCO3، ويكون على شكل ملح أبيض اللون لا يذوب في الماء، وله استخدامات عديدة علاجياً وصناعياً وصيدلانياً.
الخصائص
مسحوق أبيض ضخم عديم الرائحة، أو كتل خفيفة بيضاء هشة، عديم الانحلال عملياً في الماء، ولا ينحل في الكحول، لكن ينحل في الحموض الممدة مع فوران.
الاستعمالات
- علاجياً: تستعمل كربونات الماغنسيوم كمادة مضادة للحموضة، كما أن لها تأثيراً مسهلاً تناضحياً.
- صناعيا: يدخل في صناعة معجون الأسنان وأدوات التجميل كالكريمات ويستخدم أيضا كمادة مالئة لتقوية البلاستيك وزيادة صلابته عند التصنيع.[4]
الاستخدام الصيدلاني
يُستعمل كممدد في المضغوطات والمحافظ حيث يُستعمل بشكل رئيسي في مضغوطات الضغط المباشر بتراكيز أعلى من 45% وزن/وزن، كما يُستخدم أيضاً لادمصاص السوائل الداخلة في تركيب المضغوطة كالمطعمات و تُعد كربونات المغنيسيوم غذاءً إضافياً ، أما علاجياً فيُستخدم كمضاد للحموضة.
التأثير على صحة الجسم
-تم تصنيف كربونات المغنيسيوم في فئة المواد غير السامة غير المخرشة لكن كما هو معروف فإن استخدام أملاح المغنيسيوم و منها كربونات المغنيسيوم هو مُضاد استطباب لدى المصابين بقصور كلوي.
-يتفاعل كربونات المغنيسيوم في المعدة مع الحموضة المعديّة مشكلاً ملح كلوريد المغنيزيوم الذوّاب و ثنائي أكسيد الكربون، لذلك لا يُنصح باستخدام كربونات المغنيسيوم كمُضاد للحموضة للأشخاص الذين لا يحتملون حركة غاز ثاني أكسيد الكربون داخل المعدة.
يُمتص جزء من المغنيزيوم و يُطرح عن طريق البول، كما يملك كربونات المغنيزيوم خصائص مليّنة كأملاح المغنيزيوم الأخرى و قد يُحدث إسهالات.
حفظ المادة
يجب أن يحفظ في عبوات محكمة الإغلاق في أماكن جافة و باردة.
اقرأ أيضاً
المراجع
- ^ Bénézeth, Pascale, et al. "Experimental determination of the solubility product of magnesite at 50 to 200 C." Chemical Geology 286.1 (2011): 21-31.
- ^ أ ب ت magnesium carbonate نسخة محفوظة 31 أغسطس 2017 على موقع واي باك مشين.
- ^ أ ب Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. ص. A22.
- ^ استفسارات - بيوتات الكيمياء التعليمية. نسخة محفوظة 04 مارس 2016 على موقع واي باك مشين.
| في كومنز صور وملفات عن: كربونات المغنيسيوم |