|
تضامنًا مع حق الشعب الفلسطيني |
خلية دبقية صغيرة
| خَلية دِبقية صَغيرة | |
|---|---|
| الاسم العلمي Microglia |
|
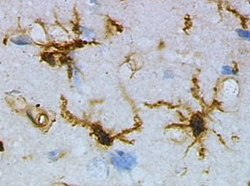
خَلية دِبقية صَغيرة مأخوذة من قِشرة جُرذ قَبل إصابته في الدِماغ
| |
| تفاصيل | |
| تعديل مصدري - تعديل |
الخَلية الدِبقية الصَغيرة (بالإنجليزية: Microglia) هي إحدى أنواع من الخلايا الدبقية الموجودة في الدماغ والحبل الشوكي.[1] تكوِّن الخلايا الدبقية الصغيرة نحو 10 إلى 15% من الخلايا الموجودة في الدماغ. تقوم تلك الخلية بدور خط الدفاع المناعي الأول في الجهاز العصبي المركزي؛ لقيامها بدور الخلايا البلعمية المقيمة. تنتشر الخلايا الدبقية الصغيرة (وغيرها من الخلايا الدبقية مثل الخلية النجمية) في مناطق واسعة غير متقاطعة في الجهاز العصبي المركزي.[2][3] تمثل الخلايا الدبقية الصغيرة حجر الأساس في حماية الدماغ، إذ تنظف الدماغ من العصبونات والوصلات العصبية غير الضرورية والخلايا الميتة والعدوى باستمرار.[4] تستشعر الخلايا الدبقية الصغيرة أصغر تغير مرضي نظراً لحساسيتها الشديدة، وتُعتبر العمليات التي تقوم بها شديدة الأهمية في حماية الدماغ من أي تلف قاتل. تتحقق تلك الحساسية نتيجة وجود قنوات البوتاسيوم الفريدة من نوعها، التي تستجيب لأصغر التغيرات في البوتاسيوم خارج الخلية.[4]
يتكون الجهاز العصبي المركزي من الدماغ والحبل الشوكي، ولا تتأثر تلك الأعضاء مباشرة بالعوامل المرضية التي يتأثر بها الجسم؛ لأنها محاطة بتركيبات معقدة وخلايا البطانة الغشائية، يُسمى هذا التركيب الحاجز الدموي الدماغي. يمنع الحاجز الدموي الدماغي أي عدوى من الوصول مباشرة للدماغ، وإذا عبرت العدوى، تستجيب الخلية الدبقية الصغيرة بسرعة لتقليل الالتهاب وتدمير المعديات قبل إتلاف النسيج العصبي الحساس. لا تعبر الأجسام المضادة الموجودة في الجسم إلى الدماغ، باستثناء بعض الأجسام المضادة صغيرة الحجم التي تتمكن من عبور الحاجز الدموي الدماغي، ونتيجة لذلك، تعمل الخلايا الدبقية الصغيرة بدورها في التعرف على الأجسام الغريبة والتهامها والعمل بوظيفة الخلية المقدمة للمستضد، وتنشيط الخلايا التائية.
الأشكال
تتميز الخلايا الدبقية الصغيرة بلدونة عالية، فتمر بدرجة عالية من التغيرات التركيبية بناءً على احتياجات الجهاز والموقع الذي توجد بهما الخلية. تؤدي تلك اللدونة وظائف عديدة مطلوبة من الخلايا الدبقية الصغيرة. تتميز الخلايا الدبقية الصغيرة بتلك القدرة على تغيير تركيبها على خلاف الخلايا البلعمية، التي يجب تغييرها بصورة منتظمة، ما يساعد الخلايا الدبقية على حماية الجهاز العصبي المركزي دون إحداث اختلال مناعي. تتبنى الخلية الدبقية الصغيرة النمط الظاهري الخاص بها استجابةً للظروف المحلية والإشارات الكيميائية التي تعرفت عليها.[5]
وراثيات السينسوم
يُعتبر مفهوم السينسوم في الخلايا الدبقية الصغيرة من المفاهيم الجديدة في البيولوجيا، ويظهر أنه يلعب دوراً كبيراً في النماء العصبي والتنكس العصبي. يُشير السينسوم إلى مجموعة فريدة من نسخ البروتينات المستخدمة لاستشعار الربيطة والميكروبات. أو بعبارة أخرى، يمثل السينسوم الجينات المطلوبة لتكوين البروتينات التي تستشعر الجزيئات الموجودة في الجسم. يمكن تحليل السينسوم عبر العديد من الوسائل ومنها تفاعل البوليميراز المتسلسل اللحظي وتسلسل الحمض النووي الريبوزي ومصفوفة دي إن إيه دقيقة، وتسلسل دي إن إيه المباشر. تشفر الجينات المعنية بالسينسوم لمستقبلات وبروتينات عبر غشائية في غشاء الخلية، تُمثَّل على سطح الخلايا الدبقية الصغيرة بصورة تفوق تمثيلها على العصبونات. لا تشمل هذه الجينات البروتينات المفرزة أو البروتين عبر الغشائي المعنيّ بعضيات الغشاء أو العضيات المرتبطة به، مثل النواة، والميتوكوندريا والشبكة الإندوبلازمية. تشفر جينات السينسوم المعروفة لمستقبلات التعرف على الأنماط، بالإضافة لمختلف الجينات الأخرى المشتركة في عملية التشفير. تتشابه الخلايا الدبقية الصغيرة مع الخلايا البلعمية من ناحية السينسوم، ولكن الخلايا الدبقية الصغيرة تتميز بوجود 22 جين فريد آخر، يُستخدم 16 منها للتفاعل مع الربيطات الداخلية. تصنع تلك الاختلافات واسمات بيولوجية فريدة للخلايا الدبقية الصغيرة، وتشمل ما يزيد عن 40 جين منها بي 2 واي 12 وHEXB. يلعب دي إيه بي 12 دوراً مهماً في تفاعل السينسوم مع البروتين، ويعمل في التأشير ويقوم بوظيفة البروتين المنظم.[6]
يجب أن يكون تفعيل جينات السينسوم قادراً على التغيير استجابةً للأخطار المحتملة. قد تقوم الخلايا الدبقية الصغيرة بدور الحماية العصبية أو السمية العصبية لمواجهة الأخطار المحتملة. لهذه الأسباب، يُعتقد أن السينسوم يلعب دوراً في التنكس العصبي. يزداد تفعيل بعض جينات السينسوم مع تقدم العمر، وتلك الجينات معنية غالباً باستشعار ربيطات الميكروبات المعدية، بينما التي يقل تفعيلها معنية غالباً بالربيطات الداخلية. يقترح هذا التحليل تنظيماً خاصاً بالخلايا الدبقية لتفضيل وظيفة الحماية العصبية عن التنكس العصبي. هذا على عكس التحول باتجاه السمية العصبية الذي نراه في حالة أمراض التنكس العصبي.[7]
يمكن أن يلعب السينسوم أيضاً وظيفة النماء العصبي. تؤدي العدوى المبكرة للدماغ في الخلايا الدبقية الصغيرة إلى جعلها شديدة الحساسية لأي محفز مناعي. يزداد تفعيل جينات السينسوم المعنية بالالتهاب العصبي عند التعرض للعدوى، ويقل تفعيل جينات السينسوم المسؤولة عن السمية العصبية. ربما يقدر السينسوم على التأثير في النماء العصبي ومكافحة الأمراض.[8]
المتشعبة
يوجد هذا الشكل بصورة شائعة في مواقع محددة في الدماغ والحبل الشوكي في غياب المواد الغريبة أو الخلايا الميتة. تتكون هذه الحالة «الساكنة» من الخلايا الدبقية الصغيرة من زوائد شجيرية طويلة وجسم خلوي صغير. يظل جسم الخلية في مكانه عند تحرك الفروع واستكشافها للمناطق المحيطة، على عكس ما يحدث في الأشكال الأميبية. تستجيب الفروع إلى التغيرات الصغيرة للغاية في الحالة الفسيولوجية، وتحتاج إلى مزارع شديدة التحديد للمتابعة خارج الكائن الحي.
لا تبتلع الخلايا الدبقية الصغيرة المتشعبة غيرها من الخلايا وتفرز القليل من الجزيئات المناعية (مثل بروتينات معقد التوافق النسيجي الكبير من النوعين الأول والثاني)، على عكس الخلايا الدبقية الصغيرة الأميبية أو النشطة. في هذه الحالة تتمكن الخلايا الدبقية الصغيرة من البحث عن الأخطار المناعية والتعرف عليها أثناء محافظتها على الاستتاب في الجهاز العصبي المركزي. تنشط الخلايا الدبقية الصغيرة في هذا الوضع بشدة، بالرغم من أنه وضع سكون، وتستكشف البيئة من حولها كيميائياً. تتحول الخلايا الدبقية الصغيرة المتشعبة إلى الحالة النشطة في أي وقت استجابةً للإصابة أو التهديد.[9][10][11]
التفاعلية
بالرغم من استخدام مصطلح الخلايا «النشطة» تاريخياً، لكن المصطلح الذي يجب استخدامه هو الخلايا «التفاعلية». لا تخلو الخلايا الدبقية الصغيرة الساكنة من الوظائف النشطة، لذلك فإن مصطلح «النشطة» مضلل قليلاً؛ إذ يشير إلى حالة «الكل أو لا شيء» بالنسبة لاستقطاب الخلية وتفاعلاتها. يُستخدم واسم الطعم الخيفي الالتهابي 1، الذي يزيد تفعيله في الخلايا الدبقية الصغيرة التفاعلية، لرؤية هذه الخلايا.[12]
لا بلعمية
تُعتبر تلك الحالة جزءًا من الاستجابة المتدرجة، إذ تنتقل الخلايا الدبقية الصغيرة من الشكل التشعبي إلى الشكل كامل النشاط البلعمي. تنشط الخلايا الدبقية نتيجة العديد من العوامل منها السيتوكين المشجع على الالتهاب وعوامل نخر الخلية والدهون عديدة السكريات والتغيرات في البوتاسيوم اللا خلوي (المشير لتمزق الخلية). تدخل الخلية في العديد من التغيرات المورفولوجية الأساسية بمجرد تفعيلها، منها زيادة السُمك وانسحاب الفروع، واستيعاب معقد التوافق النسيجي الكبير وإنتاج الجزيئات المناعية وإفراز المواد الخلوية السمية وإفراز جزيئات التجنيد وإفراز جزيئات التأشير المشجعة على الالتهاب (ما يؤدي إلى سلسلة من الإشارات المشجعة على الالتهاب). تظهر الخلايا الدبقية الصغيرة اللا بلعمية في صورة «شجيرية» أو «عصوية» أو في حالة أميبية صغيرة، بناءً على المدى الذي اتخذته الخلية في تحولها من الحالة المتشعبة إلى الحالة البلعمية الكاملة. تدخل الخلايا البلعمية في حالة تكاثر سريعة لزيادة عددها. من الناحية المورفولوجية البحتة، يرتبط الاختلاف في شكل الخلايا الدبقية الصغيرة بالتغير في التركيب المورفولوجي، ويمكن قياسه باستخدام وسائل التحليل الكسوري، التي أثبتت حساسيتها للتغيرات الطفيفة غير المرئية، المرتبطة بالمورفولوجيا المختلفة في الحالات المرضية المختلفة.
المراجع
- ^ Ginhoux F، Lim S، Hoeffel G، Low D، Huber T (2013). "Origin and differentiation of microglia". Frontiers in Cellular Neuroscience. ج. 7: 45. DOI:10.3389/fncel.2013.00045. PMC:3627983. PMID:23616747.
- ^ Kreutzberg GW (مارس 1995). "Microglia, the first line of defence in brain pathologies". Arzneimittel-Forschung. ج. 45 ع. 3A: 357–60. PMID:7763326.
- ^ Bushong EA، Martone ME، Jones YZ، Ellisman MH (يناير 2002). "Protoplasmic astrocytes in CA1 stratum radiatum occupy separate anatomical domains". The Journal of Neuroscience. ج. 22 ع. 1: 183–92. DOI:10.1523/JNEUROSCI.22-01-00183.2002. PMID:11756501.
- ^ أ ب Gehrmann J، Matsumoto Y، Kreutzberg GW (مارس 1995). "Microglia: intrinsic immuneffector cell of the brain". Brain Research. Brain Research Reviews. ج. 20 ع. 3: 269–87. DOI:10.1016/0165-0173(94)00015-H. PMID:7550361.
- ^ Verkhratsky، Alexei؛ Butt، Arthur (2013). Glial physiology and pathophysiology. Chicester: John Wiley & Sons. ISBN:978-1118402054.
{{استشهاد بكتاب}}: الوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة)[بحاجة لرقم الصفحة] - ^ Hickman SE، Kingery ND، Ohsumi TK، Borowsky ML، Wang LC، Means TK، El Khoury J (2013). "The microglial sensome revealed by direct RNA sequencing". Nature Neuroscience. ج. 16 ع. 12: 1896–905. DOI:10.1038/nn.3554. PMC:3840123. PMID:24162652.
- ^ Block, M.L., Zecca, L. & Hong, J.S. Microglia-mediated neurotoxicity: uncovering the molecular mechanisms. Nat. Rev. Neurosci. 8, 57–69 (2007).
- ^ Horiuchi M، Smith L، Maezawa I، Jin LW (2017). "CX3CR1 ablation ameliorates motor and respiratory dysfunctions and improves survival of a Rett syndrome mouse model". Brain, Behavior, and Immunity. ج. 60: 106–116. DOI:10.1016/j.bbi.2016.02.014. PMC:5531048. PMID:26883520.
- ^ Davis EJ، Foster TD، Thomas WE (1994). "Cellular forms and functions of brain microglia". Brain Research Bulletin. ج. 34 ع. 1: 73–8. DOI:10.1016/0361-9230(94)90189-9. PMID:8193937.
- ^ Aloisi F (نوفمبر 2001). "Immune function of microglia". Glia. ج. 36 ع. 2: 165–79. DOI:10.1002/glia.1106. PMID:11596125.
- ^ Christensen RN، Ha BK، Sun F، Bresnahan JC، Beattie MS (يوليو 2006). "Kainate induces rapid redistribution of the actin cytoskeleton in ameboid microglia". Journal of Neuroscience Research. ج. 84 ع. 1: 170–81. DOI:10.1002/jnr.20865. PMID:16625662.
- ^ Lan X، Han X، Li Q، Yang QW، Wang J (يوليو 2017). "Modulators of microglial activation and polarization after intracerebral haemorrhage". Nat Rev Neurol. ج. 13 ع. 7: 420–433. DOI:10.1038/nrneurol.2017.69. PMC:5575938. PMID:28524175.
- Staff members of Histology & Cell biology Department (2015),Alex. Univ. Human Histology II. p. 40
| في كومنز صور وملفات عن: خلية دبقية صغيرة |