إكسيميا (فينترمين/توبيراميت)
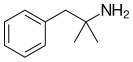
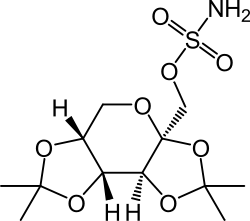
مزيج من الأدوية فنترمين وتوبيراميت (الاسم التجاري إكسيمياQsymia، سابقاQnexa) هو دواء لإستكشاف علاج البدانة والحالات ذات الصلة مثل السكري من النوع 2 ولقد وجد أنه قادر على خفض ضغط الدم ونسبة الكوليسترول.[1] ويجري تطوير Qsymia بواسطة Vivus ، وهي شركة أدوية مقرها كاليفورنيا.[2] فنترمين هو دواء مثبط للشهية ومنبه من المنشطات من فئة الأمفيتامين والفينيثيلامين .أما توبيراميت فهو عقار مضاد للصرع بسبب خسارة الوزن كأثر جانبى.
| إكسيميا (فينترمين/توبيراميت) | |
|---|---|
| مزيج من | |
| Phentermine | مفقد الشهية/منبه (مادة) of the أمفيتامين and فينيثيلامين class |
| Topiramate | مضاد اختلاج |
| اعتبارات علاجية | |
| اسم تجاري | Qsymia |
| فئة السلامة أثناء الحمل | X (الولايات المتحدة) |
| طرق إعطاء الدواء | Oral |
| معرّفات | |
| ك ع ت | None |
| بوب كيم | CID 56842108 |
| تعديل مصدري - تعديل | |
في 22 فبراير 2012، صوت مستشارو إدارة الاغذية والعقاقير 20:02 بأن توصي إدارة الأغذية والأدوية الأميريكية باعتماد فنترمين / توبيراميت كعلاج للسمنة.[3] وكان من المتوقع الموافقة النهائية في وقت لاحق في عام 2012، مع توصيات بمراقبة نبض السوق لرصد المخاطر على القلب والأوعية الدموية، وإشارة إلى إستخدامه من قبل النساء الحوامل.[3] في 17 يوليو عام 2012، وافقت إدارة الغذاء والدواء الأمريكية بإضافة إكسيميا Qsymia إلى نظم اتباع نظام غذائي مخفض السعرات الحرارية وممارسة الرياضة للسيطرة على عوارض السمنة المزمنة. .[4]
السلامة والفعالية
الدراسات السريرية أظهرت خسارة الوزن تحت العلاج بعقارQnexa . المرحلة 3 التي تشمل, 56-أسبوعا دراسة EQUIP أظهرت أن فقدان الوزن بمعدل متوسطه 14.7% (37 رطل) تم تحقيقه من قبل المرضى الذين يعانون من السمنة المفرطة الخاضعين للعلاج بعقار كنيكسا Qnexa.[5] الحرعات التالية من فينترمين IR (تحرر سريع) وتوبيراميت CR (إطلاق زمنى) أستخدمت في اختبارات المرحلة الثالثة
- تركيبة كاملة التركيز: 15 مج من الفنترمين (تحرر سريع) و 92 مج من توبيراميت CR (إطلاق زمنى)
- تركيبة متوسطة التركيز: 7.5 مج من الفنترمين (تحرر سريع) و 46 مج توبيراميت (إطلاق زمنى)
- تركيبة منخفضة التركيز: 3.75 مج الفنترمين (تحرر سريع) و 23 مج توبيراميت
(إطلاق زمنى)
في عام 2009، ذكرت Vivus أن الآثار الجانبية الرئيسية خلال مراحل الاختبار كانت جفاف الفم ، ووخز في أصابع اليدين والقدمين والإمساك.[6] ومع ذلك، في عام 2010 فإن مؤسسة بابليك سيتيزن أدلى الدكتور سيدني وولف م بشهادته أمام اللجنة الاستشارية لإدارة الاغذية والعقاقير ان الدراسات اظهرت ان Qnexa يحمل قائمة طويلة من الآثار الجانبية الخطيرة، بما في ذلك إمكان حدوث عيوب خلقية للأجنة[7]
الدراسات والجدول الزمني
EQUIP
EQUIP المتابعة مع مجموعة لمدة 56 أسبوعا في المرضى الذين يعانون من السمنة المفرطة الشديدة.[8]
CONQUER
56 أسبوعا لمحاولة تحكمها السلامة والفعالية، نشرت في اللانسيت .[9]
SEQUEL
108 أسبوع محاولة للتحكم بين أكثر المرضى من CONQUER، وجمع البيانات في الأجل الطويل.[10]
تاريخ الإجازة
في 28 ديسمبر 2009 م تطبيق دواء جديد (NDA) قدمت إلى هيئة الدواء والغذاء الفيدرالية للموافقة عليها[11] وبتاريخ 1 مارس 2010، أعلن [فيفوس] أن الوكالة قبلت تطبيق الدواء الجديد.[12]
تم رفض موافقة إدارة الاغذية والأدوية في شهر أكتوبر عام 2010 بسبب المخاوف بشأن الآثار الجانبية الخطيرة، بما في ذلك الأفكار الانتحارية، وخفقان القلب، وهفوات الذاكرة والعيوب الخلقية.[13]
في يناير 2011 ، أعربت إدارة الغذاء والدواء عن قلقها إزاء احتمال أن يسبب [ Qnexa ] تشوهات خلقية، وطالبت [فيفوس] بدراسة هذا الاحتمال قبل أن تتم الموافقة على الدواء.[14]
تم تغيير اسم [قنإكسا] إلى إكسيميا وتم إقراره للبيع في 17 يوليو 2012 من قبل إدارة الغذاء والدواء [15][16]
مراجع
- ^ Vivus Inc., نسخة محفوظة 04 مارس 2016 على موقع واي باك مشين.[وصلة مكسورة]
- ^ Vivus Inc.[وصلة مكسورة] نسخة محفوظة 20 يونيو 2012 على موقع واي باك مشين.
- ^ أ ب "FDA advisors endorse weight-loss drug Qnexa". latimes.com. 02/23/2012. مؤرشف من الأصل في 5 مارس 2012. اطلع عليه بتاريخ 23 February 2012.
{{استشهاد ويب}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - ^ FDA approves weight-management drug Qsymia نسخة محفوظة 18 يناير 2017 على موقع واي باك مشين. "نسخة مؤرشفة". مؤرشف من الأصل في 2017-01-18. اطلع عليه بتاريخ 2019-05-25.
{{استشهاد ويب}}: صيانة الاستشهاد: BOT: original URL status unknown (link) - ^ Vivus Phase 3 studies find Qnexa effective in tackling obesity نسخة محفوظة 22 سبتمبر 2015 على موقع واي باك مشين.
- ^ Vivus Says Qnexa, a Diet Drug, Did Well in Trials نسخة محفوظة 21 مايو 2013 على موقع واي باك مشين.
- ^ Weight Loss Drug أخطر من أن يسمح له بالتداول في السوق نسخة محفوظة 11 أغسطس 2016 على موقع واي باك مشين.
- ^ إطلاق زمنى فينترمين / توبيراميت في حالات السمنة الشديدة للبالغين ,محاولة متحكم فيها عشوائيا (EQUIP), [1][وصلة مكسورة] "نسخة مؤرشفة". مؤرشف من الأصل في 2020-03-13. اطلع عليه بتاريخ 2020-04-13.
{{استشهاد ويب}}: صيانة الاستشهاد: BOT: original URL status unknown (link) - ^ آثار جرعة منخفضة, إطلاق زمنى, تركيب فنترمين + توبيراميت على الوزن وأمراض المصاحبة المرتبطة بها في البالغين الذين يعانون من زيادة الوزن والسمنة(CONQUER)., [2][وصلة مكسورة] "نسخة مؤرشفة". مؤرشف من الأصل في 2020-03-13. اطلع عليه بتاريخ 2020-04-13.
{{استشهاد ويب}}: صيانة الاستشهاد: BOT: original URL status unknown (link) - ^ لمدة عامين وفقدان الوزن المطرد والفوائد الأيضية مع تسيطر عليها الافراج عن فنترمين / توبيراميت في البالغين يعانون من السمنة المفرطة وزيادة الوزن
(SEQUEL), [3][وصلة مكسورة] "نسخة مؤرشفة". مؤرشف من الأصل في 2020-03-13. اطلع عليه بتاريخ 2020-04-13.
{{استشهاد ويب}}: صيانة الاستشهاد: BOT: original URL status unknown (link) - ^ VIVUS Submits Qnexa(R) New Drug Application to the FDA for the Treatment of Obesity نسخة محفوظة 07 أكتوبر 2012 على موقع واي باك مشين.
- ^ FDA accepts Vivus application for obesity drug نسخة محفوظة 11 أكتوبر 2012 على موقع واي باك مشين.
- ^ "FDA rejects second weight-loss drug in a week". msnbc.com news services. 10/29/2010 5:06:32 AM ET. مؤرشف من الأصل في 4 نوفمبر 2012. اطلع عليه بتاريخ 29 October 2010.
{{استشهاد ويب}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - ^ Vivus says FDA asks about Qnexa birth defect link, Business Week, January 21, 2011 نسخة محفوظة 4 أبريل 2019 على موقع واي باك مشين. "نسخة مؤرشفة". مؤرشف من الأصل في 2015-09-23. اطلع عليه بتاريخ 2013-09-04.
{{استشهاد ويب}}: صيانة الاستشهاد: BOT: original URL status unknown (link) - ^ Hellmich، Nancy. "New diet drug helps patients lose about 10% of weight". USA Today. مؤرشف من الأصل في 2012-07-24. اطلع عليه بتاريخ 2012-07-17.
- ^ "Medications Target Long-Term Weight Control". FDA.gov. مؤرشف من الأصل في 2019-04-24. اطلع عليه بتاريخ 2012-07-17.