|
تضامنًا مع حق الشعب الفلسطيني |
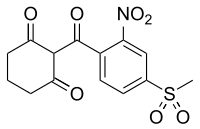
ميزوتريون
| ميزوتريون | |
|---|---|
| الاسم النظامي (IUPAC) | |
2-(4-mesyl-2-nitrobenzoyl)cyclohexane-1,3-dione |
|
| التسمية المفضلة للاتحاد الدولي للكيمياء البحتة والتطبيقية | |
2-[4-(Methylsulfonyl)-2-nitrobenzoyl]cyclohexane-1,3-dione |
|
| أسماء أخرى | |
زا1296 |
|
| المعرفات | |
| رقم CAS | 104206-82-8 |
| بوب كيم (PubChem) | 175967 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| الخواص | |
| صيغة كيميائية | C14H13NO7S |
| كتلة مولية | 339.32 غ.مول−1 |
| المظهر | مادة صلبة صفراء أو سمراء اللون |
| الكثافة | 1.49 غرام/سنتيمتر3 |
| نقطة الانصهار | 165.3 °س، 438 °ك، 330 °ف |
| الذوبانية في الماء | 1500 ملليغرام/لتر(20 °C) |
| log P | 0.11 |
| حموضة (pKa) | 3.12 |
| المخاطر | |
| رمز الخطر وفق GHS |  |
| وصف الخطر وفق GHS | تحذير |
| بيانات الخطر وفق GHS | H400, H410 |
| بيانات وقائية وفق GHS | P273, P391, P501 |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
ميزوتريون هو الاسم الشائع لمركب عضوي يستخدم كمبيد أعشاب انتقائي وخاصة في محاصيل الذرة.[1]
يُعتبر الميزوتريون مادة اصطناعية مستوحاة من مادة الليبتوسبيرمون الطبيعية، والتي تمنع إنزيم 4-هيدروكسي فينيل البيروفات ديوكسيجيناز.[2] كانت شركة سينغنتا هي التي طرحت مبيد الميزوتريون لأول مرة في الأسواق عام 2001، وكان يُباع تحت العديد من الأسماء التجارية ومنها تيناسيتي، وكاليستو.[3]
لمحة تاريخية
بدأ اختراع فئة مركبات التريكيتون من مبيدات الأعشاب في عام 1977 بعد ملاحظة وجود نشاط لمكافحة الحشائش الأليلوباثية بالقرب من شجرة الفرشاة. حدد الكيميائيون في شركة ستوفر للكيماويات بعد ذلك المركب المسؤول عن هذا النشاط، وعُرف باسم ليبتوسبيرمون، وهو منتج طبيعي معروف سابقًا،[4] ولكن حتى ذلك الوقت لم يكن معروف بأن له نشاط حيوي. أدى العمل المكثف على تطوير نظائر هذا المركب إلى اكتشاف وتطوير مركبات جديدة مثل سالكوترين، وميزوتريون.[5][6][7]
التحضير

وُصفت طريقة تحضير مركب الميزوتريون لأول مرة في براءات الاختراع المقدمة من إمبريال للصناعات الكيماوية،[8][9] وتلك التي حصلت عليها شركة ستوفر للكيماويات في عام 1987.[10] وتتضمن طريقة تحضير مركب الميزوتريون تفاعل مركب 1،3-سيكلوهكسانيدون مع كلوريد حمض 4- (ميثيل سلفونيل) -2- نيترو البنزينويك في ظل ظروف التي تتفاعل فيها مجموعة هيدروكسيل الإينوليك في مجموعة الديكيتون لتكوين مشتق البنزويل. وفي خطوة منفصلة، يتم إعادة ترتيب كل هذا إلى ميزوتريون باستخدام كمية محفزة من أيون السيانيد المشتق من سيانوهيدرين الأسيتون.

آلية العمل
يثبط مبيد الميزوتريون إنزيم 4-هيدروكسي فينيل البيروفات ديوكسيجيناز،[2] وهو مثبط قوي للغاية لإنزيم 4-هيدروكسي فينيل البيروفات ديوكسيجيناز في الاختبارات المعملية التي أجريت باستخدام نبات رشاد أذن الفأر.[5] يعد إنزيم 4-هيدروكسي فينيل البيروفات ديوكسيجيناز ضروريًا للتخليق الحيوي للتوكوفيرول والبلاستوكينون في النباتات، وهو أمر ضروري لإنتاج الكاروتين. ويؤدي تثبيط هذا المسار في النهاية إلى تبييض الأوراق حيث يتحلل الكلوروفيل، ثم موت النبات في نهاية المطاف.[5][11]
المراجع
- ^ "Compendium of Pesticide Common Names: mesotrione". BCPC. مؤرشف من الأصل في 2022-01-24.
- ^ أ ب Moran، GR (يناير 2005). "4-Hydroxyphenylpyruvate dioxygenase" (PDF). Archives of Biochemistry and Biophysics. ج. 433 ع. 1: 117–28. DOI:10.1016/j.abb.2004.08.015. PMID:15581571. مؤرشف من الأصل (PDF) في 2014-03-03.
- ^ Uttley، Nigel (3 يونيو 2011). "Product Profile: Mesotrione". AgriBusiness global. مؤرشف من الأصل في 2017-12-01. اطلع عليه بتاريخ 2020-03-28.
- ^ Hellyer، R.O. (1968). "The occurrence of β-triketones in the steam-volatile oils of myrtaceous Australian plants". Aust. J. Chem. ج. 21 ع. 11: 2825–2828. DOI:10.1071/CH9682825.
- ^ أ ب ت Beaudegnies، Renaud؛ Edmunds، Andrew J.F.؛ Fraser، Torquil E.M.؛ Hall، Roger G.؛ Hawkes، Timothy R.؛ Mitchell، Glynn؛ Schaetzer، Juergen؛ Wendeborn، Sebastian؛ Wibley، Jane (2009). "Herbicidal 4-hydroxyphenylpyruvate dioxygenase inhibitors—A review of the triketone chemistry story from a Syngenta perspective". Bioorganic & Medicinal Chemistry. ج. 17 ع. 12: 4134–4152. DOI:10.1016/j.bmc.2009.03.015. PMID:19349184.
- ^ Knudsen، Christopher G.؛ Lee، David L.؛ Michaely، William J.؛ Chin، Hsiao-Ling؛ Nguyen، Nhan H.؛ Rusay، Ronald J.؛ Cromartie، Thomas H.؛ Gray، Reed؛ Lake، Byron H.؛ Fraser، Torquil E. M.؛ Cartwright، David (2000). "Discovery of the triketone class of HPPD inhibiting herbicides and their relationship to naturally occurring β-triketones". Allelopathy in Ecological Agriculture and Forestry. ص. 101–111. DOI:10.1007/978-94-011-4173-4_7. ISBN:978-94-010-5817-9.
- ^ Derek Cornes (2005). "Callisto: a very successful maize herbicide inspired by allelochemistry". Fourth World Congress on Alleopathy. The Regional Institute Ltd. مؤرشف من الأصل في 2022-01-27. اطلع عليه بتاريخ 2020-03-28.
- ^ US patent 5006158, Carter, C.G.; Lee, D.L. & Michaely, W.J. et al., "Certain 2-(2-substituted benzoyl)-1,3-cyclohexanediones", issued 1991-04-09, assigned to ICI Americas Inc
- ^ Mitchell، Glynn؛ Bartlett، David W.؛ Fraser، Torquil E.M.؛ Hawkes، Tim R.؛ Holt، David C.؛ Townson، Jane K.؛ Wichert، Rex A. (2001). "Mesotrione: A new selective herbicide for use in maize". Pest Management Science. ج. 57 ع. 2: 120–128. DOI:10.1002/1526-4998(200102)57:2<120::AID-PS254>3.0.CO;2-E. PMID:11455642.
- ^ Hicks، Jonathan P. (6 يونيو 1987). "Imperial set to buy Stauffer". The New York Times. مؤرشف من الأصل في 2019-12-30. اطلع عليه بتاريخ 2020-03-28.
- ^ "Tenacity Herbicide". Syngenta. مؤرشف من الأصل في 2021-04-16.