|
تضامنًا مع حق الشعب الفلسطيني |
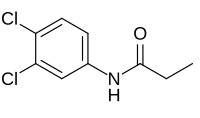
بروبانيل
| بروبانيل[1] | |
|---|---|
| التسمية المفضلة للاتحاد الدولي للكيمياء البحتة والتطبيقية | |
N-(3,4-Dichlorophenyl)propanamide |
|
| أسماء أخرى | |
أحادي'نيترو-3،4-ثنائي كلوروفينول البروبيوناميد |
|
| المعرفات | |
| رقم CAS | 709-98-8 |
| بوب كيم (PubChem) | 4933 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| الخواص | |
| الصيغة الجزيئية | C9H9Cl2NO |
| الكتلة المولية | 218.08 غرام/مول |
| المظهر | بلورات صلبة بيضاء اللون (في الحالة النقية)، ومسحوق بني اللون (في الحالة غير النقية) |
| نقطة الانصهار | 91 - 93 °س، 271 °ك، -44 °ف |
| الذوبانية في الماء | 225 ppm |
| المخاطر | |
| LD50 | 1384 mg/kg (rat, oral) |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
بروبانيل هو مبيد أعشاب يستخدم على نطاق واسع، وقد بلغ الاستهلاك العالمي منه نحو 8 ملايين رطل في عام 2001، كما يُعد البروبانيل أحد أكثر مبيدات الأعشاب استخدامًا على نطاق واسع في الولايات المتحدة الأمريكية،[2] ويقال إن البروبانيل يستخدم في زراعة ما يقرب من 400000 فدان من الإنتاج العالمي لمحاصيل الأرز كل عام.[3]
آلية العمل
تتمثل الآلية الرئيسية لعمل البروبانيل كمبيد للأعشاب والحشائش الضارة في تثبيط التمثيل الضوئي وتثبيت ثاني أكسيد الكربون. تقوم النباتات بعملية التمثيل الضوئي على مرحلتين، إذ تلتقط في المرحلة الأولى خلال تفاعلات التمثيل الضوئي طاقة ضوء الشمس وتنتج جزيئات ذات محتوى عالٍ من الطاقة، ثم تتفاعل هذه الجزيئات في المرحلة الثانية لالتقاط ثاني أكسيد الكربون، وينتج عن هذه التفاعلات سلائف الكربوهيدرات. يمتص جزيء الكلوروفيل في المرحلة الأولى من التفاعل فوتونًا واحدًا من الضوء ويفقد إلكترونًا واحدًا، ويبدأ تفاعل سلسلة نقل الإلكترون مما يؤدي إلى تفاعلات المرحلة الثانية.
يمنع البروبانيل تفاعل سلسلة نقل الإلكترون وتحويله من ثاني أكسيد الكربون إلى سلائف كربوهيدرات، مما يمنع نمو المزيد من الحشائش.[4]
يعتبر نبات الأرز محصنًا نسبيًا من تأثير البروبانيل ولكن معظم الحشائش تكون عرضة له، ويرجع السبب في هذه الانتقائية لحقيقة أن الأرز يحتوي على مستوى عالٍ من إنزيم أريل الأكيلاميداز، والذي يستقلب البروبانيل بسرعة ويحوله إلى مركب 3،4-ثنائي كلوروانيلين غير السام نسبيًا، بينما تفتقر الأعشاب الحساسة إلى ترميز الجينات لوجود إنزيم أريل الأكيلاميداز، لذا فإنها تستسلم لتأثير البروبانيل السام. ولكن تسبب الاستخدام المكثف للبروبانيل إلى جانب الانتخاب الطبيعي في الحشائش في أن تصبح بعض الأعشاب مقاومة للبروبانيل.[5]
التحضير
يُحضر البروبانيل صناعياً باستخدام مركب نترات 1،2-ثنائي كلورو البنزين لتكوين مركب 1،2-ثنائي كلورو-4-نيتروبنزين، متبوعًا بهدرجة مجموعة النيترو مع نيكل راني لينتج مركب 3،4-ثنائي كلورو الأنيلين. ثم ينتج البروبانيل عن أسيلة الأمين باستخدام كلوريد البروبانويل.[6] ويكون الناتج النهائي عبارة عن بلورات بيضاء أو بنية اللون.[7]

الدعاوى القضائية المتعلقة بحقوق الملكية وبراءة الاختراع
كانت حقوق ملكية وبراءة اختراع مركب البروبانيل موضوعاً للعديد من الدعاوى القضائية المتعلقة بالتعدي على حقوق الملكية وبراءات الاختراع. وقد قضت محكمة الاستئناف الأمريكية للدائرة الثالثة في إحدى هذه القضايا التي كان طرفاها هما شركة مونسانتو ضد شركة روم آند هاس بأن شركة مونسانتو قد ارتكبت احتيالًا على مكتب براءات الاختراع في الحصول على براءة الاختراع الخاصة بها لمنتج البروبانيل.[8]

حصلت شركة مونسانتو على براءة الاختراع من خلال تقديم بيانات إلى مكتب براءات الاختراع تبين أن مبيد البروبانيل له نشاط مبيد للأعشاب غير عادي وقيِّم، وأن نشاطه كان مفاجئًا لأن المركبات وثيقة الصلة بالبروبانيل عادةً ما تكون لها كفاءة قليلة أو معدومة في مبيدات الأعشاب. أجرت مونسانتو عددًا من الاختبارات وقدمت بيانات الاختبار إلى مكتب براءات الاختراع، والتي أشارت إلى أن البروبانيل كان متفوقًا على المواد الكيميائية المماثلة الأخرى، ومن بينها مادة كيميائية تختلف عن البروبانيل فقط في القضاء على مجموعة CH2 على يسار مجموعة CH3 في أقصى يمين الرسم كما هو موضح (ويُطلق على المادتين الكيميائيتين اسم المتماثلات المتجاورة).
حجبت شركة مونسانتو البيانات الخاصة بتلك الاختبارات، والتي أظهرت أن مركبات أخرى مماثلة لها أيضًا نشاط مبيد للأعشاب مشابه لنشاط البروبانيل. وذكرت المحكمة إن هذا يمثل تحريفاً وعملا احتياليا وأن شركة مونسانتو لا يحق لها الحصول على براءة اختراع للبروبانيل، لذلك كانت البراءة باطلة أو غير قابلة للتنفيذ. ولكن في قضية سابقة كان القاضي قد قبل حجة شركة مونسانتو بأن شركة مونسانتو لم تفعل شيئًا أكثر من تقديم أفضل ما لديها لمكتب براءات الاختراع.[9]
المراجع
- ^ فهرس ميرك, 11th Edition, 7814.
- ^ 2000-2001 Pesticide Market Estimates, U.S. Environmental Protection Agency نسخة محفوظة 2009-02-07 على موقع واي باك مشين.
- ^ Management of Propanil Resistant Sedges, UC Rice Blog (June 19, 2014). نسخة محفوظة 2021-03-04 على موقع واي باك مشين.
- ^ Irina V. Ustyugova, Propanil (3,4-DCPA)-induced alterations of macrophage function[وصلة مكسورة] 2-3 (Ph.D. thesis 2007). See also Inhibition of Photosynthesis: Inhibition at Photosystem II§§ 1–4. نسخة محفوظة 2016-06-03 على موقع واي باك مشين.
- ^ Herbicide Resistance and World Grains 215-16 (Stephen B. Powles & Dale L Shaner eds. 2001). نسخة محفوظة 20 سبتمبر 2018 على موقع واي باك مشين.
- ^ Wyatt، Stuart Warren, Paul (2008). Organic synthesis : the disconnection approach (ط. 2nd). Oxford: Wiley-Blackwell. ص. 25. ISBN:978-0-470-71236-8.
{{استشهاد بكتاب}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Propanil in PubChem Open Chemistry Database. نسخة محفوظة 2018-09-20 على موقع واي باك مشين.
- ^ 456 F.2d 592 (3d Cir. 1972).
- ^ See 456 F.2d at 597 n.4.
| بروبانيل في المشاريع الشقيقة: | |