|
تضامنًا مع حق الشعب الفلسطيني |
عملية شبه ساكنة
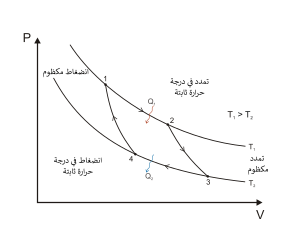
في الديناميكا الحرارية، عملية شبه ثابتة (تُعرف أيضًا باسم شبه التوازن، من شبه اللاتينية، بمعنى «كما لو»[1])، هي عملية ديناميكية حرارية تحدث ببطء كافٍ حتى يظل النظام قريباً من حالة توازن داخلي. مثال على ذلك هو الضغط شبه الثابت، حيث يتغير حجم النظام بمعدل بطيء بدرجة كافية للسماح للضغط بالبقاء موحدًا وثابتًا في جميع أنحاء النظام.[2] هذه العملية هي سلسلة من حالات التوازن، والبطء اللامتناهي هو سمة مميزة لها.[3]
فقط في العملية شبه الثابتة يمكننا تحديد الخواص المكثفة (مثل الضغط ودرجة الحرارة والحجم المحدد والإنتروبيا المحددة) للنظام في كل لحظة خلال العملية برمتها ؛ بخلاف ذلك، نظرًا لعدم وجود توازن داخلي، سيكون لأجزاء مختلفة من النظام قيم مختلفة لهذه الكميات.
أي عملية قابلة للعكس هي عملية شبه ثابتة. ومع ذلك، فإن العمليات شبه الساكنة التي تشمل إنتاج الانتروبيا لا يمكن عكسها. مثال على عملية شبه ثابتة غير قابلة للعكس هو الضغط على نظام بمكبس معرض للاحتكاك؛ على الرغم من أن النظام دائمًا في حالة توازن حراري، فإن الاحتكاك يضمن توليد إنتروبيا مشتتة، والتي تتعارض مع تعريف الانعكاس. بدلاً من ذلك، يمكن للمرء أن يقول إن الاحتكاك سوف يولد حرارة وانتروبيا تبديدية فقط إذا لم تكن حركة المكبس بطيئة بشكل غير محدود. أحد الأمثلة البارزة على عملية ليست حتى شبه ثابتة هو التبادل الحراري البطيء بين جسمين على درجتين حراريتين مختلفتين تمامًا، حيث يتم التحكم في معدل التبادل الحراري بواسطة قسم ثابت الحرارة تقريبًا بين الجسمين — في هذه الحالة، لا يهم وببطء حدوث العملية، فإن حالات النظام المركب المكون من الجسمين بعيدة كل البعد عن التوازن، لأن التوازن الحراري لهذا النظام المركب يتطلب أن يكون الجسمان في نفس درجة الحرارة.
العلاقة بين الشغل والضغط والحجم (PV) في العمليات شبه الساكنة
- الضغط الثابت: عمليات متساوية الضغط،
- الحجم الثابت: عمليات متساوية الحجم،
- درجة حرارة ثابتة: عمليات متساوية الحرارة،
- حيث P يختلف مع V عبر، وبالتالي
- عمليات متعددة الاتجاهات،
مراجع
- ^ Lewis, C.T., Short, C. (1879). A Latin Dictionary, Clarendon Press, Oxford, page 1507.
- ^ Schroeder، Daniel (2000). An Introduction to Thermal Physics. United States: Addison Wesley Longman. ص. 20–21. ISBN:0-201-38027-7.
- ^ Rajput, R.K. (2010). A Textbook of Engineering Thermodynamics, 4th edition, Laxmi Publications (P) Ltd, New Delhi, pages 21, 45, 58.