|
تضامنًا مع حق الشعب الفلسطيني |
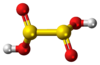
حمض ثنائي الثيونوز
| حمض ثنائي الثيونوز | |
|---|---|
 |
 |
| الاسم النظامي (IUPAC) | |
Dithionous acid |
|
| أسماء أخرى | |
Hydrosulfurous acid |
|
| الخواص | |
| الصيغة الجزيئية | H2S2O4 |
| الكتلة المولية | 130.14 غ/مول |
| حموضة (pKa) | 0.35 2.45 [1] |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
حمض ثنائي الثيونوز هو حمض أكسجيني مضاعف الكبريت صيغته H2S2O4، وهو غير مستقر؛[2] لكن أملاحه التي تدعى ثنائي ثيونيت معروفة ومستقرة، ولا يمكن إجراء عملية استحصال الحمض منها.
الخواص
بينت حسابات «منذ البدء» النظرية أن البنية المتناظرة من النمط C2 حيث يكون الجزيء على الشكل HOS(=O)-S(=O)OH هي أكثر بنية مستقرة بين المتصاوغات.[2] يعود سبب ذلك إلى وجود الروابط الهيدروجينية بين الجزيئية.
بالرغم من ذلك، فإن هذا المركب غير مستقر كيميائياً ويتفكك إلى ثنائي أكسيد الكبريت SO2 وحمض الهيبوكبريتوز.S(OH)2
الأملاح

تعد أملاح هذا الحمض أكثر استقراراً؛ إذ أن ثنائي الثيونيت هو أنيون أكسجيني للكبريت،[3] صيغته −2S2O4.
تخضع هذه الأنيونات إلى تفاعل أكسدة-اختزال حيث يتشكل أنيون الكبريتيت، حيث تبلغ قيمة جهد الاختزال مقدار −0.66 فولت:[4]
ومن الأمثلة عليها ثنائي ثيونيت الصوديوم، وهو يوجد على شكل مسحوق أبيض وله خواص مختزلة ويستخدم في عمليات التبييض الصناعية.
طالع أيضاً
مراجع
- ^ Catherine E. Housecroft؛ Alan G. Sharpe (2008). "Chapter 16: The group 16 elements". Inorganic Chemistry, 3rd Edition. Pearson. ص. 520. ISBN:978-0-13-175553-6.
- ^ أ ب Drozdova، Yana؛ Steudel، Ralf؛ Hertwig، Roland H.؛ Koch، Wolfram؛ Steiger، Thomas (1998). "Structures and Energies of Various Isomers of Dithionous Acid, H2S2O4, and of Its Anion HS2O4- 1". The Journal of Physical Chemistry A. ج. 102 ع. 6: 990–996. Bibcode:1998JPCA..102..990D. DOI:10.1021/jp972658d.
- ^ International Union of Pure and Applied Chemistry (2005). Nomenclature of Inorganic Chemistry (IUPAC Recommendations 2005). Cambridge (UK): Royal Society of Chemistry–International Union of Pure and Applied Chemistry (IUPAC). (ردمك 0-85404-438-8). p. 130. نسخة إلكترونية باللغة الإنجليزية.
- ^ Mayhew, S. G. (2008). "The Redox Potential of Dithionite and SO2− from Equilibrium Reactions with Flavodoxins, Methyl Viologen and Hydrogen plus Hydrogenase". European Journal of Biochemistry. ج. 85: 535–547. DOI:10.1111/j.1432-1033.1978.tb12269.x.
| حمض ثنائي الثيونوز في المشاريع الشقيقة: | |
