|
تضامنًا مع حق الشعب الفلسطيني |
شبيغلمر

شبيغلمر (المشابه الضوئي) (من الألمانية شبيغل "مرآة") هو جزء يشبه الحمض الريبي النووي يتكون من وحدات إل-ريبوز .[1] وهو النيوكليوتيدات الصناعية سمي بهذه التسمية لكونه نسخة متطابقة من النيوكليوتيدات الطبيعية. وتعد المشابهات الضوئية شكلاً من أشكال الأبتمرات. ونظرًا للنيوكليوتيدات الخاصة بها، وهي مقاومة بدرجة كبيرة للتحلل بسب نوكليازات.[1] كما تعتبر المشابهات الضوئية عقاقير محتملة، ويجري حاليًا اختبارها في التجارب السريرية.
الميزات
الخصائص الكيميائية
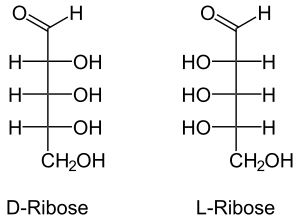
المشابهات الضوئية، التي تم تكوينها باستخدام الريبوز إل، هي المقابلات الضوئية للأليغنوكليوتيد الطبيعي، والذي يتكون من الريبوز دي. تحتوي أبتامرات الحمض النووي، بما في ذلك المشابهات الضوئية، على أحادي فوسفات الأدينوزين وغوانوزين الأدينوزين وسيتيدين الأدينوزين ويوريدين الأدينوزين ومجموعة الفوسفات ونكليوبس، وسكر الريبوز.
الخصائص البيولوجية
وكغيرها من الأبتامرات، المشابهات الضوئية قادرة على ربط جزيئات مثل الببتيدات والبروتينات والمواد ذات الوزن الجزيئي المنخفض. ويقع تقارب من المشابهات الضوئية لجزيئاتها المستهدفة في كثير من الأحيان في نطاق بيكو إلى مولي متناهي الصغر، وبالتالي فإنها تضاهي الأجسام المضادة.[2]
وللمشابهات الضوئية نفسها استضداد منخفض. وعلى النقيض من الأبتامرات الأخرى، تتميز المشابهات الضوئية باستقرارية عالية في مصل الدم، نظرًا لأنها أقل عرضة للانشطار هيدروليكيًا بفعل الإنزيمات.[3] ويتم إفرازها بواسطة الكلى في وقت قصير نظرًا لانخفاض الكتلة المولية بها (وهي أقل من الحد الكلوي الأدنى).
تظهر المشابهات الضوئية المعدلة بالكتلة المولية، مثل المشابهات الضوئية التي عولجت بجلايكول الإيثيلين البولي ، نصف عمر بلازمي طويل الأمد.
الإنتاج
على عكس الأبتامرات الأخرى، لا يتم تصنيع المشابهات الضوئية باستخدام SELEX بشكل مباشر (تطور الليجندات المنهجي بواسطة التخصيب الأسي)، حيث أن الأحماض النووية إل ليست قابلة للطرق الأنزيمية مثل تفاعل البوليميراز المتسلسل المستخدمة في تطور الليجندات المنهجي بواسطة التخصيب الأسي. ومن ثم، يتم الاختيار بالجزيئات المستهدفة المعكوسة.
انعكاس الجزيء المستهدف
أول خطوة هي إنتاج جزيئات الهدف المتماثلة صوريًا. في حالة من الببتيدات والبروتينات الصغيرة التي يتم إنتاجها صناعيًا، يتم عمل جزيئات متماثلة باستخدام الأحماض الأمينية دي الاصطناعية. فإذا كان الهدف أكبر من جزء البروتين، خارج القدرات الاصطناعية، فإن المُصاوِغ المِرْآتِيّ لحاتمة يتم إنتاجه.[3]
تطور الليجندات المنهجي بواسطة التخصيب الأسي (SELEX)
الوجود التقليدي (حتى 1016أليغنوكليوتيد مختلفة) لمكتبة الجزيء يعمل كنقطة بداية لعملية تطور الليجندات المنهجي بواسطة عملية التخصيب الأسي (SELEX) التالية. يتم تنفيذ الاختيار، والانفصال، والتضخيم باستخدام صورة طبق الأصل من جزيء الهدف.
التسلسل والتحليل
يتم تحديد تسلسل النوكليوتيدات الذي تم اختياره باستخدام تطور الليجندات المنهجي بواسطة التخصيب الأسي من خلال مساعدة سلسلة الحمض النووي. ويتم استخدام هذه المعلومات لتحليل الجزيئات المماثلة للنيوكليوتيدات، والمشابه الضوئي، باستخدام النيوكليوتيدات إل.
الاستخدامات
وقد تم الحصول على المشابهات الضوئية للكيموكينات سي سي إل 2 والعامل 1 المستمد من الخلية السدوية، والمكونات المتممة سي 5 إيه، والغريلين. فهي حاليًا في التطوير قبل السريري أو الإكلينيكي. ويمكن أيضًا أن تستخدم كعوامل تشخيص.[3]
المراجع
- ^ أ ب Helmling, S.H.؛ Eulberg, D.E.؛ Maasch, C.M.؛ Buchner, K.B.؛ Klussmann, S.K. (July 2003). "RNA-Spiegelmers: a new substance class to efficiently inhibit peptide hormones". European Journal of Biochemistry. ج. 1 ع. supplement. مؤرشف من الأصل في 9 ديسمبر 2019. اطلع عليه بتاريخ أغسطس 2020.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) والوسيط غير المعروف|abstract_number=تم تجاهله (مساعدة) - ^ Wlotzka، Britta؛ Leva، Susanne؛ Eschgfäller، Bernd؛ Burmeister، Jens؛ Kleinjung، Frank؛ Muhn، Peter؛ Hess-Stumpp، Holger؛ Klussmann، Sven (يونيو 2002). "In vivo properties of an anti-GnRH Spiegelmer: an example of an oligonucleotide-based therapeutic substance class". Proceedings of the National Academy of Sciences of the United States of America. ج. 99 ع. 13: 8898–902. Bibcode:2002PNAS...99.8898W. DOI:10.1073/pnas.132067399. PMC:124395. PMID:12070349.
{{استشهاد بدورية محكمة}}: النص "last6Kaduk" تم تجاهله (مساعدة) والوسيط|مؤلف6-الأول=يفتقد|مؤلف6-الأخير=(مساعدة) - ^ أ ب ت Klussmann S, Nolte A, Bald R, Erdmann VA, Fürste JP (سبتمبر 1996). "Mirror-image RNA that binds D-adenosine". Nat. Biotechnol. ج. 14 ع. 9: 1112–5. DOI:10.1038/nbt0996-1112. PMID:9631061.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link)