|
تضامنًا مع حق الشعب الفلسطيني |
بيروكسيد الزنك
| بيروكسيد الزنك | |
|---|---|
| الاسم النظامي (IUPAC) | |
بيروكسيد الزنك |
|
| أسماء أخرى | |
فوق أكسيد الزنك |
|
| المعرفات | |
| رقم CAS | 1314-13-2 |
| بوب كيم (PubChem) | 10129902 |
| الخواص | |
| الصيغة الجزيئية | ZnO2 |
| الكتلة المولية | 97.38 غ/مول |
| المظهر | مسحوق بلوري أبيض إلى أصفر |
| الكثافة | 1.57 غ/سم3 |
| نقطة الانصهار | 212 °س يتفكك |
| المخاطر | |
| ترميز المخاطر | |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
بيروكسيد الزنك هو مركب كيميائي له الصيغة ZnO2، ويكون على شكل مسحوق بلوري لونه يتفاوت بين الأبيض إلى الأصفر.
الخواص
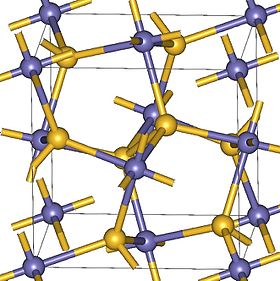
- يمتلك فوق أكسيد الزنك بنية بلورية مكعبة مثل البيريت FeS2، وتكون الفجوة الطاقية لديه بمقدار 3.8 إلكترون فولت [2]
- يعد فوق أكسيد الزنك من أشباه الموصلات غير المباشرة، وتبلغ قيمة معامل المرونة الحجمية Bulk modulus لمركب فوق أكسيد الزنك 174 GPa (غيغاباسكال).[3]
التحضير
يحضر مركب فوق اكسيد الزنك من تفاعل أكسيد أو خلات الزنك مع فوق أكسيد الهيدروجين (الماء الأكسجيني):[2]
- ZnO + H2O2 → ZnO2 + H2O
الاستخدامات
- يستعمل فوق أكسيد الزنك في عمليات التبييض نظرا لوجود الرابطة O-O في بنيته. كما يدخل في تركيب بعض المطهرات.
- يستعمل لتحفيز التشابك في صناعة مطاط النتريل وفي الوحدات المرنة الأخرى.[4]
- يستعمل كمؤكسد في بعض خلائط المتفجرات والألعاب النارية.[5]
المراجع
- ^ Zinc peroxide 50-60% | Sigma-Aldrich نسخة محفوظة 18 سبتمبر 2020 على موقع واي باك مشين.
- ^ أ ب D. Sebok؛ وآخرون (2009). Applied Surface Science. ج. 255: 6953. DOI:10.1016/j.apsusc.2009.03.020.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة) والوسيط|title=غير موجود أو فارغ (مساعدة) - ^ W. Chen؛ وآخرون (2009). "Synthesis, Thermal Stability and Properties of ZnO2 Nanoparticles". J. Phys. Chem. C. ج. 113: 1320. DOI:10.1021/jp808714v.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة) - ^ Akiba، M. (1997). "Vulcanization and crosslinking in elastomers". Progress in Polymer Science. ج. 22: 475–521. DOI:10.1016/S0079-6700(96)00015-9.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|مؤلفين مشاركين=تم تجاهله يقترح استخدام|authors=(مساعدة) - ^ R. Hagel, K. Redecher, Patent US4363679-A, 1981