ورم الدماغ
سرطان الدماغ وتشمل أورام المخ كل أنواع الأورام التي تظهر داخل القحف أو في قناة العمود الفقري المركزية. وهي تنجم عن انقسام غير طبيعي للخلايا ولا يمكن السيطرة عليه، غالبًا ما يكون ذلك في المخ نفسه، لكنه يحدث أيضاً في النسيج الليمفاوي، وفي الأوعية الدموية، وفي الأعصاب القحفية أو في أغلفة المخ (السحايا)، أوالجمجمة، أو الغدة النخامية، أو في الغدة الصنوبرية. داخل المخ نفسه، يمكن أن تكون الخلايا التي يحدث بها الانقسام عبارة عن خلايا عصبية[محل شك] أو خلايا دبقية، والتي تشتمل على الخلايا النجمية والخلايا الدبقية قليلة التغصن وخلايا البطانة العصبية). كما يمكن أن تتسبب السرطانات الموجودة في الأعضاء الأخرى (الأورام الخبيثة) في انتشار أورام في المخ.
| ورم الدماغ | |
|---|---|
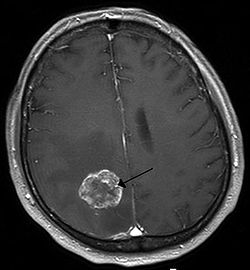 انبثاث الورم الدماغي في نصف الكرة الدماغية الأيمن بسبب سرطان الرئة يظهر بالتصوير بالرنين المغناطيسي الموزون بT1 مع التباين داخل الوريد.
| |
| تعديل مصدري - تعديل |
ويكون أي ورم في المخ بطبيعته خطيرًا ويمكن أن يؤدي إلى الوفاة بسبب طبيعته الغزوية والارتشاحية في المساحة المحدودة في التجويف الموجود داخل الجمجمة. ومع ذلك، فإن أورام المخ (حتى تلك الخبيثة) لا تكون قاتلة بصفة دائمة، خصوصًا الورم الشحمي الذي يكون حميدًا بطبيعته. ويمكن أن تكون أورام المخ أو الأورام التي تظهر داخل القحف سرطانية (خبيثة) أو غير سرطانية (حميدة، ومع ذلك، تختلف تعريفات الأورام الخبيثة أو الأورام الحميدة عن تلك المستخدمة بشكل شائع في الأنواع الأخرى من الأورام السرطانية أو غير السرطانية في الجسم. ويعتمد مستوى التهديد على مجموعة من العوامل مثل نوع الورم وموقعه وحجمه وحالته من ناحية التطور. ونظرًا لأن المخ يكون محميًا حماية جيدة من خلال الجمجمة، فإن الاكتشاف المبكر لأورام المخ لا يحدث إلا عندما يتم توجيه أدوات التشخيص تجاه تجويف داخل الجمجمة. وغالبًا ما يحدث الاكتشاف في المراحل المتقدمة عندما يسبب الورم أعراضًا لا يوجد لها تفسير.
وفي الغالب، تظهر أورام المخ الرئيسية (الحقيقية) في الحفرة القحفية الخلفية لدى الأطفال وفي الثلثين الأماميين من نصفي الكرة المخية لدى البالغين، رغم أنها يمكن أن تؤثر على أي جزء من المخ.
سرطان الدماغ، أو الورم داخل القحف، يحدث عندما تتشكل خلايا غير طبيعية داخل الدماغ،[1] هناك نوعان رئيسيان من الأورام: الورم الخبيث (السرطاني)و الورم الحميد[1]
الأورام السرطانية تقسم إلى أورام اولية التي تبدأ داخل الدماغ أو أورام ثانوية التي تنتشر من مكان اخر لتستقر داخل الدماغ أو ما يعرف النقيلة في الدماغ. في هذه المقالة سنتعامل مع الاورام الاولية. جميع أنواع الأورام قد ينتج عنها أعراض تختلف حسب موقع الورم في الدماغ [2] الأعراض تشمل: الصداع، تشنجات عصبية، مشكلات بصرية، تقيؤ واختلالات عقلية.[3][4] الصداع بشكل تقليدي يكون في اسوأ حالاته خلال الصباح، ويخف هذا الصداع عند التقيؤ.[2] المشاكل الأكثر تحديداَ تشمل: صعوبة في المشي، الكلام والإحساس.[5][6] مع تطور المرض قد يصل المريض إلى حالة اللاوعي (الغيبوبة).[6]
سبب معظم أورام الدماغ غير معروفة.[2] تشمل عوامل الخطر العوامل الجينية الوراثية والمعروفة باسم الورم العصبي الليفي، وكذلك التعرض للكيماويات الصناعية مثل الفينيل كلوريد، وفيروس ابشتاين بار والاشعاعات المؤينة.[5][6][7] كانت هناك بعض المخاوف من اشعاعات الهاتف المحمول، لكنها لم تثبت علمياً.[6] الأنواع الأكثر شيوعا من الأورام الأولية في البالغين هي: السحائية (عادة تكون ورماً حميدة)، و astrocytomas مثل الورم الأرومي الدبقي.[5] في الأطفال أكثر الانواع شيوعاَ هوالورم النخاعي الخبيث.[6] التشخيص يكون عادةَ عن طريق الفحص الطبي بالإضافة للتصوير المقطعي المحوسب أو التصوير بالرنين المغناطيسي. يثبت ذلك عادةً بأخذ خزعة.[5] بناء على نتائج الابحاث; نقسم الأورام الي درجات مختلفة من الشدة.[5]
قد يشمل العلاج الجمع بين الجراحة والعلاج الإشعاعي والعلاج الكيميائي.[5] قد تكون هناك حاجة إلى أدوية الاختلاج في حالة حدوث النوبات.[5] يمكن أن يستخدم ديكساميثازون وفوروسيميد لتقليل التورم حول السرطان.[5] بعض الأورام تنمو تدريجيا، الأمر الذي يتطلب مراقبة فقط، وربما لا تحتاج إلى أي تدخل آخر.[5] حالياَ يتم دراسة العلاجات التي تستخدم النظام المناعي للشخص.[2] تختلف النتائج كثيرا تبعا لنوع الورم ومدى انتشاره في التشخيص.[6] الورم الأرومي الدبقي عادة ما تكون نتائجه سيئة في حين أن الأورام السحائية عادة نتائجها جيدة.[6] ويبلغ متوسط معدل البقاء على قيد الحياة لمدة خمس سنوات 33٪ لمرضى سرطان الدماغ في الولايات المتحدة.[8]
أورام المخ الثانوية أو المتنقلة هي أكثر شيوعا من أورام الدماغ الأولية [2]، وما يقارب النصف من الانبثاثات تكون قادمة من سرطان الرئة.[2] تحدث أورام الدماغ الأولية في حوالي 250000 شخص سنويا على مستوى العالم، التي تشكل أقل من 2٪ من السرطانات.[6] في الأطفال الذين تقل أعمارهم عن 15 أورام الدماغ تأتي في المرتبة الثانية بعد سرطان الدم الليمفاوي الحاد كسبب للسرطان.[9] في أستراليا التكلفة الاقتصادية في متوسط حالة سرطان الدماغ 1.9 مليون دولار، أكثر من أي نوع من أنواع الأورام.[10]
العلامات والاعراض
علامات وأعراض الورم في الدماغ تعتمد بشكل رئيسي على حجم الورم وموقعه. وظهور الأعراض - في الجدول الزمني لتطور الورم - يعتمد في كثير من الحالات على طبيعة الورم (لكونها حميدة أو خبيثة)، وفي كثير من الحالات يرتبط أيضا بتغيير في طبيعة الأورام من بطيء النمو لأسرع نموا.
يمكن تقسيم أعراض كل من أورام الدماغ الأولية والثانوية إلى ثلاث فئات رئيسية هي:
•الأعراض الناتجة عن زيادة الضغط داخل الجمجمة (معظم الاوقات يكون أول عرض): الأورام الكبيرة أو الأورام مع انتفاخ كبير حول الورم (وذمة) ستؤدي حتما إلى ضغط مرتفع داخل الجمجمة والتي تترجم سريريا إلى صداع وتقيؤ (مع أو بدون غثيان)، حالة وعي متقلبة (النعاس والغيبوبة)، توسع البؤبؤ على جانب الإصابة (تفاوت الحدقتين)، ذمة حليمة العصب البصري (القرص البصري بارز في فحص العين funduscopic). ومع ذلك، يمكن لبعض الأورام الصغيرة عرقلة مرور السائل النخاعي (سي إس إف) لتقديم مثل هذه الأعراض. زيادة الضغط داخل الجمجمة قد يؤدي إلى فتق الدماغ (أي تهجير) أجزاء معينة من الدماغ، مثل لوزتي المخيخ أو المعقف الصدغي، مما يؤدى إلى الضغط المميت لجذع الدماغ.عند الأطفال الصغار قد يسبب ارتفاع الضغط داخل الجمجمة إلى زيادة في قطر الجمجمة وانتفاخ اليافوخ.
•الاختلال الوظيفي: اعتمادا على موقع الورم والأضرار التي قد تسببها لهيكل الدماغ المحيط بها، إما عن طريق الضغط أو التسلل، قد يحدث أي نوع من الأعراض العصبية، مثل ضعف الإدراك والسلوك (بما في ذلك ضعف الحكم، وفقدان الذاكرة، وعدم القدرة على التعرف، واضطرابات التوجه المكاني)، التغيرات الشخصية أو العاطفية، فالج، نقص الحس، فقدان القدرة على الكلام، ترنح، ضعف المجال البصري، ضعف حاسة الشم، وضعف السمع، الشلل الوجهي، الرؤية المزدوجة، والدوخة، ولكن بعض الأعراض الأكثر شدة قد تحدث أيضا، مثل الشلل على جانب واحد من الجسم (شلل نصفي) وانخفاض في البلع. هذه الأعراض ليست محددة لأورام الدماغ - لأنها قد تكون ناجمة عن مجموعة كبيرة ومتنوعة من الامراض العصبية (مثل السكتة الدماغية، وإصابات في الدماغ). لكن ما هو مهم فعلياَ هو موقع الورم والأنظمة الوظيفية المتأثرة (مثل الحركة، والحس والبصر، وما إلى ذلك). قد يحدث عيب المجال البصري الثنائي (عمى شقي بين الصدغين بسبب الضغط على optic chiasm)، الذي يرتبط غالباَ مع خلل الغدد الصماء، إما قصور النخامية أو زيادة إفراز هرمونات الغدة النخامية وزيادة إنتاج البرولاكتين وهذا يدل على وجود ورم في الغدة النخامية.
•التهيج: تعب غير طبيعي، الشرود والهزات العصبية، وأيضا نوبات الصرع. قد لا تظهر أعراض لبعض أورام الدماغ الحميدة لعدة سنوات. اما البعض الآخر فقد يظهر أعراض غامضة ومتقطعة مثل الصداع والقيء والإرهاق وقد يخطأ في التشخيص بينه وبين اضطرابات الجهاز الهضمي. في هذه الحالات تحتاج الأعراض الثانوية إلى إعادة النظر فيها.
الاسباب
هناك حاجة لدراسات وبائية لتحديد عوامل الخطر.[11] وبصرف النظر عن التعرض لكلوريد الفينيل أو الإشعاع المؤين، لا توجد عوامل بيئية معروفة مرتبطة بأورام المخ. الطفرات وحذف ما يسمى بالجينات القامعة للورم، مثل P53، يعتقد أن تكون سبب لبعض أشكال أورام في المخ.[12] الصفات الموروثة، مثل مرض فون هيبل لينداو، أورام متعددة في الغدد الصماء، والورم العصبي الليفي نوع 2 تحمل مخاطر عالية لتطوير أورام المخ. على الرغم من أن الدراسات لم تظهر أي صلة بين الهاتف الخليوي أو إشعاع الهاتف المحمول وحدوث أورام الدماغ [13] لكن منظمة الصحة العالمية صنفت إشعاع الهاتف المحمول على نطاق IARC في المجموعة 2B - التي يمكن أن تسبب السرطان.[14]
الفيزيولوجيا المرضية
الأغشية السحائية
تحيط الادمغة البشرية نظام من أغشية النسيج الضام تسمى السحايا التي تفصل الدماغ من الجمجمة. ويتكون هذا الغطاء من ثلاث طبقات وهي (من الداخل إلى الخارج): الجافية («الأم الصعبة»)، الأم العنكبوتية، والأم الحنون («أم العطاء»). والعنكبوتي والحنون ترتبطان مع بعضهن البعض، وبالتالي غالبا ما تعتبران بمثابة طبقة واحدة، الحنون العنكبوتية. بين الأم العنكبوتية والأم الحنون يوجد فراغ تحت العنكبوتية الذي يحتوي على السائل النخاعي (CSF). هذا السائل يدور في المساحات الضيقة بين الخلايا وذلك من خلال تجاويف في الدماغ تسمى البطينات، لتغذية ودعم وحماية أنسجة الدماغ. الأوعية الدموية تدخل الجهاز العصبي المركزي من خلال الفراغ المحيط بالأوعية فوق الأم الحنون. خلايا جدران الأوعية الدموية ملتصقة مع بعضها بعضاَ بإحكام مشكلةً حاجز الدم في الدماغ الذي يحمي الدماغ من السموم التي قد تدخل عن طريق الدم. أورام السحايا تسمى بالسحائية وغالبا ما تكون حميدة.
مادة الدماغ
تتكون أدمغة البشر والفقاريات الأخرى من أنسجة رخوة جدا ملمسها يشبه الجيلاتين. النسيج الحي لونه وردي من الخارج (المادة الرمادية)، ولونه ابيض تقريبا في الداخل (المادة البيضاء)، مع وجود اختلافات طفيفة في اللَون. ثلاث مناطق منفصلة من الدماغ تشكل معظم حجمه:
•الدماغ الانتهائي (نصفي الكرة المخية أو المخ)
•الدماغ المتوسط (دماغ متوسط)
•المخيخ
وتتكون هذه المناطق من طبقتين واسعتين من الخلايا: الخلايا العصبية والخلايا الدبقية. هذين النوعين متساويان في العدد في الدماغ ككل، على الرغم من أن الخلايا الدبقية تفوق عدد الخلايا العصبية بما يقارب من 4-1 في القشرة المخية. الخلايا الدبقية تأتي في عدة أنواع، وتؤدي عدداَ من الوظائف الهامة، بما في ذلك الدعم الهيكلي، دعم التمثيل الغذائي، والعزل، وتوجيه النمو. وتسمى الأورام الأولية من الخلايا الدبقية الاورام الدبقية وهي خبيثة في معظم الأحيان.
الحبل الشوكي وانسجة أخرى
الجسر المخيخي في الدماغ هي منطقة محددة تتكون من محاور عصبية ميالينية مثل تركيب الحبل الشوكي. غدة المهاد وتحت المهاد في الدماغ البيني (المتوسط) تتكون أيضا من الخلايا العصبية وأنسجة الخلايا الدبقية مع الغدة النخامية والغدة الصنوبرية في اسفل الدماغ; أورام الغدة النخامية والغدة الصنوبرية غالبا ما تكون حميدة. النخاع المستطيل يكون في بداية الحبل الشوكي ويتكون أساسيا! من الخلايا العصبية التي تلفها خلايا شوان وأنسجة السحايا. ويتكون الحبل الشوكي من حزم من هذه المحاور. الخلايا الدبقية مثل خلايا شوان موجودة في محيط الحبل أو داخل الحبل نفسه، قليلة التشعب، تلف أنفسها حول محور عصبي، وبالتالي تعزز نقل أسرع للإشارات الكهربائية وتوفر حماية للبيئة المحيطة للحبل، وفي اجزاء من الحبل تقوم هذه الخلايا بنقل مختلف المركبات الكيميائية بعد التعرض لمؤثر أو اصابة.
التشخيص
يتم فصل معظم خلايا الدماغ عن مجرى الدم عن طريق حاجز الدم في الدماغ (BBB)، الذي يمنع دخول جميع المركبات أو المواد في الدم إلى الدماغ. ولذلك يتم انتقال الورم إلى الدماغ فقط في حالة وجود خلل في حاجز الدم في الدماغ. والتي يمكن الكشف عنها بواسطة التصوير بالرنين المغناطيسي والتصوير المقطعي، ويعتبر المؤشر الرئيسي لتشخيص الاورام الدبقية الخبيثة، السحائية، والانعاثات الدماغية.[15]
على الرغم من عدم وجود أعراض سريرية محددة لاورام الدماغ، وجود مجموعة من الأعراض وغياب المؤشرات السريرية للالتهابات أو غيرها يمكن أن يكون مؤشر لامكانية وجود الأورام داخل الجمجمة. قد يصعب تشخيص هذه الاورام لاختلافها عن بقية اورام الجسم، مع ذلك فانها تسلك سلوكاً مميزاً تبعا لموقعها.[15] سيبدأ التشخيص في كثير من الأحيان عن طريق أخذ التاريخ الطبي مشيرا إلى السوابق الطبية، والأعراض الحالية. تفيد التحقيقات السريرية والمخبرية في استبعاد الالتهابات التي قد تكون هي سبب الأعراض. ويمكن أن تشمل الاختبارات في هذه المرحلة العيون، طب الأذن والحنجرة (أو ENT) وفحصوصات كهربية لموجات الدماغ. واستخدام كهربية (EEG) غالبا ما يلعب دورا في تشخيص أورام الدماغ. تورم أو إعاقة مرور السائل النخاعي (CSF) من الدماغ (المبكر) قد يسبب علامات زيادة الضغط داخل الجمجمة والتي تترجم سريريا إلى الصداع، والقيء، أو تغير في حالة الوعي، اما في الأطفال فيتغير قطر الجمجمة وينتفخ اليافوخ. عند حصول الأعراض الأكثر تعقيدا مثل اختلالات الغدد الصماء يجب على الأطباء التنبه على عدم استبعاد أورام الدماغ.
عيب المجال البصري الثنائي (بسبب الضغط على التصالبة البصرية) أو توسع البؤبؤ، أو حدوث أي تطور ببطء أو ظهور مفاجئ لأعراض عصبية، مثل: ضعف الإدراك والسلوك (بما في ذلك ضعف الحكم، وفقدان الذاكرة، عدم القدرة على التعرف والتميز، واضطرابات التوجه المكاني)، التغيرات الشخصية أو التغيرات العاطفية، خزل شقي، نقص الحس، فقدان القدرة على الكلام، ترنح، ضعف المجال البصري، ضعف حاسة الشم، وضعف السمع، الشلل الوجهي، الرؤية المزدوجة، أو أعراض أكثر شدة مثل الهزات، والشلل على جانب واحد مثل الشلل النصفي للجسم، أو (الصرع) في المريض مع عدم وجود تاريخ لعلاج الصرع، ينبغي ان يرفع احتمال وجود ورم في الدماغ.
التصوير
التصوير الطبي يلعب دورا محوريا في تشخيص أورام الدماغ. وقد تم التخلي عن الطرق القديمة الخطرة، مثل تصوير الدماغ المحقون بالغاز وتصوير الأوعية الدماغية واستبدلت بتقنيات عالية الدقة، والتصوير بالرنين المغناطيسي (تصوير بالرنين المغناطيسي) والتصوير المقطعي (تصوير مقطعي محوسب) بالاشعة. سوف تظهر الأورام غالبا للطبيب ملونة ومختلفة (كما يشار إلى العمليات) في نتائج CT أو MRI. • تظهر أورام الدماغ الحميدة غالبا على نحو أغمق من أنسجة الدماغ الطبيعية على الأشعة المقطعية (CT). اما على MRI فإنها تظهر إما غامقة أو بنفس الشدة كما في أنسجة المخ على T1-weighted scans ، أو (أكثر إشراقا من أنسجة المخ) T2-weighted scans ، على الرغم من أن مظهرها متغير. • عند امتصاص الدماغ لكيماويات تسمى (عوامل التباين)، يمكن الكشف عن معظم أورام الدماغ الأولية والاورام الثانوية (النقيلية الخبيثة) في أي من الأشعة المقطعية أو الرنين المغناطيسي. • مناطق الضغط التي تم فيها الضغط على أنسجة الدماغ من الورم تظهر بشكل مشرق على T2-weighted scans، وربما تدل على وجود ورم منتشر بسبب الحدود الغير واضحة المحيطة بالورم. يمكن وجود انتفاخ من السوائل حول الورم المعروف باسم الوذمة المحيطة بالورم الذي قد يظهر نتيجة مماثلة. وذلك لأن هذه الأورام تعطل السير العادي للBBB وتؤدي إلى زيادة نفاذيتها. ومع ذلك، فإنه ليس من الممكن تشخيص الاورام الدبقية عالية الدرجة من الأورام الدبقية منخفضة الدرجة استنادا إلى نمط التعزيز فقط. يمكن تأكيد التشخيص النهائي للورم في الدماغ فقط عن طريق الفحص النسيجي لعينات الأنسجة السرطانية التي يتم الحصول عليها إما عن طريق خزعة الدماغ أو الجراحة المفتوحة. الفحص النسيجي أمر ضروري لتحديد العلاج المناسب والتشخيص الصحيح. هذا الفحص، الذي يؤديه الطبيب الشرعي، يتم على ثلاث مراحل: فحص خلال العملية من أنسجة جديدة، الفحص المجهري الأولي لأنسجة معدّة، ومتابعة فحص الأنسجة المعدة بعد الفحص الكيميائي الهستولوجي المناعى أو التحليل الجيني.
علم الأمراض
الأورام لها خصائص تسمح بتحديد إذا ما كانت خبيثة أو كيف سوف تتطور، وتحديد هذه الخصائص يسمح للفريق الطبي بتحديد خطة للعلاج. كشم أو فقد التمايز: فقدان تمايز الخلايا أو ترابطها، وهي سمة من سمات الأنسجة السرطانية المتحولة. فتفقد الخلايا المتحولة السيطرة الكاملة على وظائفها العادية والعديد منها يتدهور هياكل الخلية لها. الخلايا المتحولة غالبا ما تكون فيها نسب النووية للسيتوبلازم (الحشوة) عالية بشكل غير طبيعي، وكثير منها يكون متعدد النوى. بالإضافة إلى ذلك، نوى الخلايا المتحولة عادة ما تكون على شكل غير طبيعي أو متضخم. الخلايا يمكن أن تصبح كشمي بطريقتين: الخلايا السرطانية الورمية يمكن ان تصبح بدائية، أو الخلايا الجذعية السرطانية يمكن أن تزيد في قدرتها على التكاثر (أي نمو غير مسيطر عليه بسبب فشل التمايز).[16]
النمطية: مؤشرا على خلل في الخلية (والتي قد تكون مؤشرا لورم خبيث). أهمية الاختلاف تعتمد بشكل كبير على المحتوى. الأورام: هو انقسام الخلايا (غير المنضبط). على هذا النحو، الأورام ليست هي المشكلة بل نتائجها: فالانقسام الغير منتهي يزيد حجمها، وإذا كانت في مكان ضيق مثل تجويف الجمجمة تتطور المشكلة بسرعة لأن الكتلة ستجتاح مكان الدماغ وتدفعه جانبا، مما يؤدي إلى الضغط على أنسجة الدماغ، وزيادة الضغط داخل الجمجمة وتدمير حمة الدماغ (النسيج الحشوي). زيادة الضغط داخل الجمجمة (ICP) قد يعزى إلى التأثير المباشر لحجم الورم، زيادة حجم الدم، أو زيادة حجم السائل النخاعي (CSF)، والتي قد تسبب بدورها أعراض ثانوية. موت الخلايا (النخر): موت الخلايا، الناجم عن عوامل خارجية مثل العدوى، السم أو الصدمة. الخلايا الميتة تقوم بإرسال إشارات كيميائية خاطئة فتمنع الخلايا البالعة من التخلص من الخلايا الميتة، مما يؤدي إلى تراكم الأنسجة الميتة، وحطام الخلية والسموم في أو بالقرب من موقع الخلايا الميتة.[16] نقص الأكسجين في الشراين والأوردة، أو فقدان الإمدادات الكافية من الأوكسجين إلى مناطق معينة من الدماغ، تحدث عندما يستغل الورم امدادات الدم المحيطة بالنسيج الطبيعي ليتنافس معه في أخذ الغذاء والاوكسجين. إن أكثر الأورام تسبب إطلاق المنتجات النهائية لعمليات الأيض (على سبيل المثال، الايونات الحرة، معادن، نواقل عصبية)، وإطلاق السيتوكينات التي تعطل وظيفة النسيج العادي. التصنيف
الأورام الثانوية
الأورام الثانوية من الدماغ هي من النوع الذي ينتشر، وتكون قد غزت الدماغ من السرطانات التي تنشأ في الأجهزة الأخرى. هذا يعني أن الورم نشأ في عضو اخر من الجسم ثم انتشر عن طريق نظام الأوعية الدموية والنظام اللمفاوي. وبعد ذلك وصلت لمجرى الدم، واخيرا استقرت في الدماغ لتستمر في النمو والانقسام. أصبحت الأورام الثانوية شائعة في المرضى الذين يعانون من سرطان في أي مكان من الجسد غير قابل الشفاء. الأنواع الأكثر شيوعا من السرطانات التي أدت إلى إحداث أورام ثانوية في الدماغ هي: سرطان الرئة، سرطان الثدي، سرطان الجلد الخبيث، سرطان الكلى وسرطان القولون (بالترتيب التنازلي تبعا للتكرار).
أورام المخ الثانوية أكثر شيوعا من تلك الأولية؛ في الولايات المتحدة هناك حوالي 170000 حالة جديدة كل عام. ان أورام الدماغ الثانوية هي السبب الأكثر شيوعا للأورام في تجويف داخل الجمجمة. ويمكن أيضا أن تكون عظام الجمجمة عرضة للورم لأنه بطبيعته يقلل من حجم التجويف داخل الجمجمة، ويمكن أن يسبب تلفا في الدماغ.[17] من خلال السلوك أورام الدماغ أو الأورام داخل الجمجمة يمكن أن تكون سرطانية (خبيثة) أو غير سرطانية (حميدة). ومع ذلك، فإن تعريف الأورام الخبيثة أو الحميدة يختلف عن تلك المستخدم عادة في أنواع أخرى من الأورام السرطانية أو غير سرطانية في الجسم. الاورام الحميدة لا تغزو النسيج المحيط، ثلاث خصائص تميز الاورام الخبيثة من الحميدة .
•الانقسام غير المنضبط (النمو والانقسام أكثر من الحدود الطبيعية).
•كشم: الخلايا في الأورام لها شكل مختلف واضح (الحجم والشكل). الخلايا المتحولة عادة تتعدد فيها الأشكال الملحوظة. نواة الخلايا السرطانية تتميز للغاية بانها فائقة التلون وكبيرة الجحم. قد يصل حجم النواة بنفس حجم سيتوبلازم الخلية (نسبة النوية إلى الحشوية قد نقترب 1: 1، بدلا من العادية 1: 4 أو 1: 6). الخلايا العملاقة - أكبر بكثير من جيرانهم - قد تشكل وتمتلك إما نواة هائلة واحدة أو عدة أنوية. نوى الخلايا المتحولة متغيرة وغريبة في الحجم والشكل.
•الغزو أو التسلل: هو التوسع المكاني للورم عن طريق الانقسام غير المنضبط، بمعنى أن الأورام تغزو الحيز الذي تشغله الأنسجة المجاورة، مما يدفع بالأنسجة الأخرى جانبا ويسبب ضغط على الأنسجة. غالبا ما تكون هذه الاورام واضحة عند التصوير. التسلل هو سلوك الورم إما أن ينمو كالمخالب ينغرس في الانسجة الطبيعية المحيطة (في كثير من الأحيان مما يجعل الخطوط العريضة للورم غير واضحة) أو أن تكون الخلايا السرطانية في الأنسجة خارج المحيط من كتلة ورمية؛ هذا لا يعني أن الورم الارتشاحي لا يأخذ مساحة أو لا يضغط الأنسجة المحيطة به لأنه ينمو، ولكن في أورام التسلل، من الصعب الجزم من أين ينتهي الورم اومن اين تبدأ الأنسجة السليمة.
بعض خصائص الاورام الخبيثة لا تنطبق على الأورام في الدماغ:
نادرا ما تنتقل أورام الدماغ الأولية إلى الأعضاء الأخرى. يمكن لبعض أشكال أورام الدماغ الأولية الانتقال لكن لن تنتشر خارج تجويف الجمجمة أو القناة الشوكية المركزية. يرجع ذلك إلى حاجز الدماغي للدم BBB.[18] العديد من نظم التصنيف تستخدم لتصنيف الورم في الجهاز العصبي المركزي، وتستخدم منظمة الصحة العالمية (WHO) نظام الدرجات للورم النجمي. أنشئت في عام 1993 منظمة الصحة العالمية في محاولة لإزالة الالتباس بشأن التشخيص، أربعة مستويات نسيجية لتصنيف الأورام النجمية من 1- 4، 1 الأقل عدوانية و4 الأكثر عدوانية.
الأنواع
يمكن أن تكون الأورام حميدة أو خبيثة، ويمكن أن تحدث في أجزاء مختلفة من الدماغ، ويمكن أن تكون أولية أو ثانوية. الورم الأولي هو الذي بدأ في الدماغ، عكس الورم النقيلي، وهو الورم الذي قد انتشر إلى الدماغ من جزء آخر في الجسم.[19] والورم النقيلي أكثر انتشارًا من الأورام الأولية بنسبة 4: 1.[20] الأورام قد تكون لها أعراض أو لا تكون: يتم اكتشاف بعض الأورام لأن المريض يعاني من أعراض، أما البعض الآخر يكتشف بالصدفة على المسح الضوئي والتصوير، أو في تشريح الجثة.
وأورام الدماغ الأولية الأكثر شيوعا هي:[21]
•الأورام الدبقية (50.4٪)
•السحائية (20.8٪)
•أورام الغدة النخامية (15٪)
•أورام العصب غمد (8٪)
ويمكن أيضًا أن يتم تصنيف هذه الأورام للأكثر شيوعًا وفقًا للأنسجة الأصلية كما هو موضح أدناه:[22]
| المنشأ النسيجي | الأطفال | البالغين |
|---|---|---|
| الخلايا النجمية | الخلايا النجمية الشعرية (PCA) | ورم أرومي دبقي الأشكال (GBM) |
| خلايا قليلة التغصن | ورم الدبقيات القليلة التغصن | |
| خلايا البطانة العصبية | البطانة العصبية | |
| الخلايا العصبية | نخاعي | |
| السحايا | سحائي |
العلاج .
عندما يتم تشخيص ورم في الدماغ، يتم تشكيل فريق طبي لتقييم الخيارات العلاجية التي يقدمها الجراح للمريض وعائلته. نظرا لموقع الأورام الصلبة الأولية في الدماغ يجب القيام بعملية العلاج. اخصائي الاعصاب يأخذ وقتا لملاحظة تطور الورم قبل البدأ بالتخطيط للعلاج.
أنواع العلاج المختلفة تعتمد على نوع الورم وموقعه. الجمع بين هذه الطرق قد يعطي نسبة أفضل للشفاء.
الجراحة: الاستئصال الكامل أو الجزئي للورم مع الهدف المتمثل في إزالة أكبر قدر ممكن من الخلايا السرطانية .
العلاج الإشعاعي: العلاج الأكثر شيوعا لعلاج أورام الدماغ. يتعرض المريض في هذا النوع من العلاج لاشعة بيتا، الأشعة السينية أو أشعة جاما. العلاج الكيميائي: هو خيار لعلاج السرطان، ولكن نادرا ما يتم استخدامه لعلاج أورام الدماغ بسبب حاجز الدم في الدماغ الذي يقوم بمنع الأدوية من الوصول إلى الخلايا السرطانية. ويمكن اعتبار العلاج الكيميائي بمثابة العلاج الذي يمنع نمو وتقسيم جميع الخلايا في الجسم بما في ذلك الخلايا السرطانية. هذا يتسبب في آثار جانبية كبيرة يعاني منها المرضى الذين يخضعون للعلاج الكيميائي. تتوفر من خلال التجارب السريرية مجموعة متنوعة من العلاجات التجريبية.
تعتمد معدلات البقاء على قيد الحياة في أورام الدماغ الأولية على نوع الورم، والعمر، والحالة الوظيفية للمريض، ومدى إزالة الورم الجراحية وغيرها من العوامل المحددة لكل حالة.[23]
الجراحة
النوع الأساسي والمفضل من أنواع العلاج. الهدف الرئيسي من العلاج بالجراحة هو إزالة أكبر عدد ممكن من خلايا الورم، مع إزالة كاملة كونها تعطي أفضل النتائج.[24] في بعض الحالات الوصول إلى الورم أمر مستحيل ويمنع عمل الجراحة.
العديد من الأورام السحائية، باستثناء بعض الأورام الموجودة في قاعدة الجمجمة، يمكن إزالتها جراحيا بنجاح. معظم أورام الغدة النخامية يمكن ازالتها جراحيا، وغالبا ما يصل اليها عن طريق التجويف الانفي، وقاعدة الجمجمة (عبر الأنف، عبر العظم الوتدي). أورام الغدة النخامية الكبيرة تتطلب (فتح الجمجمة) لإزالتها. العلاج الإشعاعي، بما في ذلك التوجه اللمسي، محجوز للحالات الغير صالحة للجراحة. حاليا تهدف العديد من الدراسات البحثية لتحسين الاستئصال الجراحي للأورام الدماغية عن طريق وضع العلامات للخلايا السرطانية مع حمض 5-أمينوليفولنيك ويمكن أن يسبب لهم التوهج.[25] العلاج الإشعاعي والعلاج الكيميائي بعد الجراحة هو امر مهم في لأورام الخبيثة. ويمكن أيضا تعالج الأمراض نهائيا بالعلاج الكيميائي أو الاشعاعي لكن عندما نعجز عن ذلك نلجأ للجراحة. في أي عملية جراحية في الدماغ قد يعاني المريض من نوبات صرعية تختلف في شدتها. يمكن التحكم بها مستقبلياً عن طريق إعطاء أدوية خاصة لوقف النوبات الاهتزازية.
العلاج الإشعاعي
الهدف من العلاج الإشعاعي هو قتل الخلايا السرطانية بينما تترك أنسجة الدماغ السليمة دون أن تصاب بأذى. في العلاج الإشعاعي الخارجي القياسي، يتم تطبيق علاجات متعددة من جرعة قياسية من الإشعاع إلى الدماغ. يتم تكرار هذه العملية ليصبح المجموع 10-30 جلسة علاجية، يقدم هذا العلاج للمرضى نتائج أفضل وفرص أكبر للنجاة.
الجراحة الشعاعية هي طريقة العلاج التي تستخدم حسابات محوسبة لتركيز الإشعاع في موقع الورم بنفس الوقت تقلل جرعة الإشعاع إلى الانسجة المحيطة بها. قد تكون الجراحة الإشعاعية مساعد للعلاجات الأخرى، أو أنها قد تمثل العلاج الاساسي. وتشمل النماذج المستخدمة الاشعاعية المجسمة، مثل سكين غاما، (Cyberknife), أو نوفاليس تكساس الشعاعية.[26] أكثر العلاجات الاشعاعية شيوعا، العلاج الإشعاعي الموضعي والعلاج بالبروتون الذي يستخدم خصوصا للأطفال. العلاج الإشعاعي هو العلاج الأكثر شيوعا لعلاج أورام الدماغ الثانوية. حجم العلاج الإشعاعي يعتمد على حجم المنطقة من الدماغ المتضررة من السرطان. الشعاع الخارجي التقليدي «العلاج الاشعاعي للدماغ كاملاً» (WBRT) أو «تشعيع كامل الدماغ» قد يقترح إذا كان هناك خطر يتمثل في أن هناك أورام ثانوية أخرى ستتطور في المستقبل.[27] وعادة ما ينصح العلاج الإشعاعي المجسم في الحالات التي تنطوي على أقل من ثلاثة أورام ثانوية صغيرة في الدماغ. الناس الذين يتعرضون للإشعاع المجسم (SRS) والعلاج الإشعاعي الكامل للدماغ (WBRT) لعلاج أورام الدماغ المنتشر لديهم خطر أكثر بمرتين للإصابة بمشاكل التعلم والذاكرة من الذين عولجوا بSRS وحدها. .[28][29]
العلاج الكيميائي
المرضى الذين يخضعون للعلاج الكيميائي يتعرضون لأدوية مصممة لقتل الخلايا السرطانية. على الرغم من أن العلاج الكيميائي قد يحسن البقاء على قيد الحياة في المرضى الذين يعانون من أورام الدماغ الأولية الخبيثة، فإنه يفعل ذلك فقط في حوالي 20 بالمئة من المرضى. وكثيرا ما يستخدم العلاج الكيميائي في الأطفال الصغار بدلا من الإشعاع، لأن الإشعاع قد يكون له تأثيرات سلبية على الدماغ في مرحلة النمو. ويستند القرار بأن يوصف هذا العلاج على صحة المريض ، ونوع الورم، ومدى تطور السرطان. يعاني المرضى في هذا العلاج من سمية الأدوية والعديد من الآثار الجانبية للأدوية. .نشرت UCLA Neuro-Oncology بيانات عن نجاة المرضى الذين شخصوا بالورم الأرومي الدبقي متعدد الأشكال. تعتبر UCLA Neuro-Oncology المؤسسة الوحيدة في الولايات المتحدة التي تعرض كيفية استجابة مرضى الاورام الدماغية. وهي تظهر أيضا قائمة مواد العلاج الكيميائي المستخدمة لعلاج الأورام من الدرجة العالية.[30] أخرى يمكن أن تستخدم تحويلة لتخفيف الأعراض الناجمة عن الضغط داخل الجمجمة، عن طريق الحد من تراكم السائل الناجم عن انسداد في التدفق الحر للسائل النخاعي.[31]
التشخيص
يعتمد التشخيص على نوع السرطان. الورم الارومي النخاعي يتفاعل جيدا مع العلاج الكيميائي، العلاج الإشعاعي، والاستئصال الجراحي. بينما الورم الأرومي الدبق مختلف الشكل له احتمالية نجاة تقدر ب12 شهرا حتى مع أقوى العلاجات الكيميائية والجراحة. الأورام الدبقية في جذع الدماغ لديها أفقر الاستجابات من أي شكل من أشكال سرطان الدماغ، معظم المرضى يموتون خلال سنة واحدة، وحتى مع العلاج الذي يتكون عادة من الإشعاع على الورم مع الستيرويدات القشرية. مع ذلك، نوع واحد من الاورام الدبقية في جذع الدماغ لديها تفاعل جيد مع العلاج واحتمالية نجاة عالية.[32]
ورم أرومي الأشكال
ورم أرومي الأشكال هو الشكل الأكثر عدوانية (الصف الرابع)، والأكثر شيوعا بين الأورام الخبيثة في الدماغ. حتى عند استخدام العلاج المتعدد الطرق ((multimodality القوي الذي يتكون من العلاج الإشعاعي، والعلاج الكيميائي، والاستئصال الجراحي، تبقى احتمالية الحياة 12 إلى 17 شهرا فقط. العلاج القياسي لورم أرومي الأشكال يتكون من الاستئصال الجراحي للورم، يليه العلاج الإشعاعي بين اثنين وأربعة أسابيع بعد العملية الجراحية لإزالة السرطان، ثم العلاج الكيميائي. معظم المرضى الذين يعانون من ورم أرومي يأخذون كورتيكوستيرويد، وعادة ديكساميثازون، أثناء مرضهم لتخفيف الأعراض. وتشمل العلاجات التجريبية سكين جاما الاشعاعية [33]، علاج القبض على البورون النيوترون ونقل الجينات.[34][35]
ورم الدبقيات القليلة التغصن ورم الدبقيات القليلة التغصن هو ورم غير قابل للعلاج لكن بطيء التطور يمكن علاجه بالاستئصال الجراحي، والعلاج الكيميائي والعلاج الإشعاعي أو مزيج منهم. بالنسبة لبعض المرضى المصابين بدرجة اقل (الدرجة الثاني)، يتم علاج الأعراض فقط. تظهر هذه الأورام طفرات حذف على كل من P و Q من كروموسوم 1 (1p19q)، وقد وجد أنها حساسة للعلاج الكيماوي وقد اثبت ذلك في أحد الأبحاث أن هذه الأورام حساسة للعلاج الكيماوي.[35] معدل البقاء على قيد الحياة هو 16.7 سنة للدرجة الثاني.[36]
علم الأوبئة
أرقام حالات سرطانات الدماغ تظهر فرقا كبيرا بين البلدان النامية والمتطورة (البلدان الأقل نموا لديها حالات أقل من أورام الدماغ) [37] ، - وهذا يمكن تفسيره بأن الوفيات الناجمة عن ورم غير مشخصة (المرضى في حالات الفقر المدقع لا يحصلون على تشخيص، ببساطة لأنهم لا يستطيعون الوصول إلى المرافق التشخيصية الحديثة اللازمة لتشخيص ورم في المخ) والوفيات الناجمة عن أسباب مرتبطة بالفقر الأخرى التي تسبق ظهور الأورام. ومع ذلك الدراسات تشير إلى أن أشكال معينة من أورام الدماغ الأولية هي أكثر انتشارا بين فئات معينة من السكان. أظهرت الدراسات حدوث أورام الجهاز العصبي المركزي في الولايات المتحدة، وإسرائيل، والدول الاسكندنافية مرتفع نسبيا، في حين أن اليابان والدول الآسيوية لديهم معدلات أقل. هذه الاختلافات ربما تعكس بعض الاختلافات البيولوجية وكذلك الاختلافات في تشخيص المرضي وتقديم التقارير.[38] البيانات في جميع أنحاء العالم المتعلقة باللإصابة بسرطان يمكن العثور عليها في (WHO) منظمة الصحة العالمية والتعامل معها من قبل (وكالة IARC الدولية لبحوث السرطان) الموجود في فرنسا.[39]
الولايات المتحدة الأمريكية
بالنسبة للولايات المتحدة في عام 2005 كان من المتوقع أن يكون هناك 43800 حالة جديدة من حالات أورام المخ [40][41] التي مثلت أقل من 1 في المئة من جميع حالات السرطان، و 2.4 في المئة من مجموع وفيات السرطان [42]، و 20-25 في المئة من السرطانات التي تصيب الأطفال.[42][43] ، تشير التقديرات إلى وجود 13000 حالة وفاة سنويا في الولايات المتحدة وحدها نتيجة لأورام المخ [41] المملكة المتحدة أورام الدماغ، الجهاز العصبي المركزي أو غيرها من الأورام داخل الجمجمة هي تاسع أكثر أنواع السرطانات شيوعا في المملكة المتحدة (تم تشخيص نحو 9400 شخص في عام 2011)، وهذا هو ثامن أكثر الأسباب شيوعا لوفيات السرطان (توفي حوالي 5200 شخص في عام 2012).[44]
العلاج
العلاج المناعي
لم يتم اكتشاف أي علاج للأورام الدبقية الخبيثة.[45] التهاب الفم الحويصلي الفيروسي في عام 2000، استخدم الباحثون فيروس التهاب الفم الحويصلي، أو VSV، لاصابة وقتل الخلايا السرطانية دون التأثير على الخلايا السليمة.[46][47] الاكتشاف الأولي للفيروس اقتصر على أنواع قليلة من السرطان. وقد حددت عدة دراسات مستقلة العديد من الأنواع التي تكون عرضة لهذا الفيروس، بما في ذلك خلايا سرطان الورم الأرومي الأشكال، والتي تمثل غالبية أورام الدماغ. في عام 2008، قام الباحثون بتصميم سلالات من VSV تميزت باقل سمية للخلايا الطبيعية. هذا التقدم يسمح بحقن الفيروس دون التناول المتزامن مع مضاد للفيروسات. الفيروس يمكن أن يعطى عن طريق الوريد أو عن طريق العصب الشمي. في مجال البحوث، تم زرع ورم الدماغ البشري في عقول الفئران. وقد أجريت بحوث على العلاج الفيروسي مثل هذا، ولكن لم تظهر أي فيروسات أخرى لتكون فعالة مثل VSV.
ناقلات نسخ فيروسات النسخ العكسي
بقيادة الأستاذ نوري كاساهارا ذكر باحثون من جامعة جنوب كاليفورنيا، في عام 2001 أول مثال ناجح لتطبيق استخدام ناقلات نسخ الفيروسات نحو نقل الخلايا المشتقة من الأورام الصلبة.[48] وبناء على هذا العمل الأولي، استخدم الباحثون هذه التقنية على نماذج في الجسم الحي من السرطان، وفي عام 2005 ذكروا الفائدة منها للنجاة على المدى الطويل بعد دراسات على الورم الدماغي في الفئران .[49] وفي وقت لاحق، استعدادا للتجارب السريرية على الإنسان، تم تطوير هذه التكنلوجيا من قبل Tocagen (شركة أدوية تركز في المقام الأول على علاجات سرطان الدماغ) كعلاج مركب (TOCA 511 & TOCA FC). وقد كان هذا قيد الدراسة منذ عام 2010 في المرحلة I / II كانت التجارب السريرية لعلاج تكرر رجوع الاورام. حتى الآن لم تنشر النتائج.[50]
الأطفال
في الولايات المتحدة، يتم تشخيص حوالي 2000 من الأطفال والمراهقين الذين تقل أعمارهم عن 20 سنة من العمر على وجود ورم خبيث في الدماغ. تم الإبلاغ عن معدلات أعلى للإصابة في 1985-1994 مما كانت عليه في 1975-1983. هناك بعض النقاشات حول الأسباب؛ أحد النظريات هي نتيجة لتحسن التشخيص وإعداد التقارير، حيث أنه منذ أن بدأ استخدام الرنين المغناطيسي في الفحص على نطاق واسع ارتفعت نسب الإصابة وبقي معدل الوفيات كما هو. وكان متوسط معدل البقاء على قيد الحياة في الأطفال حوالي 60٪. النسبة تختلف اعتمادا على نوع السرطان والعمر، المرضى الأصغر سنا يكون معدل الوفيات بينهم اعلى .[51]
في الأطفال دون سن 2، حوالي 70٪ من أورام الدماغ هي الأورام الأرومية النخاعية، الورم البطاني العصبي، الورم الدبقي. الأورام الأقل شيوعا، والتي عادة ما ينظر إليها عند الرضع، هي المسخي، والورم المسخي المعيني الغير نمطي[52] أورام الخلايا الجرثومية، بما في ذلك مسخي، يشكلون 3٪ فقط من أورام الدماغ الأولية للأطفال، ولكن الإصابة في جميع أنحاء العالم تختلف بشكل كبير.[53]
المراجع
- ^ أ ب "General Information About Adult Brain Tumors". NCI. 14 أبريل 2014. مؤرشف من الأصل في 2015-04-25. اطلع عليه بتاريخ 2014-06-08.
- ^ أ ب ت ث ج ح 1. "General Information About Adult Brain Tumors". NCI. 2014-04-14. Retrieved 8 June 2014.
- ^ Jump up to:a b c d e f g h i j k "Adult Brain Tumors Treatment". NCI. 2014-02-28. Retrieved 8 June2014.
- ^ 3. Jump up^ Longo, Dan L (2012). "369 Seizures and Epilepsy". Harrison's principles of internal medicine (18th ed.). McGraw-Hill. p. 3258. (ردمك 978-0-07-174887-2)
- ^ أ ب ت ث ج ح خ د ذ Jump up to:a b c d e f g h i j k "Adult Brain Tumors Treatment". NCI. 2014-02-28. Retrieved 8 June2014
- ^ أ ب ت ث ج ح خ د 4. ^ Jump up to:a b c d e f g h World Cancer Report 2014. World Health Organization. 2014. pp. Chapter 5.16. ISBN 92-832-0429-8
- ^ 1. "General Information About Adult Brain Tumors". NCI. 2014-04-14. Retrieved 8 June 2014
- ^ 5. Jump up^ "SEER Stat Fact Sheets: Brain and Other Nervous System Cance". NCI. Retrieved18 June 2014.
- ^ 6. Jump up^ World Cancer Report 2014. World Health Organization. 2014. pp. Chapter 1.3.ISBN 92-832-0429-8
- ^ 7. Jump up^ "Brain Tumour Facts 2011". Brain Tumour Alliance Australia. Archived from the original (PDF) on 20 Nov 2014. Retrieved 9 June 2014.
- ^ 8. Jump up^ Krishnatreya, M; Kataki, AC; Sharma, JD; Bhattacharyya, M; Nandy, P; Hazarika, M (2014). "Brief descriptive epidemiology of primary malignant brain tumors from North-East India.". Asian Pacific journal of cancer prevention : APJCP 15 (22): 9871–3.doi:10.7314/apjcp.2014.15.22.9871. ببمد: 25520120.
- ^ 9. Jump up^ Kleihues P, Ohgaki H, Eibl RH, Reichel MB, Mariani L, Gehring M, Petersen I, Höll T, von Deimling A, Wiestler OD, Schwab M (1994). "Type and frequency of p53 mutations in tumors of the nervous system and its coverings". Molecular Neuro-oncology and Its Impact on the Clinical Management of Brain Tumors. Recent results in cancer research 135. Springer. pp. 25–31. ISBN 3-540-57351-8
- ^ 10. Jump up^ Frei P, Poulsen AH, Johansen C, Olsen JH, Steding-Jessen M, Schüz J (19 October 2011). "Use of mobile phones and risk of brain tumours: update of Danish cohort study.".BMJ (Clinical research ed.) 343: d6387. doi:10.1136/bmj.d6387. PMC 3197791.ببمد: 22016439
- ^ 11. Jump up^ "IARC classifies radiofrequency electromagnetic fields as possibly carcinogenic to humans" (PDF). World Health Organization press release N° 208 (Press release).International Agency for Research on Cancer. 31 May 2011. Retrieved 2 June 2011.
- ^ أ ب 12. ^ Jump up to:a b Herholz K, Langen KJ, Schiepers C, Mountz JM (November 2012). "Brain tumors".Semin Nucl Med 42 (6): 356–70. doi:10.1053/j.semnuclmed.2012.06.001.PMC 3925448. ببمد: 23026359.
- ^ أ ب 13. Jump up^ MedlinePlus Encyclopedia Necrosis
- ^ 14. Jump up^ Chen, Yi-Bin. "Metastatic Brain Tumor: MedlinePlus Medical Encyclopedia." A.D.A.M., Inc. U.S. National Library of Medicine, 12 May 2015. Web. 3 June 2015.http://www.nlm.nih.gov/medlineplus/ency/article/000769.htm نسخة محفوظة 2016-07-05 على موقع واي باك مشين.
- ^ 15. Jump up^ Frappaz D, Mornex F, Saint-Pierre G, Ranchere-Vince D, Jouvet A, Chassagne-Clement C, Thiesse P, Mere P, Deruty R (1999). "Bone metastasis of glioblastoma multiforme confirmed by fine needle biopsy". Acta neurochirurgica (Wien) 141 (5): 551–552.doi:10.1007/s007010050342. ببمد: 10392217
- ^ 16. Jump up^ "What you need to know about brain tumors". National Cancer Institute. Retrieved25 February 2012
- ^ 17. Jump up^ Merrel RT (Dec 2012). "Brain tumors.". Dis Mon. 58 (12): 678–89.doi:10.1016/j.disamonth.2012.08.009. ببمد: 23149521
- ^ 18. Jump up^ Park, Bong Jin; Kim, Han Kyu; Sade, Burak; Lee, Joung H. (2009). "Epidemiology". In Lee, Joung H. Meningiomas: Diagnosis, Treatment, and Outcome. Springer. p. 11.(ردمك 978-1-84882-910-7).
- ^ 19. Jump up^ حسين عبد الستار. Pathoma.com
- ^ 20. Jump up^ Nicolato A, Gerosa MA, Fina P, Iuzzolino P, Giorgiutti F, Bricolo A (September 1995)."Prognostic factors in low-grade supratentorial astrocytomas: a uni-multivariate statistical analysis in 76 surgically treated adult patients". Surg Neurol 44 (3): 208–21; discussion 221–3. doi:10.1016/0090-3019(95)00184-0. ببمد: 8545771.
- ^ 21. Jump up^ Spetzler RF, Sanai N (2012). "The quiet revolution: Retractorless surgery for complex vascular and skull base lesions". Journal of Neurosurgery 116 (2): 291–300.doi:10.3171/2011.8.JNS101896. ببمد: 21981642
- ^ 22. Jump up^ Paul Brennan (4 August 2008). "Introduction to brain cancer". cliniclog.com. Retrieved19 December 2011
- ^ 23. Jump up^ "Radiosurgery treatment comparisons – Cyberknife, Gamma knife, Novalis Tx". Retrieved 22 July 2014
- ^ 24. Jump up^ "Treating secondary brain tumours with WBRT". Cancer Research UK. Retrieved5 June 2012
- ^ 25. Jump up^ "Whole Brain Radiation increases risk of learning and memory problems in cancer patients with brain metastases". MD Anderson Cancer Center. Retrieved 5 June 2012.
- ^ 26. Jump up^ "Metastatic brain tumors". International RadioSurgery Association. Retrieved 5 June2012.
- ^ 27. Jump up^ "How Our Patients Perform: Glioblastoma Multiforme". UCLA Neuro-Oncology Program. Retrieved 5 June 2012.
- ^ 28. Jump up^ Dalvi A. "Normal Pressure Hydrocephalus Causes, Symptoms, Treatment".eMedicineHealth. Emedicinehealth.com. Retrieved 17 February 2012.
- ^ 29. Jump up^ "Brain Stem Gliomas in Childhood". Childhoodbraintumor.org. Retrieved 17 February2012.
- ^ 30. Jump up^ "GBM Guide – MGH Brain Tumor Center". Brain.mgh.harvard.edu. Retrieved17 February 2012.
- ^ 31. Jump up^ Chien-Kuo Tai, Noriyuki Kasahara (1 January 2008). "Replication-competent retrovirus vectors for cancer gene therapy" (PDF). Frontiers in Bioscience 13: 3083–3095.doi:10.2741/2910. ببمد: 17981778.
- ^ أ ب 32. Jump up^ Murphy AM, Rabkin SD (Apr 2013). "Current status of gene therapy for brain tumors".Transl Res. 161 (4): 339–54. doi:10.1016/j.trsl.2012.11.003. ببمد: 23246627
- ^ 34. Jump up^ "Neurology". Neurology. Retrieved 17 February 2012.
- ^ 35. Jump up^ Bondy ML, Scheurer ME, Malmer B et al. (2008). "Brain Tumor Epidemiology: Consensus from the Brain Tumor Epidemiology Consortium (BTEC)". Cancer 113 (7 Suppl): 1953–1968. doi:10.1002/cncr.23741.
- ^ 36. Jump up^ Jallo GI, Benardete EA (January 2010). "Low-Grade Astrocytoma"
- ^ 37. Jump up^ "CANCERMondial". International Agency for Research on Cancer. Retrieved17 February 2012.
- ^ 38. Jump up^ "Central Brain Tumor Registry of the United States, Primary Brain Tumors in the United States, Statistical Report, 2005–2006" (PDF). Retrieved 23 July 2014.
- ^ أ ب 39. ^ Jump up to:a b Greenlee RT, Murray T, Bolden S, Wingo PA (2000). "Cancer statistics, 2000". CA Cancer J Clin 50 (1): 7–33. doi:10.3322/canjclin.50.1.7. ببمد: 10735013
- ^ أ ب 40. ^ Jump up to:a b "What are the key statistics about brain and spinal cord tumors?". American Cancer Society. May 1, 2012.
- ^ 41. Jump up^ Chamberlain MC, Kormanik PA (February 1998). "Practical guidelines for the treatment of malignant gliomas". West J Med. 168 (2): 114–20. PMC 1304839. ببمد: 9499745.
- ^ 42. Jump up^ "Brain, other CNS and intracranial tumours statistics". Cancer Research UK. Retrieved27 October 2014.
- ^ 43. Jump up^ Bloch, O (2015). "Immunotherapy for malignant gliomas.". Cancer treatment and research163: 143–58. doi:10.1007/978-3-319-12048-5_9. ببمد: 25468230
- ^ 44. Jump up^ Auer R, Bell JC (January 2012). "Oncolytic viruses: smart therapeutics for smart cancers". Future Oncology 8 (1): 1–4. doi:10.2217/fon.11.134. ببمد: 22149027.
- ^ 45. Jump up^ Garber K (1 March 2006). "China Approves World's First Oncolytic Virus Therapy For Cancer Treatment". J Natl Cancer Inst 98 (5): 298–300. doi:10.1093/jnci/djj111.ببمد: 16507823
- ^ 46. Jump up^ Logg CR, Tai CK, Logg A, Anderson WF, Kasahara N (20 May 2001). "A uniquely stable replication-competent retrovirus vector achieves efficient gene delivery in vitro and in solid tumors". Human Gene Therapy 12 (8): 921–932. doi:10.1089/104303401750195881.ببمد: 11387057
- ^ 47. Jump up^ Tai CK, Wang WJ, Chen TC, Kasahara N (November 2005). "Single-shot, multicycle suicide gene therapy by replication-competent retrovirus vectors achieves long-term survival benefit in experimental glioma". Molecular Therapy 12 (5): 842–851.doi:10.1016/j.ymthe.2005.03.017. ببمد: 16257382
- ^ 48. Jump up^ "A Study of a Retroviral Replicating Vector Administered to Subjects With Recurrent Malignant Glioma". Clinical Trials.gov. July 2014.
- ^ 49. Jump up^ Gurney JG, Smith MA, Bunin GR. "CNS and Miscellaneous Intracranial and Instraspinal Neoplasms" (PDF). SEER Pediatric Monograph. National Cancer Institute. pp. 51–57. Retrieved 4 December 2008. In the US, approximately 2,200 children and adolescents younger than 20 years of age are diagnosed with malignant central nervous system tumors each year. More than 90 percent of primary CNS malignancies in children are located within the brain.
- ^ 50. Jump up^ Rood BR. "Infantile Brain Tumors". The Childhood Brain Tumor Foundation. Retrieved23 July 2014.
- ^ 51. Jump up^ Echevarría ME, Fangusaro J, Goldman S (June 2008). "Pediatric central nervous system germ cell tumors: a review". Oncologist 13 (6): 690–9. doi:10.1634/theoncologist.2008-0037. ببمد: 18586924
انظر أيضًا
- نقيلة دماغية
- التأقين
- قائمة بأشهر المرضى المصابين بأورام المخ
- الجراحة الإشعاعية
- الجراحة النمطية
- علاج إشعاعي
- درجات أورام الجهاز العصبي المركزي
- Visualase تقنية الليزر لتذرية الأورام (LITT)
وصلات خارجية
- Brain and CNS cancers على مشروع الدليل المفتوح
- معلومات ورم الدماغ من منظمة Cancer Research المملكة المتحدة (بالإنجليزية)
- Cancer.Net: Brain Tumor - معلومات من الجمعية الأمريكية لعلم الأورام السريري (بالإنجليزية)
- علم الأورام العصبي: توجيهات إدارة السرطان (بالإنجليزية)
- MayoClinic: Brain tumor Medical Encyclopedia
- Brain Tumor: Definitions Neurosurgery UCLA
- MedPix Teaching File MR Scans of Primary Brain Lymphoma, etc.
| ورم الدماغ في المشاريع الشقيقة: | |