|
تضامنًا مع حق الشعب الفلسطيني |
ظاهرة العبور والارتباط الوراثي
ظاهرة العبور والارتباط في علم الوراثة (تكون الطفرات) هو نوع من الانتقال الجيني أو الانقسام الخلوي الذي قد يحدث أثناء مرحلة الإنقسام المنصف (MEIOSIS) في كل من المخلوقات الحية الجنسية وغير الجنسية، حيث تعد دراسة الارتباط والعبور الوراثي في المخلوقات غير الجنسية إحدى الطرق لفهم الطفرات الوراثية لأنها تعد المصدر الوحيد لمتابعة انتقال المورثات بالارتباط والعبور في خلية واحدة.[1] بالإضافة إلى ذلك يمكن أن تؤدي ظاهرة العبور إلى التعبير عن الجينات المتنحية أو الغير متماثلة لدى الفرد وهذا التعبير له آثار مهمة لدراسة الأورام والجينات المتنحية الفتاكة.[2] تحدث عملية الارتباط المتماثل أو العبور بشكل رئيسي بين الكروماتيدات الشقيقة بعد مرحلة التضاعف (ولكن قبل انقسام الخلايا)، وهذا النمط من العبور المتماثل بين الكروماتيدات الشقيقة عادةً يكون صامت وراثياً (أي متنحي الصفات)، ويجدر الإشارة هنا إلى أن نسبة العبور بين الكروماتيدات المتماثلة ولكن غير شقيقة حوالي 1 ٪ مقارنة بالعبور في الكروماتيدات الشقيقة في مرحلة الانقسام المباشر.[3]
إكتشافها
تم اكتشاف ظاهرة العبور الوراثي من اكتشاف الطفرة النقطية في ذبابة الفاكهة السوداء المسماة بحشرة الدروسفيلا، حيث لوحظ هذا الاكتشاف المزدوج أو الفسيفساء في حشرة الدروسفيلا ميلانوقستر (D. melanogaster) في أوائل عام 1925م، ولكن قام دكتور كورت ستيرن (Curt Stern) في عام 1936م بشرح تفصيلي لهذة الظاهرة كنتيجة للانقسام المباشر، قبل اكتشاف دكتور ستيرون لقد افترض العلماء أن ظاهرة الطفرة النقطية قد حدثت لأن بعض الجينات لديها القدرة على التخلص من الكروموسوم الذي توجد عليه، [4] ولكن بعد هذا الاكتشاف العديد من التجارب قامت بتوضيح ما قد يحدث أثناء الانقسام المباشر في دورة الخلية وآلية حدوث ظاهرة العبور والارتباط الوراثي.
حدوثه
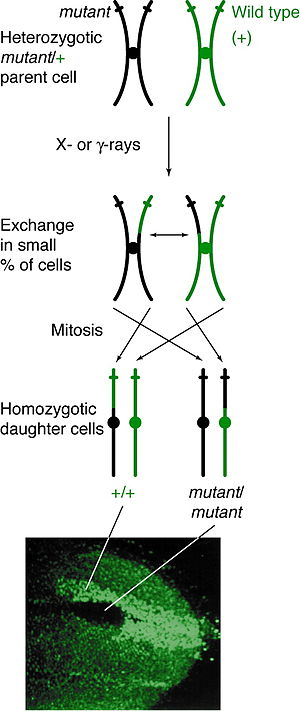
يمكن أن يحدث العبور في أي مرحلة من مراحل الانقسام ولكن يمكن ملاحظته بشكل واضح في الأفراد غير المتجانسة في صفات محددة، إذا حدث العبور بين الكروماتيدات غير الشقيقة في موقع محدد يؤثر هذا العبور في الصفات المحموله في تلك الجينات في نفس الموقع، ومن ثم كل من الكروموسومات المتجانسة سوف تكون كروماتيد الذي يحتوي على الصفات الوراثية مما ينتج عنه نمط ظاهري، ويعتمد النمط الظاهري الناتج على الطريقة التي تصطف بها الكروموسومات في مرحلة الطور البيني ما قبل الانقسام مباشرة، إذا حدث واحتوت هذه الكروماتيدات على أليلات مختلفة على نفس الجانب من الصف، فستظهر الخلايا الناتجة غير متجانسة وبذلك تكون غير قابلة للكشف بالرغم من حدوث عبور في الكروماتين، أما إذا اصطفت الكروماتيدات التي تحتوي على الأليلات متماثلة على نفس الجانب فإن الخلايا الناتجة ستكون متجانسة في هذا الموقع، مما ينتج عنه اكتشاف طفرة نقطية حيث تعرض إحدى خلاياه النمط الظاهري المتنحي متماثل اللزوجة بينما تحتوي الخلية الأخرى على النمط الظاهري للنوع البري المتجانس، وإذا استمرت تلك الخلايا الناتجة في التكرار والانقسام، فستستمر ظاهرة الطفرة النقطية في النمو مما ينتج عنه نمط جديد وهو النمط الظاهري الغير متجانس.
العبور يحدث خلال الطور البيني من الانقسام الخلوي وقد اقترح أن العبور قد يحدث بالتحديد خلال G1 من الانقسام، عندما يكون الحمض النووي DNA في مرحلته المزدوجة، ويتضاعف خلال مراحل الانقسام واعادة تكوين الـ DNA، [5] ومن الممكن أيضًا حدوث كسر أو تلف في الـ DNA مما يؤدي إلى تكون العبور أو الطفرة خلال G1 ، ولكن من مميزات الـ DNA اصلاح أي خلل يحدث اثناء عملية التضاعف في مراحل الانقسام.[6][7]
نواتج التلف في الحمض النووي DNA
في فطر الخميرة المعروف بـ Saccharomyces cerevisiae ينتج من حدوث الطفرة في جينات متعددة لازمة لعملية الانقسام المباشر وغير المباشرنتيجة لعبور المورثات إلى زيادة في حساسية الخلية للتثبيط الإشعاعي أو المواد الكيميائية السامة [8] على سبيل المثال الجين rad52 هو جين له دور فعال في عملية الانقسام المباشر [9] وكذلك الانقسام غير المباشر في الخلية [10] الخلايا الحاملة لطفرة في هذا الجين زادت حساسيتها للأشعة السينية وmethyl methanesulfonate وDNA crosslinking agent 8-methoxypsoralen-plus-UV light ، حيث يظهر أن الإصلاح التلقائي لـ DNA مهم وضروري لإزالة الأضرار الناتجة عن تلف الـ DNA من التعرض لهذه المركبات.
الية العبور
آلية العبور الوراثي تشبه الية الانقسام الاختزالي، وهي تشمل على الكروماتيدات الشقيقة والعمليات المتعلقة في اصلاح وترميم الحمض النووي DNA المزدوج بواسطة إعادة التركيب المتماثل او المتجانس مثل single-strand annealing وهي إصلاح التلف في كروماتيد واحد، التي تعتمد على التكوين من خلال ترجمة المورثات في الكروماتيد الآخر وتسمى بـ (synthesis-dependent strand annealing)، وتحويل الجينات أو ترجمة الجينات بواسطة مايقابلها من الكروماتين الآخر. بالإضافة إلى ذلك، فإن العبور غير المتجانس غالبًا يعزى إلى الارتباط غير المتماثل في الكروماتين.
طريقة حدوثه
هناك العديد من النظريات حول كيفية حدوث الطفرة أثناء عملية الانقسام، مثلاً في العبور البسيط يتداخل الكروماتيدان المتماثلان بالقرب أو في موقع قابل للكسر على الكروموسوم يعرف بـ (Chromosomal fragile site (CFS مما يؤدي إلى كسر او تلف مزدوج في كلا الكروماتيدان، [11] والذي يتم إصلاحه بعد ذلك باستخدام أحد الكروماتيدات وهذا ينتج عن عبور في مكانين مختلفين من الكروماتيد، في مثال آخر تشكل الكروماتيدات الشقيقة المتداخلة عبوراً مزدوجًا في موقع التضاعف الكروموسومي وهذا يتم إصلاحه لاحقًا بطريقة استبدال أو عبور المورثات. في كلا المثالين لا يمكن ضمان حدوث العبور الوراثي بشكل متجانس، أو حتى الارتباط على الجانبين المتجانسين وبالتالي فإن معظم أطوار الانقسام الخلوي لا تؤدي إلى عبورغالباً، أما العبور الغير متجانس ينتج عنه العديد من الآثار الضارة نتيجة لطفرات في جينات لا يمكن اصلاحها أو تعديلها.
بدلاً من ذلك، يمكن أن يحدث العبور أثناء عملية ترميم وإصلاح الحمض النووي [12] وحالة التلف الشديد قد يتم اختيار الكروموسوم المتجانس ليكون القالب لتكوين الكروماتيد الجديد، وهذا يؤدي إلى نسخ نسخة واحدة من الأليل من الكروموسوم المتجانس ومن ثم ربطها في الكروموسوم التالف، والأثر الناتج من هذه الآلية هو تكون كروموسوم مماثل وآخر غير مماثل.
المميزات والعيوب
من المعروف أن العبور الوراثي أو الطفرات تحدث في حشرة الدروسفيلا وبعض الفطريات التي تتكاثرلاجنسياً وفي الخلايا البشرية بشكل طبيعي، حيث قد يسمح بالتعبير عن الجينات المتنحية والمسببة للسرطان بشكل طبيعي وبالتالي تهيئ الخلية للانقسام وتكوين الورم السرطاني، كما أنه قد تنتج الخلية طفرة متجانسة للجين الحامل للورم السرطاني وهذا يؤدي إلى نفس النتيجة.[2] على سبيل المثال تتسبب متلازمة بلوم في حدوث طفرة في هليكس RecQ والتي تلعب دورًا في تضاعف الحمض النووي وإصلاحه، تؤدي هذه الطفرة إلى ارتفاع معدلات تكرار العبور الوراثي أو الطفرة عند الفئران، وهذا المعدل هو بدوره مسؤول عن التسبب في حساسية الورم في تلك الفئران.[13] في الوقت ذاته قد تكون الطفرة مفيدة وقد تلعب دورًا مهمًا في إصلاح التلف المزدوجة في الحمض النووي، وقد تكون مفيدة للمخلوق الحي إذا كان وجود أليلات سائدة متجانسة أكثر فعالية من غير المتجانسة، وهذا يشيع استخدامه في التجارب العلمية للمورثات أو الجينات في للمخلوقات الحية مثل حشرة الدروسفيلا، حيث يمكن احداث هذه الطفرات داخل المعمل من خلال استخدام الأشعة السينية ونظام إعادة التركيب FLP-FRT recombination system.[14]
المراجع
- ^ Hartl، Daniel L. and Maryellen Ruvolo (2012). Genetics: Analysis of Genetics and Genomes. Burlington: Jones & Bartlett.
- ^ أ ب Tischfield، Jay A. (نوفمبر 1997). "Loss of Heterozygosity, or: How I learned to Stop Worrying and Love Mitotic Recombination". American Journal of Human Genetics. ج. 61 ع. 5: 995–999. DOI:10.1086/301617.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ "Mitotic homologous recombination maintains genomic stability and suppresses tumorigenesis". Nat. Rev. Mol. Cell Biol. ج. 11 ع. 3: 196–207. 2010. DOI:10.1038/nrm2851. PMID:20177395.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ Stern، Curt (1936). "Somatic Crossing Over and Segregation in Drosophila Melanogaster". Genetics. ج. 21 ع. 6: 625–730.
- ^ Esposito، Michael S (سبتمبر 1978). "Evidence that Spontaneous Mitotic Recombination Occurs at the Two-Strand Stage". Proceedings of the National Academy of Sciences of the USA. ج. 75 ع. 9: 4436–4440. DOI:10.1073/pnas.75.9.4436.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ Lee، Phoebe S.؛ Greenwell، Patricia W.؛ Dominska، Margaret؛ Gawel، Malgorzata؛ Hamilton، Monica؛ Petes، Thomas D. (2009). "A Fine-Structure Map of Spontaneous Mitotic Crossovers in the Yeast Saccharomyces cerevisiae". PLoS Genet. ج. 5 ع. 3: e1000410. DOI:10.1371/journal.pgen.1000410. PMID:19282969.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ LaFave، MC؛ J Sekelsky (2009). "Mitotic Recombination: Why? When? How? Where?". PLoS Genet. ج. 5 ع. 3: e1000411. DOI:10.1371/journal.pgen.1000411.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ Haynes, R.H. & Kunz, B.A. (1981). DNA repair and mutagenesis in yeast. In: Strathern, J; Jones, E; Broach J. editors. The Molecular Biology of the Yeast Saccharomyces. Life Cycle and Inheritance. Cold Spring Harbor, N.Y., Cold Spring Harbor Laboratory, 371-414.
- ^ "The RAD52 gene is required for homothallic interconversion of mating types and spontaneous mitotic recombination in yeast". Proc. Natl. Acad. Sci. U.S.A. ج. 77 ع. 1: 503–7. 1980. DOI:10.1073/pnas.77.1.503. PMID:6987653.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ "The Role of Radiation (rad) Genes in Meiotic Recombination in Yeast". Genetics. ج. 94 ع. 1: 51–68. 1980. PMID:17248996.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ Helleday، T. "Double-Strand Break Repair via Double Holliday Junctions (Szostak Model)". Animation. MIT. مؤرشف من الأصل في 2018-10-15.
- ^ Helleday، Thomas (27 نوفمبر 2003). "Pathways for mitotic homologous recombination in mammalian cells" (PDF). Mutation Research. ج. 532 ع. 1–2: 103–115. DOI:10.1016/j.mrfmmm.2003.08.013. مؤرشف من الأصل (PDF) في 2014-05-24. اطلع عليه بتاريخ 2012-12-26.
- ^ Luo، Guangbin؛ وآخرون (2000). "Cancer predisposition caused by elevated mitotic recombination in Bloom mice". Nature Genetics. ج. 26: 424–429. DOI:10.1038/82548. PMID:11101838.
- ^ Xu، T؛ GM Rubin (أبريل 1993). "Analysis of genetic mosaics in developing and adult Drosophila tissues". Development. ج. 117 ع. 4: 1223–12237.
- Griffiths et al. 1999. Modern Genetic Analysis. W. H. Freeman and Company.