|
تضامنًا مع حق الشعب الفلسطيني |
سائل خارج خلوي
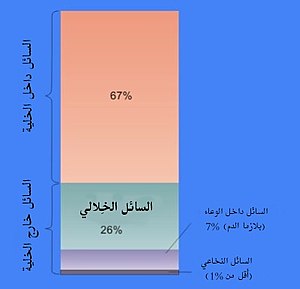
السائل خارج الخلوي (بالإنجليزية: Extracellular fluid) أو السائل البَرَّانِي[1] أو حجم السائل خارج الخلوي (بالإنجليزية: extracellular fluid volume) هو مجموع السوائل المتواجدة خارج الخلايا في أي كائن متعدد الخلايا. يبلغ إجمالي ماء الجسم لدى البالغين الأصحاء حوالي 60% (بين 45 إلى 75%) من وزن الجسم الكلي، وتكون النسبة لدى النساء والأفراد السِّمان عادة أقل من نظيرتها لدى الرجال.[2] يشكل السائل خارج الخلوي حوالي ثلث مياه الجسم ويشكل السائل الجواني داخل الخلايا الثُلثين المتبقيين.[3] المكون الرئيسي للسائل خارج الخلوي هو السائل الخلالي الذي يحيط بالخلايا.
السائل خارج الخلوي هو البيئة الداخلية لجميع الحيوانات متعددة الخلايا، وتعتبر بلازما الدم لدى الحيوانات التي تمتلك نظام دورة دموية جزءا من السائل خارج الخلوي.[4] تشكل بلازما الدم والسائل الخلالي حوالي 97% من السائل خارج الخلوي. ويشكل اللمف نسبة صغيرة من السائل الخلالي.[5] والنسبة المتبقية (حوالي 2.5%) هي سائل عابر للخلايا. يمكن اعتبار أن السائل خارج الخلوي يتكون من نظامين: البلازما واللمف كنظام توصيل، والسائل الخلالي كنظامٍ لتبادل الماء والمذاب (المغذيات والفضلات) مع الخلايا.[6]
يشكل السائل خارج الخلوي -السائل الخلالي بشكل أخص- البيئة الداخلية للجسم التي تسبح فيها جميع خلايا الجسم، وهو أساسي لتقوم بوظائفها الطبيعية. وتتم صيانته عبر عدة آليات استتباب بالاعتماد على الارتجاع السلبي. ينظِّم الاستتباب: الأس الهيدروجيني، الصوديوم، البوتاسيوم وتراكيز الكالسيوم في السائل خارج الخلوي بالإضافة إلى أمور أخرى. مستويات حجم مياه الجسم، غلوكوز الدم، الأكسجين، وثنائي أكسيد الكربون تتم موازنتها بإحكام كذلك.
حجم السائل خارج الخلوي لدى شاب بالغ يزن 70 كلغ هو 20% من وزن الجسم أي حوالي 14 لتر، 11 لتر هي سائل خلالي واللترات الثلاث المتبقية هي بلازما.[7]
المكونات
يتكون السائل خارج الخلوي من مكونين رئيسيين: السائل الخلالي ويسمى كذلك السائل النسيجي ويحيط بخلايا الجسم، وسائل داخل الأوعية الخاصة بجهاز الدوران ويسمى بلازما الدم. النسبة المتبقية الصغيرة من السائل خارج الخلوي تتمثل في السائل العابر للخلايا. عادة ما يُطلق على هذه المكونات أحياز السائل، حجم السائل خارج الخلوي لدى شاب بالغ يزن 70 كلغ هو 20% من وزن الجسم أي حوالي 14 لترا.
السائل الخلالي
السائل الخلالي أو السائل النسيجي (بالإنجليزية: tissue fluid) هو السائل المتواجد بين الأوعية الدموية والخلايا،[8] ويحتوي على المغذيات التي يحصل عليها من الشعيرات الدموية بواسطة الانتشار كما يحتوي على الفضلات التي طرحتها الخلايا نتيجة عملية الأيض.[9] إحدى عشر لترا من السائل خارج الخلوي هي سائل خلالي واللترات الثلاث المتبقية هي بلازما.[7] البلازما والسائل الخلالي متماثلان جدا لأنهما يتبادلان الماء والآيونات والمذابات الصغيرة باستمرار عبر جدران الأوعية الدموية من خلال المسامات والشقوق الشعيرية.
يتكون السائل الخلالي من مذيب مائي يحتوي على السكريات، الأملاح، الأحماض الدهنية، الأحماض الأمينية، العوامل المرافقة، الهرمونات، النواقل العصبية، خلايا الدم البيضاء وفضلات الخلايا المطروحة. يشكل هذا المحلول حوالي 26% من الماء في جسم الإنسان. يعتمد تركيب السائل الخلالي على التبادلات بين الخلايا في النسيج البيولوجي والدم.[10] وهذا يعني أن السائل النسيجي يحتوي على مكونات مختلفة باختلاف الأنسجة التي يتواجد فيها في مختلف مناطق الجسم.
لا تحتوي البلازما التي تتدفق من خلال الشعيرات الدموية إلى السائل الخلالي على الخلايا الحمراء أو الصفائح الدموية لأنها كبيرة الحجم ولا يمكنها المرور، لكنها تحتوي على بعض الخلايا البيضاء لمساعدة الجهاز المناعي.
حين يتجمع السائل خارج الخلوي في أوعية صغيرة (شعيرات ليمفاوية) يُعتبر أنه لمف، وتسمى الأوعية التي تعيد نقله إلى الدم بالأوعية اللمفية. يُعيد الجهاز اللمفي البروتيناتَ ويصل السائل الخلالي بجهاز الدورة الدموية. يختلف التركيب الأيوني للسائل الخلالي نتيجة تأثير غيبس-دونان، ويسبب ذلك اختلافا طفيفا في تراكيز الكاتيونات والأنيونات بين حيزي السائل.
السائل العابر للخلايا
يتشكل السائل العابر للخلايا من وظائف النقل الخلوية، وهو أصغر مكونات السائل خارج الخلوي. هذه السوائل محتواة داخل فراغات باطنية طلائية. من الأمثلة على هذا السائل: السائل الدماغي الشوكي، الخلط المائي في العين، السائل المصلي في الأغشية المصلية التي تبطن تجاويف الجسم. اللمف المحيطي واللمف الداخلي في الأذن الداخلية، والسائل الزلالي.[2][11] تختلف مكونات السائل العابر للخلايا بشكل كبير بسبب الأماكن المختلفة التي يتواجد فيها. من الكهارل الموجودة في السائل العابر للخلايا: أيونات الصوديوم، أيونات الكلوريد، وأيونات البيكربونات.
الوظيفة


يوفر السائل خارج الخلوي وسطا لتبادل المواد بينه وبين الخلايا، ويمكن أن يحدث ذلك عبر إذابة أو خلط أو نقل هذه المواد في وسط السائل.[12] تشمل المواد الموجودة في السائل خارج الخلوي غازات مذابة، مغذيات، وكهارل وكلها ضرورية للمحافظة على الحياة.[13] ويحتوي كذلك على المواد المفرزة من الخلية على هيئة سائلة، والتي سرعان ما تلتحم وتتكتل إلى ألياف (مثل: الكولاجين، النسيج الضام الشبكي، والليف المرن [English]) أو تترسب إلى هيئة صلبة أو نصف صلبة (مثل: البروتيوغليكان الذي هو أحد مكونات الغضروف، ومكونات العظم). يظهر بأن هذه المواد وغيرها -خاصة بالارتباط مع البروتيوغليكانات- تقوم بتشكيل المطرس خارج الخلوي أو مادة «الحشو» بين الخلايا في مختلف أنحاء الجسم.[14] تظهر هذه المواد في الفراغ خارج الخلوي لذلك هي جميعا سابحة أو مغمورة في السائل خارج الخلوي دون أن تكون جزءا منه.
الأكسجة
أحد الأدوار الرئيسية للسائل خارج الخلوي هو تسهيل نقل جزيئات الأكسجين من الدم إلى خلايا النسيج وثنائي أكسيد الكربون CO2 الذي تنتجه متقدرات الخلية وإعادته إلى الدم. بما أن ثنائي أكسيد الكربون قابل للذوبان في الماء 20 مرة أكثر من الأكسجين فإن بإمكانه الانتشار بسهولة نسبية في المحلول السائل بين الخلايا والشعيرات الدموية.[15]
لكن جزيئات الأكسجين الكارهة للماء تملك قابلية ذوبان ضعيفة في الماء وتفضل بُنى الليبيد البلورية الكارهة للماء.[16][17] ونتيجة لذلك يمكن للبروتينات الليبيدية البلازمية حمل جزيئات الأكسجين O2 بكمية أكبر من الوسط المحلولي المجاور.[18][19]
إذا كان الهيموغلوبين لدى حقيقيات النوى هو الناقل الأساسي للأكسجين في الدم، فإن البروتينات الليبيدية البلازمية يمكن أن تكون الناقل الوحيد له في السائل خارج الخلوي.
تنخفض قدرة نقل البروتينات الليبيدية للأكسجين OCCL مع التقدم في العمر أو حدوث الالتهابات، وينتج عن ذلك تغيرات في وظائف السائل خارج الخلوي وانخفاض في كمية الأكسجين في الأنسجة ويساهم ذلك في تطور نقص تأكسج الأنسجة. تحدث هذه التغيرات في البروتينات الليبيدية بواسطة ضرر تأكسدي أو التهابي.[20]
التنظيم

تستقر البيئة الداخلية للسائل خارج الخلوي عبر عملية الاستتباب، حيث تعمل آليات استتبابية معقدة على تنظيم وإبقاء مكوناته متوازنة. تنظم الخلايا الفردية تركيبها الداخلي كذلك عبر آليات متنوعة.[21]
يوجد فارق كبير بين تراكيز أيونات الصوديوم والبوتاسيوم خارج وداخل الخلية، فتركيز أيونات الصوديوم مرتفع إلى حد كبير في السائل خارج الخلوي عن نظيره في السائل داخل الخلوي.[22] والعكس صحيح بالنسبة لتركيز أيونات البوتاسيوم فهو مرتفع داخل الخلية ومنخفض خارجها. تجعل هذه الفروقات جميع الأغشية الخلوية مشحونة كهربائيا بشحنة موجبة خارج الخلايا وشحنة سالبة داخلها. حين يكون العصبون في حالة راحة (لا يقوم بنبض) يُعرف الجهد الغشائي على أنه جهد الراحة وتكون قيمته بين جانبي الغشائي -70 ميلي فولت.[23]
يتشكل هذا الجهد بواسطة مضخات الصوديوم-بوتاسيوم الموجودة على الغشاء الخلوي والتي تضخ أيونات الصوديوم خارج الخلية إلى السائل خارج الخلوي وفي المقابل تدخل أيونات البوتاسيوم منه إلى الخلية. الحفاظ على هذا الفرق في تراكيز الأيونات بين داخل وخارج الخلية أمر حاسم لإبقاء أحجام الخلية الطبيعية مستقرة وكذلك يُمكِّن بعض الخلايا من توليد جهود الفعل.[24]
في أنواع عدة من الخلايا يمكن لقنوات الأيون المبوبة بالفولتية على سطح الخلية أن تنفتح لعدة ميكروثواني في كل مرة، وهذا يسمح بتدفق موجز لأيونات الصوديوم إلى داخل الخلية (يُحدثه تدرج تركيز أيونات الصوديوم الموجود بين داخل وخارج الخلية)، وهذا يتسبب في زوال قطبية الغشاء الخلوي مؤقتا (فقدانه للشحنات الكهربائية) ويشكل أساس حدوث جهود الفعل.
تلعب قنوات الصوديوم في السائل خارج الخلوي دورا مهما في حركة الماء من حيز جسمي إلى آخر. حين تُفرز الدموع أو يتشكل اللعاب فإنه يتم ضخ أيونات الصوديوم من السائل خارج الخلوي إلى القنوات التي تشكلت وتجمعت فيها هذه السوائل. المحتوى المائي لهذه السوائل ينتج من حقيقة أن الماء يتبع أيونات الصوديوم (والأنيونات المرافقة لها) أسموزيا.[25][26] نفس المبدأ ينطبق على تشكل العديد من سوائل الجسم الأخرى.
لدى أيونات الكالسيوم ميول كبير للارتباط بالبروتينات،[27] وهذا الارتباط يُغير توزيع الشحنات الكهربائية في البروتين مما يؤدي إلى تغيير بنيتة الثالثية.[28][29] تعتمد البنية الطبيعية ووظيفة العديد من البروتينات خارج الخلوية وكذلك الجزء خارج الخلوي من البروتينات الغشائية على تراكيز دقيقة جدا لأيونات كالسيوم في السائل خارج الخلوي. من البروتينات الحساسة بشكل خاص لتغيُّر تركيز أيونات الكالسيوم في السائل خارج الخلوي: العديد من بروتينات تجلط الدم في بلازما الدم، والتي تفقد وظيفتها في غياب أيونات الكالسيوم، لكنها تصبح نشيطة بالكامل عند إضافة التركيز الصحيح من أملاح الكالسيوم.[22][27] تملك قنوات أيون الصوديوم المبوبة بالفولتية المتواجدة على الأغشية الخلوية للعصبونات والعضلات حساسية أكبر للتغيرات في تراكيز أيونات الكالسيوم بالسائل خارج الخلوي.[30] وتسبب أيّ انخفاضات صغيرة نسبيا في مستويات الكالسيوم المتأين البلازمي (نقص كالسيوم الدم) تسريب هذه القنوات للصديوم داخل خلايا أو محوارت العصب مما يجعلها فائقة الاستثارة، وتتسبب في تقلصات عضلية عفوية (التكزز) وتشوش الحس (الشعور بوخز الدبابيس والإبر) في الأطراف وحول الفم.[28][30][31] حين يرتفع تركيز أيونات الكالسيوم في البلازما فوق المستوى الطبيعي (فرط كالسيوم الدم) فإن المزيد من الكالسيوم يرتبط بقنوات الصوديوم هذه ويحدث تأثيرا معاكسا وهو ما يسبب الخمول، ضعف العضلات، فقدان الشهية، الإمساك وعواطف متغيرة.[31][32]
تتأثر البنية الثالثية للبروتينات كذلك بالأس الهيدروجيني للمحلول المغمورة فيه، ويؤثر الأس الهيدروجيني الخاص بالسائل خارج الخلوي على نسبة الكالسيوم -من الكمية الكلية له- التي تظهر في البلازما على هيئة حرة أو متأينة مقارنة بالنسبة التي تكون مرتبطة بالبروتين أو أيونات الفوسفات. وأيُّ تغيُّر في الأس الهيدروجيني للسائل خارج الخلوي يُغير تركيز الكالسيوم فيه. وبما أن الأس الهيدروجيني للسائل خارج الخلوي مرتبط مباشرة بالضغط الجزئي لثنائي أكسيد الكربون فيه، فإن فرط التنفس الذي يخفض الضغط الجزئي لثنائي أكسيد الكربون في السائل، تنتج عنه أعراض لا يمكن تمييزها تقريبا عن أعراض انخفاض تركيز أيونات الكالسيوم في البلازما.[28]
يقوم جهاز الدوران «بتحريك وخلط» السائل خارج الخلوي بالاستمرار، وهو ما يضمن أن البيئة المائية المغمورة فيها خلايا الجسم متماثلة تقريبا عبر سائر الجسم. ويعني ذلك أن المغذيات يمكن أن تُفرز في السائل خارج الخلوي في منطقة معينة ( البطن، الكبد، أو الخلايا الدهنية) ثم تتوزع بانتظام خلال حوالي دقيقة عبر سائر الجسد. الهرمونات أيضا تتوزع بانتظام وبسرعة إلى كل الخلايا في الجسم بغض النظر عن مكان إفرازها في الدم. الأكسجين المأخوذ بواسطة الرئتين من هواء الحويصلة يُوزَّع باتنظام كذلك بالضغط الجزئي الصحيح بين كل خلايا الجسم. تنتشر الفضلات الناتجة بانتظام كذلك على طول السائل خارج الخلوي، وتُزال منه في نقاط أو أعضاء معينة، وهو ما يضمن عدم تراكم مركبات غير مرغوب بها في منطقة معينة أو تجاوز الحد المطلوب للمواد الضرورية في منطقة ما (مثل أيونات الصوديوم أو أي مكونات أخرى للسائل خارج الخلوي). الاستثناء الوحيد لهذه القاعدة العامة هو البلازما في الأوردة حيث تكون تراكيز المواد المنحلة في كل وريد مفرد مختلفة بدرجة معينة عن تلك الموجودة في السائل خارج الخلوي. غير أن هذه البلازما محتواة في أوعية وريدية جدرانها غير نافذة للماء وبالتالي لا تؤثر على السائل الخلالي الذي تعيش فيه خلايا الجسد. حين يختلط الدم من جميع أوردة الجسد في القلب والرئتين فإن تراكيز مختلف المكونات تقوم بتحييد بعضها البعض (كمثال يُعادَل الدم الحمضي للعضلات النشطة بواسطة الدم القلوي المنتج استتبابيا بواسطة الكليتين). من الأذين الأيسر وما يليه قدما نحو كل عضو في الجسد، يسترجع السائل خارج الخلوي قيم مكوناته الطبيعية المنظمة استبابيا.
التآثر بين بلازما الدم والسائل الخلالي واللمف


تتآثر بلازما الدم الشريانية والسائل الخلالي واللمف على مستوى الشعيرات الدموية، هذه الأخيرة نفوذة ويمكن للماء التحرك بحرية داخلا وخارجا. يكون ضغط الدم في النهاية الشُرينية للشعيرات الدموية أكبر من الضغط المائي في الأنسجة،[22][33] وبالتالي يتحرك الماء خارج الشعيرات الدموية نحو السائل الخلالي. المسامات التي يمر من خلالها الماء كبيرة بالقدر الذي يسمح للجزيئات الصغيرة (حتى حجم البروتينات الصغيرة مثل الإنسولين) أن تمر بحرية عبر جدار الشعيرة، وهذا يعني أن تراكيزها على جانبي جدار الشعيرة يكون متوازنا وبالتالي لا يكون هنالك تأثيرا أسموزيا (لأن الضغط الأسموزي الذي تُحدثه هذه الجزيئات الصغيرة والأيونات -ويسمى الضغط الأسموزي البلوراني لتمييزه عن التأثير الأسموزي الذي تحدثه الجزيئات الأكبر حجما والتي لا يمكنها عبور جدار الشعيرة الدموية- متماثلٌ على كلا طرفي جدار الشعيرة).[22][33]
يتسبب تحرك الماء وخروجه من الشعيرة الدموية في النهاية الشرينية في زيادة تركيز المواد التي لا يمكنها عبور جدار الشعيرة مع تحرك الدم نحو النهاية الوُريدية للشعيرات الدموية. من أهم المواد التي لا يمكنها عبور جدار الشعيرات هي: ألبيومين المصل، غلوبيولين المصل والفيبرينوجين، وبسبب وفرتها الجزيئية في البلازما - وبشكل أخص ألبومين المصل- فهي مسؤولة على ما يسمى بالضغط الجرمي أو الضغط الأسموزي الغرواني والذي يعاود سحب الماء من السائل الخلالي إلى الشعيرات الدموية خاصة عند النهاية الوريدية.[33]
التأثير الصافي لكل هذه العمليات هو تحرك الماء خارج الشعيرات ثم عودته إليها، بينما تتوازن المواد البلورانية في الشعيرات والسائل الخلالي. بما أن سائل الشعيرات يتجدد بسرعة وباستمرار بواسطة تدفق الدم، فإن تركيبه يسود على تركيز التوازن الذي يحققه سرير الشعيرات. وهذا يضمن بأن البيئة المائية لخلايا الجسم قريبة دائما من بيئتها المثالية (التي يحددها الاستتباب).
نسبة صغيرة من السائل الذي يتسرب من الشعيرات لا يعود إليها بواسطة القوى الأسموزية الغروانية. وتبلغ هذه الكمية بين 2-4 لترات في مجمل الجسم كل يوم. يُجمع هذا الماء بواسطة الشعيرات اللمفية في الجهاز اللمفي ويصب بالنهاية في وريد تحت الترقوة الأيسر أين يختلط مع الدم القادم من الذراع الأيسر والماضي في طريقه إلى القلب.[22] يتدفق اللمف داخل الشعيرات اللمفية إلى العقد اللمفاوية أين تزال منه البكتيريا والبقايا النسيجية، وفي نفس الوقت تضاف إليه عدة أنواع من الخلايا البيضاء (بشكل رئيسي الخلايا اللمفاوية). فضلا عن ذلك، يحتوي اللمف الذي يُصرَف من الأمعاء الدقيقة على قطيرات دهنية تسمى كيلومكرونات بعد تناول وجبة دهنية.[27] يسمى هذا اللمف بالكيلوس وله مظهر يشبه الحليب، وتسمى الأوعية اللمفية التي تحتويه في الأمعاء الدقيقة بالأوعية اللبنية [English] نتيجة لمظهره الحليبي.[34]
المكونات الكهرلية
يلخص الجدول التالي المكونات الرئيسية للسائل خارج الخلوي البشري وخصائصها الفيزيائية الرئيسية، وقيمها ونطاقاتها الطبيعية، والحدود الدنيا والقصوى التي يمكن أن يتحملها الشخص لفترة قصيرة من الزمن دون الموت. القيم الخارجة عن هذه الحدود عادة ما تكون نتيجة المرض.[35][36]
| المكون | القيمة الطبيعية | المجال الطبيعي | الحدود غير المميتة
تقريبيا |
الوحدات |
|---|---|---|---|---|
| الأكسجين | 40 | 35-45 | 10-1000 | ملم زئبقي (mm Hg) |
| ثنائي أكسيد الكربون | 40 | 35-45 | 5-80 | ملم زئبقي |
| أيون الصوديوم (Na+) | 142 | 138-146 | 115-175 | ميلي مول/ل (mmol/L) |
| أيون البوتاسيوم (K+) | 4.2 | 3.8-5.0 | 1.5-9.0 | ميلي مول/ل |
| أيون الكالسيوم (Ca2+) | 1.2 | 1.0-1.4 | 1.0-1.4 | ميلي مول/ل |
| أنيون الكلوريد (Cl-) | 108 | 103-112 | 70-130 | ميلي مول/ل |
| أنيون البيكربونات (HCO3-) | 28 | 24-32 | 8-45 | ميلي مول/ل |
| أنيون الفوسفات (HPO42−) | 1.5 | 0.8-1.4 | ميلي مول/ل | |
| الجلوكوز | 85 | 75-95 | 20-1500 | ملغ/دسل (mg/dl) |
| حرارة الجسم | 37.0 | 36.5–37.5 | 18.3-43.3 | م° (°C) |
| الحموضة والقاعدية | 7.4 | 7.3-7.5 | 6.9-8.0 | pH |
انظر أيضًا
المراجع
- ^ المعجم الطبي الموحد
- ^ أ ب "Fluid Physiology: 2.1 Fluid Compartments". www.anaesthesiamcq.com. مؤرشف من الأصل في 2021-10-15. اطلع عليه بتاريخ 2019-11-28.
- ^ Tortora G (1987). Principles of anatomy and physiology (ط. 5th). New York, NY: Harper and Row. ص. 693. ISBN:978-0-06-350729-6. مؤرشف من الأصل في 2021-07-16.
- ^ Hillis D (2012). Principles of life. Sunderland, MA: Sinauer Associates. ص. 589. ISBN:978-1-4292-5721-3.
- ^ Pocock G، Richards CD (2006). Human physiology : the basis of medicine (ط. 3rd). Oxford: Oxford University Press. ص. 548. ISBN:978-0-19-856878-0. مؤرشف من الأصل في 2022-06-30.
- ^ Canavan A، Arant BS (أكتوبر 2009). "Diagnosis and management of dehydration in children" (PDF). American Family Physician. ج. 80 ع. 7: 692–6. PMID:19817339. مؤرشف من الأصل (PDF) في 2020-08-06.
- ^ أ ب Hall J (2011). Guyton and Hall textbook of medical physiology (ط. 12th). Philadelphia, Pa.: Saunders/Elsevier. ص. 286–287. ISBN:978-1-4160-4574-8.
- ^ Wiig، Helge؛ Swartz، Melody A. (2012). "Interstitial Fluid and Lymph Formation and Transport: Physiological Regulation and Roles in Inflammation and Cancer". Physiological Reviews. American Physiological Society. ج. 92 ع. 3: 1005–1060. DOI:10.1152/physrev.00037.2011. ISSN:0031-9333. PMID:22811424. S2CID:11394172.
- ^ "Interstitial Fluid - What is the Role of Interstitial Fluid". Diabetes Community, Support, Education, Recipes & Resources. 22 يوليو 2019. مؤرشف من الأصل في 2021-08-21. اطلع عليه بتاريخ 2019-07-22.
- ^ Widmaier, Eric P., Hershel Raff, Kevin T. Strang, and Arthur J. Vander. "Body Fluid Compartments." Vander's Human Physiology: The Mechanisms of Body Function. 14th ed. New York: McGraw-Hill, 2016. 400-401. Print.
- ^ Constanzo LS (2014). Physiology (ط. 5th). Elsevier Saunders. ص. 264. ISBN:9781455708475.
- ^ Tortora G (1987). Principles of anatomy and physiology (ط. 5th ed. Harper international). New York: Harper & Row. ص. 61–62. ISBN:978-0-06-046669-5. مؤرشف من الأصل في 2021-10-21.
- ^ Tortora G (1987). Principles of anatomy and physiology (ط. 5th ed. Harper international). New York: Harper & Row. ص. 17. ISBN:978-0-06-046669-5. مؤرشف من الأصل في 2021-10-21.
- ^ Voet D، Voet J، Pratt C (2016). Fundamentals of Biochemistry: Life at the Molecular Level. Hoboken, New Jersey: John Wiley & Sons. ص. 235. ISBN:978-1-118-91840-1.
- ^ Arthurs, G.J.; Sudhakar, M (Dec 2005). "Carbon dioxide transport". Continuing Education in Anaesthesia, Critical Care & Pain (بEnglish). 5 (6): 207–210. DOI:10.1093/bjaceaccp/mki050. Archived from the original on 2018-06-12.
- ^ Bačič, G.; Walczak, T.; Demsar, F.; Swartz, H. M. (Oct 1988). "Electron spin resonance imaging of tissues with lipid-rich areas". Magnetic Resonance in Medicine (بEnglish). 8 (2): 209–219. DOI:10.1002/mrm.1910080211. PMID:2850439. S2CID:41810978. Archived from the original on 2018-06-05.
- ^ Windrem, David A.; Plachy, William Z. (Aug 1980). "The diffusion-solubility of oxygen in lipid bilayers". Biochimica et Biophysica Acta (BBA) - Biomembranes (بEnglish). 600 (3): 655–665. DOI:10.1016/0005-2736(80)90469-1. PMID:6250601. Archived from the original on 2018-06-27.
- ^ Petyaev, I. M.; Vuylsteke, A.; Bethune, D. W.; Hunt, J. V. (1 Jan 1998). "Plasma Oxygen during Cardiopulmonary Bypass: A Comparison of Blood Oxygen Levels with Oxygen Present in Plasma Lipid". Clinical Science (بEnglish). 94 (1): 35–41. DOI:10.1042/cs0940035. ISSN:0143-5221. PMID:9505864. Archived from the original on 2023-02-10.
- ^ Jackson، M. J. (1 يناير 1998). "Plasma Oxygen during Cardiopulmonary Bypass". Clinical Science. ج. 94 ع. 1: 1. DOI:10.1042/cs0940001. ISSN:0143-5221. PMID:9505858. مؤرشف من الأصل في 2022-04-07.
- ^ Petyaev, Ivan M.; Hunt, James V. (Apr 1997). "Micellar acceleration of oxygen-dependent reactions and its potential use in the study of human low density lipoprotein". Biochimica et Biophysica Acta (BBA) - Lipids and Lipid Metabolism (بEnglish). 1345 (3): 293–305. DOI:10.1016/S0005-2760(97)00005-2. PMID:9150249. Archived from the original on 2021-12-01.
- ^ Pocock G، Richards CD (2006). Human physiology : the basis of medicine (ط. 3rd). Oxford: Oxford University Press. ص. 3. ISBN:978-0-19-856878-0. مؤرشف من الأصل في 2022-06-30.
- ^ أ ب ت ث ج Tortora G (1987). Principles of anatomy and physiology (ط. 5th). New York: Harper & Row, International. ص. 40, 49–50, 61, 268–274, 449–453, 456, 494–496, 530–552, 693–700. ISBN:978-0-06-046669-5. مؤرشف من الأصل في 2021-10-21.
- ^ Tortora G (1987). Principles of Anatomy and Physiology. ص. 269. ISBN:978-0-06-046669-5. مؤرشف من الأصل في 2021-10-21.
- ^ Tortora G (2011). Principles of anatomy and physiology (ط. 13th). Hoboken, N.J.: Wiley. ص. 73–74. ISBN:978-0-470-64608-3.
- ^ Tortora G، Anagnostakos N (1987). Principles of anatomy and physiology (ط. 5th). New York, NY: Harper and Row. ص. 34, 621, 693–694. ISBN:978-0-06-350729-6. مؤرشف من الأصل في 2021-07-16.
- ^ "Data". pcwww.liv.ac.uk. مؤرشف من الأصل في 2017-11-10.
- ^ أ ب ت Stryer L (1995). Biochemistry (ط. Fourth). New York: W.H. Freeman and Company. ص. 255–256, 347–348, 697–698. ISBN:0-7167-2009-4.
- ^ أ ب ت Macefield G، Burke D (فبراير 1991). "Paraesthesiae and tetany induced by voluntary hyperventilation. Increased excitability of human cutaneous and motor axons". Brain. 114 ( Pt 1B) ع. 1: 527–40. DOI:10.1093/brain/114.1.527. PMID:2004255.
- ^ Stryer L (1995). Biochemistry (ط. Fourth). New York: W.H. Freeman and Company. ص. 347, 348. ISBN:978-0-7167-2009-6.
- ^ أ ب Armstrong CM، Cota G (مارس 1999). "Calcium block of Na+ channels and its effect on closing rate". Proceedings of the National Academy of Sciences of the United States of America. ج. 96 ع. 7: 4154–7. Bibcode:1999PNAS...96.4154A. DOI:10.1073/pnas.96.7.4154. PMC:22436. PMID:10097179.
- ^ أ ب Harrison TR (1947). Principles of Internal Medicine (ط. third). New York: McGraw-Hill Book Company. ص. 170, 571–579.
- ^ Waters M (2009). "Hypercalcemia". InnovAiT. ج. 2 ع. 12: 698–701. DOI:10.1093/innovait/inp143.
- ^ أ ب ت Hall J (2011). Guyton and Hall textbook of medical physiology (ط. 12th). Philadelphia, Pa.: Saunders/Elsevier. ص. 177–181. ISBN:978-1-4160-4574-8.
- ^ Williams PL، Warwick R، Dyson M، Bannister LH (1989). Gray's Anatomy (ط. Thirty-seventh). Edinburgh: Churchill Livingstone. ص. 821. ISBN:0443-041776.
- ^ Guyton، Arthur C. (2001). Tratado de fisiología médica (ط. 10. ed. en español). McGraw-Hill Interamericana. ص. 7. ISBN:970-10-3599-2. OCLC:49608187. مؤرشف من الأصل في 2021-10-07.
- ^ "Blood – Inorganic substances". in: Scientific Tables (ط. Seventh). Basle, Switzerland: CIBA-GEIGY Ltd. 1970. ص. 561–568.
وصلات خارجية
- extracellular+fluid في قاموس إي ميديسين
| سائل خارج خلوي في المشاريع الشقيقة: | |