|
تضامنًا مع حق الشعب الفلسطيني |
هربس نطاقي
| الهِربِس النُطاقي | |
|---|---|
| Shingles | |
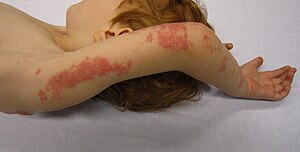
بثرات الهِربِس النُطاقي على العُنق والكتفين
| |
| معلومات عامة | |
| الاختصاص | طب الجلد |
| الأسباب | |
| الأسباب | فيروس جدري الماء النطاقي[1] |
| عوامل الخطر | التقدم في العُمر، والمناعة الضعيفة، والإصابة بجدري الماء قبل عُمر 18 شهرًا.[1] |
| المظهر السريري | |
| الأعراض | طُفحٌ شَريطيٌ مؤلمٌ[1] |
| المدة | 2–4 أسابيع[2] |
| المضاعفات | ألم عصبي تال للهربس[1] |
| الإدارة | |
| الوقاية | لقاح الهربس النطاقي[1] |
| التشخيص | يعتمدُ على الأعراض[3] |
| أدوية | |
| حالات مشابهة | الهربس البسيط، الذبحة الصدرية، لسعات الحشرات[4] |
| الوبائيات | |
| انتشار المرض | 33% (في مرحلةٍ ما)[1] |
| الوفيات | 6,400 (لديهم جدري الماء)[5] |
| تعديل مصدري - تعديل | |
الهِربِس النُطاقي(1) هو مرضٌ فيروسيٌّ يظهرُ فيه طفحٌ جلديٌّ مؤلمٌ مع بثراتٍ في منطقةٍ مُعينة.[2][6] عادةً ما يحدثُ الطفحُ على شكلِ شريطٍ عريضٍ واحدٍ إما على الجانب الأيسر أو الأيمن من الجسم أو الوجه،[1] كما قد يحدثُ نخزٌ أو ألمٌ موضعيٌّ في المنطقة المتأثرة قبل يومين إلى أربعة أيامٍ من ظهورِ الطفح.[1][7] قد تظهر لدى البعض أعراضٌ أُخرى مثل الحمى والصداع والشعور بالتعب.[1][8] عادةً ما يُشفى الطفح «بالعلاج السريع» خلال أسبوعين إلى أربعة أسابيع.[2] فالعلاج السريع من الطبيب مهم جدا لمنع الانتشار في الجسم. بعد العلاج تكمن بعض الفيروسات في بعض التفرعات العصبية المصابة، ولكنها تنشط ثانيا إذا ضعف الجسم وانخفضت مناعته. وقد يحدثُ لدى البعض ألمٌ عصبيٌ مُستمر، والذي قد يستمرُّ لأشهرٍ أو سنواتٍ، وتُسمى هذه الحالة بالألم العصبي التالِ للهربس (PHN).[1] قد يكونُ انتشار الطفح واسعًا لدى الأشخاص ضعيفي المناعة.[1] إذا وصل الطفحُ إلى العين، فإنهُ قد يؤدي إلى فقدان البصر.[2][9]
يحدثُ الهربس النطاقي بسبب تنشيط فيروس جدري الماء النطاقي في جسم الإنسان،[1] وتؤدي العدوى الأولية بهذا الفيروس إلى حدوث مرض جدري الماء.[1] بعد الشفاء من جدري الماء، يبقى الفيروس كامنًا في العصبونات.[1] ثم ينتقل عند تنشيطهِ من جسم العصبون إلى النهايات العصبية على الجلد، مُؤديًا لحدوث البثرات.[7] يوجدُ عددٌ من عوامل الخطر المؤدية لتنشيط الفيروس، وتشمل التقدم في العُمر وضعف الوظيفة المناعية والإصابة بجدري الماء قبل عُمر 18 شهرًا.[1] آلية بقاء الفيروس في الجسم أو كيفية تنشيطه لاحقًا غيرُ مفهومةٍ جيدًا.[1] قد يؤدي التَعرضُ إلى الفيروس في البثرات إلى حدوث جدري الماء في الأشخاص الذين لم يُصابوا به سابقًا، ولكنه لن يؤدي مباشرةً إلى حدوث الهربس النطاقي.[10] يعتمد تشخيص الهربس النطاقي أساسًا على العلامات والأعراض الظاهرة على الشخص.[3] يختلفُ فيروس جدري الماء النطاقي عن فيروس الهربس البسيط، ولكنهما ينتميان لنفس عائلة الفيروسات.[11]
يُقلل لقاح الهربس النطاقي من خطرِ حدوث الهربس النطاقي بحوالي 50% إلى 90%، وذلك اعتمادًا على اللقاح المُستعمل.[1][12] كما يُقلل أيضًا من معدلات حدوث الألم العصبي التالِ للهربس، وإذا حدث الهربس، فإنهُ يقلل من شدته.[1] إذا ظهر الهربس النطاقي، فإنَّمضادات الفيروسات مثل الآسيكلوفير يُمكنها أن تُقلل من شدة المرض ومدته، وذلك إذا بدأ استعمالها خلال الساعات 72 الأولى من ظهور الطفح.[3] لم تُظهر الأدلة أي تأثيرٍ هام لمضادات الفيروسات أو الستيرويدات على معدلات حدوث الألم العصبي التالِ للهربس.[13][14] قد يُستعمل الباراسيتامول أو الأدوية اللاستيرويدة المضادة للالتهاب أو أشباه الأفيونيات مع الألم الحاد.[3]
يُقدر بأنَّ حوالي ثلث الناس يُصابون بالهربس النطاقي في مرحلةٍ ما خلال حياتهم.[1] على الرغم من أنَّ الهربس النطاقي أكثر شيوعًا بين كبار السن، إلا أنهُ قد يصيب الأطفال أيضًا.[11] يتراوح عدد الحالات الجديدة سنويًا من 1.2 إلى 3.4 لكل 1,000 شخص-سنة بين الأفراد السليمين، ويترواح من 3.9 إلى 11.8 لكل 1000 شخص-سنة في الأشخاص الأكبر من 65 عامًا.[8] حوالي نصف الذين يعيشون حتى سن 85 عامًا سوف يتعرضون لإصابةٍ واحدةٍ على الأقل، وأقل من 5% سيواجهون أكثر من إصابة.[1][15] حُدد الهربس النطاقي منذ العصور القديمة.[1]
العلامات والأعراض
يبدأُ الهربس النطاقي بظهور أعراضٍ أولية، تتضمن الصداع والحمى والتوعك، وهذه الأعراض غيرُ خاصةٍ بالهربس النطاقي، وقد تؤدي إلى خطأٍ في التشخيص.[8][16] عادةً ما تُتبع هذه الأعراض بإحساسٍ مؤلمٍ حارق، وحكة، وفرطٍ في الإحساس، أو مذل (نخز أو تنمل).[17] قد يكون الألم طفيفًا أو شديدًا في القطاع الجلدي المُصاب، مع إحساسٍ عادةً ما يُوصف بأنهُ لاسعٌ أو نابضٌ أو نخزٌ أو تنميلٌ، وقد يترافقُ مع ألمٍ مبرحٍ يُشبه الطعنات السريعة.[18]
غالبًا يكونُ الهربس النطاقي غير مؤلمٍ في الأطفال، ولكن من المُحتمل أن يحدثُ لديهم مع التقدم في العمر، كما أنَّ المرض قد يميل ليُصبح أكثر حدةً.[19]
تُتبع الأعراض الأولية بظهور طفحٍ جلديٍ مُميز، والذي يظهر بعد يومٍ إلى يومين في معظم الحالات، ولكن أحيانًا قد يتأخر ظهوره إلى ثلاثة أسابيع. عادةً ما يحدثُ الألم والطفح في الجذع، ولكنه قد يظهر على الوجه أو العينين أو أجزاءٍ أُخرى من الجسم. يبدو الطفح الجلدي في البداية مُشابهًا لأول ظٍهور للشرى، ولكن على عكس الشرى، فإنَّ الهربس النطاقي يُسبب تغيراتٍ جلدية محدودةٌ في القطاع الجلدي المُتأثر، مما يؤدي عادةً إلى وجود شكلٍ مُشابهٍ للشريط أو الحزام، كما يقتصرُ على جانبٍ واحد من الجسم ولا يعبر خط الوسط.[17] يصفُ مُصطلح «النُطاقي اللاهِربسيّ» الشخص الذي يُعاني من جميع أعراض الهربس النطاقي باستثناء الطفح الجلدي المُميز.[20]
يُصبح الطفح فيما بعد حويصليًا، حيث يُكون بثورًا صغيرةً مملوءةً بإفرازاتٍ مصلية، مع استمرار الحُمى والشعور بتوعكٍ عام. في النهاية، تُصبح الحويصلات المؤلمة ضبابيةً أو مُظلمة؛ وذلك لامتلائها بالدم، كما تسقطُ القشور في خلال سبعة إلى عشرة أيام، وعادةً ما تسقط القُشور ويلتئم الجلد، ولكن أحيانًا ونتيجةً لحدوث تثبرٍ شديد، فإنَّ الجلد يبقى متندبًا ولونهُ مُتغير.[17]
| اليوم الأول | اليوم الثاني | اليوم الخامس | اليوم السادس |
|---|---|---|---|

|

|

|

|
الوجه
قد تظهرُ أعراضٌ إضافيةٌ للهربس النطاقي، وذلك اعتمادًا على القطاع الجلدي المُصاب. يُعتبر العصب ثلاثي التوائم العصب الأكثر تأثرًا،[21] ويُعتبر فرعه العيني أكثر الفروع تأثرًا.[22] عندما يتنشطُ الفيروس في هذا الفرع العصبي فإنَّ الحالة تعرف باسم الهربس النطاقي العيني، وقد يتأثر أيضًا جلد الجبهة والجفن العلوي ومحجر العين. يحدث الهربس النطاقي العيني في حوالي 10% إلى 25% من الحالات. قد تحدثُ أعراضٌ أُخرى في بعض الأشخاص، وتتضمن التهاب الملتحمة، والتهاب القرنية، والتهاب العنبية، وشلل العصب البصري الذيقد يُسبب أحيانًا حدوث التهابٍ مزمنٍ في العين وفقدانٍ للبصر وألمٍ موهن.[23]
الهربس النطاقي الأذني (يُعرف أيضًا باسم النوع الثاني من متلازمة رامسي-هانت)، حيثُ يُعتقد بأنهُ يحدث بسبب انتشار الفيروس من العصب الوجهي إلى العصب الدهليزي القوقعي، وتشملُ أعراضهُ فقدان السمع والدوار.[24]
إذا تأثر فرع الفك السفلي وفرع الفك العلوي للعصب ثلاثي التوائم، فإنَّ الهربس النطاقي قد يحدثُ في الفم،[25] حيثُ قد يظهر طفحٌ على الغشاء المخاطي للفك العلوي (عادةً الحنك، وأحيانًا لثة الأسنان العلوية) أو الفك السفلي (اللسان أو لثة الأسنان السفلية).[26] قد يتأثر الفم لوحده أو يترافق مع حدوث طفحٍ جلديٍ على التوزيع الجلدي لنفس فرع العصب ثلاثي التوائم.[25] وكما هو الحال في الهربس النطاقي الجلدي، فإنَّ الآفات تميل للتأثير على جانبٍ واحدٍ فقط، مما يجعله مميزًا عن الحالات الأخرى للبثور في الفم.[26] يظهرُ الهربس النطاقي في الفم بدايةً على شكل بثراتٍ (حويصلاتٍ) غير شفافة (1-4 ملليمتر)،[25] والتي تتحلل سريعًا مخلفةً تقرحاتٍ تلتئمُ خلال 10-14 يومًا.[26] قد يحدث خلطٌ بين الخلط بين الألم الأولي (قبل الطفح الجلدي) وبين ألم الأسنان،[25] مما قد يؤدي أحيانًا لعلاج الأسنان دون أي فائدة.[26] من غير الشائع أن يحدث الألم العصبي التالِ للهربس في حالات الهربس النطافي الفموي.[26] قد تحدثُ مُضاعفاتٌ غير اعتيادية مع الهربس النطاقي داخل الفم والتي لا تُرى في مكانٍ آخر. نظرًا لقرب الأوعية الدموية من الأعصاب، فإنَّ الفيروس قد ينتشر ليؤثر على الأوعية الدموية ويقلل تزويد الدم، مما يؤدي إحيانًا إلى نخر إقفاري.[25] لذلك، نادرًا ما تسبب إصابة الفم مضاعفاتٍ مثل نخر العظم وفقدان الأسنان والتهاب دواعم السن (أمراض اللثة) وتكلس اللب ونخر اللب وآفات قمة الأسنان وتشوهات نمو الأسنان.[21]
الهربس النطاقي المنتشر
قد يحدثُ الهربس النطاقي المنتشر (طفحٌ واسع) في الأشخاص ضعيفي الوظيفة المناعية.[1] يُعرف الهربس النطاقي المنتشر على أنه ظهور أكثر من عشرين آفةٍ جلدية إما على القطاع الجلدي المُصاب أساسًا أو القطاعات الجلدية المُجاورة مباشرةً له. بالإضافة إلى الجلد، قد تتأثر أعضاءٌ أخرى مثل الكبد مُسببةً التهاب كبدي أو الدماغ مُسببةً التهاب الدماغ،[27][28] مما يجعل الحالة مُميتةً.[29]:380
الفيزيولوجيا المرضية

يحدثُ الهربس النطاقي بسبب فيروس جدري الماء النطاقي (VZV)، وهو فيروسٌ ذو حمضٍ نووي ريبوزي منقوص الأكسجين مزدوج السلسلة، ويرتبط مع فيروس الهربس البسيط. يُعتبر الأطفال أكثر الأفراد الذين يُصابون بفيروس جدري الماء النطاقي، حيثُ يُسبب لهم جدري الماء. في النهاية يتعرفُ الجهاز المناعي على الفيروس في مُعظم مواقع تواجده، ولكنه يبقى كامنًا في العُقد المُجاورة للحبل الشوكي (تُسمى عقدة الجذر الظهراني) أو في عقدة العصب الثلاثي التوائم في قاعدة الجمجمة.[30]
يحدثُ الهربس النطاقي فقط في الأشخاص الذين سبقَ أن أُصيبوا بفيروس جدري الماء النطاقي، ولكن على الرغم من هذا إلا أنهُ قد يحدثُ في أي فئةٍ عُمرية، حيثُ أنَّ حوالي نصف الحالات في الولايات المتحدة تحدث في الأشخاص الذين تبلغ أعمارهم 50 عامًا أو أكبر.[31] من النادر تكرار حدوث الهربس النطاقي،[17] ومن النادر جدًا أن يتكرر في شخصٍ واحدٍ أكثر من ثلاث مراتٍ.[30]
تتحول جسيمات الفيروس في عقدةٍ حسيةٍ مُنفردة من دورة المستذيب الكامنة إلى الدورة الحالة النشطة.[32] على عكس فيروس الهربس البسيط، فإن كمون فيروس جدري الماء النطاقي غير مفهومٍ جيدًا، كما أنه لم يكن ممكنًا النجاحُ في استرجاع الفيروس من الخلايا العصبية البشرية عبر زراعة الخلايا. تستمرُ الخلايا المُصابة في صنع البروتينات الخاصة بالفيروس خلال فترة الكمون، مما يعنى أنَّ الفيروس يكون حقًا كامنًا، وذلك على عكس العدوى المزمنة النشطة مُنخفضة المستوى، حيثُ لم يثبت حدوثها في فيروس جدري الماء النطاقي.[33][34] على الرغم من اكتشاف فيروس جدري الماء النطاقي عند تشريح الأنسجة العصبية،[35] إلا أنهُ لا توجد طرقٌ للعثور على الفيروس الكامن في عُقد الأفراد الأحياء.
إذا لم يحدث نقصٌ في المناعة، فإنَّ الجهاز المناعي يُثبط تنشيط الفيروس ويمنعُ تفشي الهربس النطاقي، إلا أنَّ الجهاز المناعي يفشل أحيانًا في ذلك، وهو أُمرٌ غير مفهومٍ جيدًا،[36] ولكن يُرجح بأنَّ الهربس النطاقي يحدث في الأشخاص الذين يعانون من ضعفٍ في جهاز المناعة بسبب الشيخوخة أو العلاج المُثبط للمناعة أو الضغط النفسي أو غيرها من العوامل.[37][38] عند تنشيط الفيروس، فإنهُ يتكاثر في أجسام الخلايا العصبية، وتفصل الفيريونات (الأجسام الفيروسية) من الخلايا وتنقل المحاور العصبية إلى منطقة الجلد المُعصبة بالعقدة المُصابة. يؤدي الفيروس إلى حدوث تقرحاتٍ والتهابٍ موضعيٍ في الجلد، كما يؤدي تفشي الهربس النطاقي إلى حدوث ألمٍ قصير الأمد وآخر طويل الأمد؛ بسبب التهاب الأعصاب المُصابة؛ وذلك بسبب نمو الفيروس بشكلٍ واسع في تلك المناطق.[39]
كما هو الحال في جدري الماء وغيره من أشكال العدوى بالفيروسات الهربسية ألفا، فإنَّ الاتصال المُباشر بطفحٍ جلدي نشطٍ قد يؤدي إلى انتشار الفيروس إلى شخصٍ منقوص المناعة، حيثُ قد يصاب هذا الشخص بجدري الماء، ولكنه لن يصاب مباشرةً بالهربس النطاقي.[17]
نُشرت السلسلة الكاملة للمجموع المورثي (الجينوم) للفيروس في عام 1986.[40]
التشخيص

إذا ظهر الطفح الجلدي، فإنَّ تحديد المرض (إجراء تشخيص تفريقي) يتطلب فقط إجراء فحصٍ بصري؛ وذلك لأنَّ عددًا قليلاً جدًا من الأمراض يُسبب طفحًا بنمطٍ جلدي، ولكن فيروس الهربس البسيط يُسبب أحيانًا طفحًا جلديًا مماثلًا في مثل هذا النمط (الهربس البسيط شبيه النطاق).[41][42] يُساعد اختبار تزانك على تشخيص العدوى الحادة بفيروس الهربس، ولكنه لا يُفرق بين فيروس الهربس البسيط (HSV) وفيروس جدري الماء النطاقي (VZV).[43]
عندما يكون الطفح الجلدي غير موجودٍ (في مرحلةٍ مبكرة أو متأخرة من المرض، أو في حالة النُطاقي اللاهِربسيّ)، فإنهُ يصعُب تشخيص الهربس النطاقي، حيثُ أنَّ الأعراض الأُخرى قد تحدث أيضًا في حالات أخرى.[44]
تُوجد اختباراتٌ مخبرية لتشخيص الهربس النطاقي. يكشفُ الاختبار الأكثر شيوعًا عن الغلوبيولين المناعي م الخاص بفيروس جدري الماء النطاقي في الدم، ويظهرُ فقط خلال الإصابة بجدري الماء أو الهربس النطاقي، وليس أثناء حالة كمون الفيروس.[45] تقوم المختبرات الكبيرة بفحص اللمف المُجمع من بثرة، وذلك بواسطة تفاعل البوليميراز المتسلسل للحمض النووي الريبوزي منقوص الأكسجين لفيروس جدري الماء النطاقي، أو بفحصه بالمجهر الإلكتروني للبحث عن جزئيات الفيروس.[46] تعتبر الاختبارات الحيوية الجزيئية المُعتمدة على تضخيم الحمض النووي مختبريًا (اختبارات تفاعل البوليميراز المتسلسل) الأكثر موثوقيةً حاليًا. يمتلك اختبار تفاعل البوليميراز المتسلسل العشي حساسيةً عالية، ولكنه عرضةٌ للتلوث، مما يؤدي إلى نتائج إيجابية خاطئة. يكون اختبار تفاعل البوليميراز المتسلسل بالزمن الحقيقي سريعًا وسهل الأداء، وحساسًا مثل تفاعل البوليميراز المتسلسل العشي، كما له خطر تلوث أقل. هذه الاختبارات حساسيتها أكثر من زرع الفيروسات.[47]
التشخيص التفريقي
قد يحدثُ خلطٌ بين الهِربس النُطاقي مع الهربس البسيط أو التهاب الجلد الهربسي الشكل أو القوباء أو المظاهر الجلدية الناجمة عن التهاب الجلد التماسي وداء المبيضات ولسعات الحشرات وبعض الأدوية.[48]
الوقاية
توجد العديد من لُقاحات الهربس النُّطاقيّ الّتي تخفِّف من خطر الإصابة بالهربس النُّطاقيّ أو الإصابة الحادَّة إذا ما كانت الإصابة حاصِلة بالفعل؛[1][12] وذلك باحتواء اللقاح على فيروس حي مُضعَّف، كاللقاح «زوستافاكس» (بالإنجليزية: Zostavax) المُستعمل منذ عام 2006، أو كلُقاح الوُحَيدات المُساعِد المُسمَّى «شِنغريكس» (بالإنجليزية: Shingrix).[49][50]
أفادت مُراجعة قامت بها مؤسسة كوكرين أنَّ زوستافاكس كان مُفيدًا في الوقاية من الهربس النُّطاقي لمدَّة فعاليَّة لا تقلُّ عن ثلاث سنوات،[7] هذا يساوي قُرابة 50% من تخفيض الاخْتطار النِّسبيّ. يُقلِّل اللُّقاح من مُعدَّلات استِدامة شِدَّة الألم بعد الإصابة بالهربس النُّطاقيّ بنسبة 66% عند الأشخاص الَّذين تعرَّضوا للهربس النُّطاقيّ رغم تلقيحهم.[51] وبالرُّغم من ذلك، بقيت فعاليَّة اللُّقاح لمدَّة أربع سنوات من المُتابعة.[51] ويُنصَح بعدم إعطاء اللُّقاح الحي للأشخاص ذوي عَوَز المَناعة الأَوَّليّ أو المُكتَسَب.[51]
رَخَّصت إدارة الغذاء والدواء الأمريكيَّة استعمال شِنغريكس في عام 2007[52] وبالمثل فعلت وكالة الأدوية الأوروبية في 2018.[53] يُفضَّل أخذ جرعتين من اللُّقاح ممَّا يوفِّر 90% من الحماية لحوالي ثلاث سنوات ونصف،[50] أُجريت الدِّراسات حتَّى الآن على الأشخاص الَّذين مناعتهم سليمة،[12] وتبدو أيضًا فعَّالة عند الأشخاص المُسنِّين.[12]
تقدِّم هيئة الخدمات الصحيَّة البريطانيَّة زوستافاكس لكلِّ النَّاس بعمر 70 و78 سنة، وبحلول آب/أغسطس 2017 طُعِّم أقلّ من نصف المؤهَّلين لتلقِّي التطعيم الَّذين أعمارهم بين 70–78 سنة، وحوالي 3% من أولئك المؤهَّلين لديهم حالات خاصَّة تكبَح مناعتهم لا يجب أن يتلقَّوا التطعيم. لقد ورد 1104 تقرير عن التَّفاعلات الضَّائرة للتطعيم بحلول نيسان/أبريل 2018.[54] تنصح مراكز مكافحة الأمراض واتقائها في الولايات المتَّحدة الأمريكيَّة بأن يتلقَّى البالغون فوق 50 عامًا جرعتين من شِنغريكس يفصل بينهما 2 إلى 6 شهور.[55]
العلاج
تهدف المُعالجة للحدِّ من شِدَّة ومدَّة الألم؛ ممَّا يسمح بتقليل مدَّة نوائِب الهربس النُّطاقيّ إضافةً لتقليل المُضاعفات. وغالبًا ما تُحتاج المُعالجة الجهازيَّة للألم العصبيّ التالٍ للهِربس.[56] ورغم ذلك بيَّنت دراسة على الهربس النُّطاقيّ غير المُعالَج أنَّه فور اختفاء الطفح يكون الألم العصبيّ نادرًا خصوصًا لمن هم دون 50 عامًا ويخفُّ بمرور الوقت، وبالنِّسبة لمن هم أكبر سِنًّا يخفُّ الألم ببطئ، لكن حتَّى لمن تجاوزوا السَّبعين عامًا تخلَّص 85% منهم من الألم بعد عامٍ واحدٍ من إصابتهم بالمرض.[57]
مسكنات الألم
يُعالَج الألم الخفيف إلى المتوسِّط بالمُسكِّنات المُتاحة بدون وصفة، ويمكن استعمال الغَسولات الموضعيَّة المحتوية على الكالامين على الطَّفح أو النَّفْطَة ويهدِّؤها. يحدث أحيانًا ألم شديد قد يتطلَّب دواءً أَفْيُونِيَّ المَفْعُولِ مثل المورفين، وعندما تتقشَّر الإصابة يمكن استعمال كريم كابسيسين (زوستريكس، بالإنجليزيَّة: Zostrix). أيضًا يخفِّف اللِّيدوكائين الموضعيّ ومُحصِرات الأعصاب الألَم.[58] قد يفيد إعطاء الغابابنتين بالترافُق مع المُضادَّات الفيروسيَّة بتخفيف الألم العصبيّ التالٍ للهربِس.[56]
مضادات الفيروسات


تقلِّل المُضادَّات الفيروسيَّة من حِدَّة ومُدَّة المرض؛[59] لكنَّها لا تقي من الألم العصبيّ التالٍ للهربِس.[60] من هذه الأدوية آسيكلوفير الَّذي كان العِلاج المِعياريّ، لكن أظهر العلاجين الجديدين فالاسيكلوفير وفامسيكلوفير فعاليَّة مُشابِهة أو أكثر نَجَاعةً إضافةً لكونهما أكثر أمانًا وتحمُّلًا.[56] تستعمل هذه الأدوية للوقاية (كمثال، الأشخاص المُصابون بعَوَز المناعة المُكتَسَب) وكعلاجٍ خلال الطَّور الحادِّ، ويُمكن تقليل مُضاعفات الهربس النُّطاقيّ عند الأشخاص مَنْقوصي المَناعَة بإعطاء آسيكلوفير وريديًّا. أمَّا بالنِّسبة لمن هُم مُعَرَّضون بشدَّة لهجماتٍ مُتكرِّرة من الهربس النُّطاقيّ، عادةً ما تكون خمس جرعات فمويَّة يوميَّة من الآسيكلوفير فعَّالة.[24]
ستيرويدات
لم يبدو أنَّ الستيرويدات القشريَّة تقلِّل خطر الألم الممتد لفترة طويلة،[14] وتبقى تأثيراتها الجانبيَّة قليلة. لم يُدرَس استعمالها جيِّدًا في مُتَلاَزِمَة رامسي-هانت (عدوى العصب الوجهي والسمعي بفيروس الهربس) وذلك حتى عام 2008.[61]
الهربس النطاقي العيني
علاج الهِرْبِس النُّطاقِيّ العَينِيّ مُشابه للعلاج المِعياريّ للهربس النُّطاقيّ في مناطق أُخرى من الجسم. وفي دراسة أُجريت عام 2000 لمُقارنة الآسيكلوفير مع طَلِيعَته فالاسيكلوفير، بيَّنت أنَّ لهما نفس الفعاليَّة في علاج هذا المرض.[62] لكن تبقى مَيِّزة فالاسيكلوفير عن آسيكلوفير جرعته الَّتي هي ثلاث مَرَّات في اليوم (بالمقارنة مع آسيكلوفير: خمس مرَّات باليوم)، ممَّا يزيد امتثال المريض للعِلاج.[63]
المآل
يختفي الطفح والألم عادةً خلال ثلاثة إلى خمسة أسابيع، لكن يحصل عند واحدٍ من خمسة أشخاص حالة مؤلمة تدعى الألم العصبيّ التالٍ للهِربس غالبًا ما يصعب السيطرة عليها. يمكن أن يَسْتَنْشِط الهربس النُّطاقيّ عند بعض الأشخاص مُظهرًا «نُطاقيّ لا هِربسيّ» (بالإنجليزية: zoster sine herpete): ألم ينتشر على طول مَسار عصب شوكيٍّ وحيد (توزُّع القَطَّاعِ الجِلْدِيّ) ولا يترافق مع طفح. قد تتضمَّن هذه الحالة على مُضاعفات تؤثِّر مُستويات عديدة من الجهاز العصبيّ وتُسَبِّب عِدَّة اعتلالات عصبيَّة قحفيَّة أو التهاب الأعصاب أو الْتِهاب النُّخاع أو التهاب السَّحايا العقيم، ومن التأثيرات الخطيرة الأخرى الَّتي من الممكن أن تحدث شلل وجه جزئيّ (عادةً ما يكون مؤقَّتًا) أو ضرر أذنيّ أو التهاب الدِّماغ.[24] ومن الممكن أن تؤدِّي العداوى البَدئيَّة بفيروس جدري الماء النُّطاقيّ (VZV) خلال الحمل المُسبِّب للحُماق إلى عدوى للجنين ومُضاعفات قد لا تتعلق بعدوى الجنين عند حديثي الولادة أو عدوى مُزمنة أو استنشاط الهربس النُّطاقيّ.[64][65]
هناك خطر مُتزايد قليلًا لتطوُّر السَّرَطان بعد الإصابة بالهربس النُّطاقيّ، لكن تبقى آليَّة حدوث ذلك غير واضحة ولم يبدو أن هنالك زيادة بعدد الوفيَّات بسبب السرطان كنتيجة مُباشرة للإصابة بالفيروس.[66] وعلى النَّقيض من ذلك، قد ينتج الخطر المُتزايد من تثبيط المناعة الذي يسمح باستنشاط الفيروس.[67]
بالرُّغم من أنَّ الهربس النُّطاقيّ ينصرِف في غضون 3–5 أسابيع، إلَّا أنَّ بعض المُضاعفات قد تظهر:
- عَدوى جُرْثومِيَّة ثانويَّة.[9]
- مَشاكل حركيَّة،[9] خاصَّةً بعدوى «الهربس النُّطاقيّ الحَرَكِيّ» (بالإنجليزية: motor herpes zoster).[68]
- مشاكل عينيَّة، خاصَّةً بالعَصَبُ الثُّلاثِيِّ التَّوائِم (كما يُشاهَد في الهربس النُّطاقيّ العَينِيّ) الَّذي يجب أن يُعالَج مُبكِّرًا وبقوَّة لأنَّ التهاون في علاجه قد يقود للعَمَى. يعدُّ ظهور الطفح على مقدِّمة الأنف علامة قويَّة للإصابة بالهربس النُّطاقيّ العينيّ.[69]
- الألم العصبيّ التالٍ للهِربس، هو حالة من الألم المُزمِن بعد الإصابة بالهربس النُّطاقيّ.
الوبائية

حسب علم الأوبئة، فإنَّ لفَيْروسُ جدري الماء النُّطاقيّ مُستوىً عالٍ من الإِعْداء وانتشاره عالميٌّ.[70] ويكون الهربس النُّطاقيّ هو استنشاط لعدوى فيروس جدري الماء النُّطاقيّ: يمكن للهربس النُّطاقيّ أن يحدث فقط للشخص الَّذي أُصيب سابقًا بجدري الماء.
ليس للهربس النُّطاقيّ علاقة بالفصول ولا يُحدِث وباء، لكن توجد صِلة قويَّة بالتقدُّم بالعمر.[19][37] يتراوح معدَّل حدوثه بين 2‚1 إلى 4‚3 لكلّ 1000 شخص بالسنة (هذا بالنسبة لليافعين الأصحاء) وتزداد النِّسبة إلى 9‚3–8‚11 لكل 1000 شخص بالسنة لمن هم فوق 65 سنة،[8][19] وتتشابه مُعدَّلات حصوله عالميًّا.[8][71] ولقد أُثبتت هذه العلاقة بين العمر والإصابة بالفيروس في عدَّة بُلدان[8][71][72][73][74][75] وتُعزى إلى حقيقة تراجع المَناعة الخَلَوِيَّة مع التقدُّم بالعمر.
من عوامل الاختطار الأُخرى هو التَّثبيط المَناعيّ،[76][77][78] وأيضًا الضَّغط النَّفسيّ.[18][79][80] وتبعًا لدراسة في كارولينا الشَّماليَّة تبيَّن أنَّ «ذوي البشرة السمراء أقلّ عرضة لتطور الهربس النُّطاقيّ من ذوي البشرة البيضاء»،[81][82] ومن غير الواضح فيما إذا كان الاختطار مختلفًا حسب الجنس. يجدر الإشارة إلى أنَّ من عوامل الاختطار الأُخرى الرُّضوض الميكانيكيَّة والتَّعرُّض للذيفانات المَناعيَّة.[37][80]
لا يوجد دليل قويّ للعلاقة الوراثيَّة أو للتاريخ العائلي. في حين أظهرت دراسة أُجريت عام 2008 أنَّ الأشخاص الَّذين لديهم أقرباء شديدي الصِّلة ممَّن أُصيبوا بالهربس النُّطاقيّ سابقًا تزيد احتمالية إصابتهم بالفايروس الضِّعف عن إصابتهم به بأنفسهم،[83] لكن وجدت دراسة أُخرى عام 2010 أنَّه لا توجد أي علاقة.[80]
يتلقَّى البالغون ممَّن لديهم عدوى كامِنة بفيروس جدري الماء النُّطاقيّ والَّذين يُجالسون أطفالًا مُصابين بجديري الماء دفعة مَناعيَّة،[19][80] يُساعِد هذا التعزيز الدَّوريّ للمناعة على الوقاية من الهربس النُّطاقيّ عند البالغين. كانت هناك مَخاوف في الولايات المتَّحدة عندما قُدِّم لُقاح جديري الماء بانتظام بأنَّه قد تزيد الإصابات بعداوى الهربس النُّطاقيّ عند البالغين الَّذين لن يتلقَّوا تلك الدَّفعة المناعيَّة الطَّبيعيَّة من جديد.
وضَّحت دراسات عديدة وبيانات تَرَصُّديَّة أنَّه لم تسجَّل حدوث إصابات وبائية بالهربس النُّطاقيّ في الولايات المتَّحدة الأمريكيَّة منذ بدء برنامج لُقاح جديري الماء في عام 1995،[84] لكن بتحقيقٍ أعمق وُجِد أنَّه لا زيادة بعداوى الهربس النُّطاقيّ بين تجمُّعات السُّكَّان الَّذين لم ينتشر بينهم بعد لُقاح جديري الماء.[85][86] وفي دراسة لاحقة للدكتور باتل وآخرون توصَّلوا إلى أنَّه منذ تقديم لُقاح جديري الماء ازدادت كلفة الاستشفاءات من مُضاعفات الهربس النُّطاقيّ لتتخطَّى سبعمئة مليون دولار أمريكيّ سنويًّا بالنسبة لمن هُم فوق 60 سنة،[87] وفي دراسة أُخرى للدكتور يِيه وآخرون أفادت أنَّه منذ ازدياد إعطاء لُقاح جديري الماء للأطفال نقصت عداواه ولكن ازدادت عداوى الهربس النُّطاقيّ بين البالغين بنسبة 90%.[88] وأظهرت دراسة أُخرى للدكتور ياون وآخرون زيادة بنسبة 28% في عداوى الهربس النُّطاقيّ من 1996 إلى 2001.[89] من المُحتمل تغيُّر مُعدَّلات العداوى في المستقبل بسبب تقدُّم عمر السُّكَّان والتغيُّرات في علاج الأمراض الخبيثة وأمراض المناعة الذَّاتيَّة إضافةً للتغيُّرات في مُعدَّلات التلقيح لجديري الماء؛ إنَّ التبنِّي الواسع للقاح الهربس النُّطاقيّ قد يقلِّل مُعدَّلات العداوى.[8]
تبيَّن في دراسةٍ واحدة أنَّ 26% من الَّذين يتخلَّصون من الهربس النُّطاقيّ يُعانون من مُضاعفات في نهاية المَطاف، يُمثِّل الألم العصبيّ التالٍ للهِربس 20% تقريبًا من المُصابين بالفيروس.[90] ولقد وجدت دراسة لبيانات كاليفورنيا لعام 1994 أنًَ مُعدَّلات دخول المستشفيات ارتفعت من 1‚2 لكلّ 100000 شخص بالسنة إلى 3‚9 لكلّ 100000 شخص بالسنة لمن أعمارهم 60 سنة فما فوق،[91] وفي دراسة في ولاية كونيكتيكت الأمريكيَّة وجد أنَّ مُعدَّلات دخول المستشفيات أعلى؛ قد يُعزى الاختلاف إلى انتشار فيروس العوز المناعي البشري أو إلى تقديم المُضادَّات الفيروسيَّة في كاليفورنيا قبل 1994.[92]
التاريخ
للهربس النُّطاقيّ تاريخ طويل مُسجَّل وذلك على الرُّغم من عدم قدرة المُؤرِّخين على التَّمييز بين التقرُّحات الَّتي يُسبِّبها فيروس جدري الماء النُّطاقيّ والجُدَرِيّ،[31] والتَّسَمُّمُ بالأَرْغوت والحُمْرَة. ففي أواخر القرن الثَّامن عشر قدَّم وليام هيبيردين طريقة للتفريق بين الهربس النُّطاقيّ والجدري،[93] وفي أواخر القرن التاسع عشر مُيِّزَ الهربس النُّطاقيّ عن الحمرة. ولقد افترض ريتشارد برايت أنَّ المرض ينشأ من عُقْدَة الجَذْرِ الظَّهْرانِيّ، وأثبتت ذلك ورقة لِفريدريك فيليكس فون بورينسبرنج في عام 1861.[94]
كانت أولى الإشارات الدالَّة على أنَّ جديري الماء والهربس النُّطاقيّ يسببهما نفس الفيروس في بداية القرن العشرين، فقد لاحظ الأطباء أنَّ حالات الإصابة بالهربس النُّطاقيّ تتبَع جديري الماء عند اليافعين الَّذين عاشوا مع شخصٍ مُصاب بالهربس النُّطاقيّ. لقيت فكرة الارتباط بين المرضين زخمها عندما وجِد أنَّه يمكن للِمْف شخص مُصاب بالهربس النُّطاقيّ أن يُحرِّض جديري الماء عند اليافعين المتطوعين للدراسة. ولقد أُثبِت الأمر عندما عَزَل توماس ولر الفيروس لأوَّل مَرَّة في مَزارِع خَلَوِيَّة في عام 1953.[95]
اعتُبِر المرض حميدًا حتّى أربعينيَّات القرن العشرين (~1940) وكانت المُضاعفات الخطيرة نادرة للغاية.[96] لكن بحلول عام 1942 مُيِّزَ الهربس النُّطاقيّ كأحد الأمراض الخطيرة عند البالغين أكثر منه عند الأطفال، وتزداد تواتريَّة حدوثه بالتقدُّم بالعمر. ولقد بيَّنت دراسات حثيثة في خمسينيَّات القرن العشرين (~1950) على الأشخاص المُثَبَّطين مَناعيًّا أنَّ المرض لم يكن حَميدًا كما كان يُعتَقَد وبدأ منذ ذلك الحين البحث عن الخيارات العلاجيَّة والوقائيَّة المتنوِّعة.[97] وفي منتضف الستينيَّات من ذات القرن (~1960) بيَّنت دراسات عديدة حدوث نقصٍ تدريجيّ في الخلايا المناعيَّة عند كِبار السن؛ فلقد لوحِظ في أَتْرَابِيَّة (كَوكَبة، مَجموعة أشخاص) من 1000 شخص عاشوا حتَّى عمر 85 سنة، كان قُرابة 500 شخص منهم (أي ما يُعادِل 50%) قد أُصيب على الأقل بهجمة واحدة من الهربس النُّطاقيّ و10 أشخاص (حوالي 1%) على الأقل أُصيبوا بهجمتين.[98]
في الدراسات السَّابقة اعتُقِدَ أنَّ وقوع الهربس النُّطاقيّ يزداد بالتقدُّم بالعمر، لكن اقترح هوب سيمبسون في ورقته لعام 1965 أنَّ «توزُّع العمر المُمَيَّز للهربس النُّطاقيّ قد ينعكس جزئيًّا على تواتر حدوثه، وبسبب الدفعة المَناعيَّة الناتجة عن التعرُّض لحالات من جديري الماء تُساهِم الأضداد بالحماية من هجمات الهربس النُّطاقيّ الآجِلة».[19] ومن الداعِمات لهذه الفرضيَّة أنَّ التعامُل مع الأطفال المُصابين بجديري الماء (الحُماق) يعزِّز المَناعَة المُتَواسَطَة بالخَلاَيا للمُساعدة على إِرجاء أو كَبْح الهربس النُّطاقيّ، وَأوردت دراسة لتوماس وآخرون أنَّ البالغين ممَّن يعيشون في أُسرة بها أطفال يُصابون بالهربس النُّطاقيّ بنسبٍ منخفضة عمَّا هو الحال في الأُسَر الَّتي بلا أطفال.[99] وأيضًا في دراسة لِتيرادا وآخرون أشارت إلى أنَّ أطبَّاء الأطفال يُصابون بنسبة واحد من كلِّ طبيبين وصولًا حتَّى واحد من كلِّ ثمانية أطبَّاء نسبة إلى عُموم النَّاس من نفس عمرهم.[100]
الأبحاث
كانت مُضاعفات عداوى الجهاز العصبيّ المركزيّ نادرة خصوصًا الَّتي سببها استنشاط فيروس جدري الماء النطاقي نادرة وذلك حتَّى منتصف التسعينيات (~1990)، ويلزم لتشخيص عدوى جدري الماء النطاقي وجود طفح وأعراضٍ عصبيَّة محدَّدة. ومنذ عام 2000 أصبح استعمال فحص تفاعل البوليميراز المتسلسل (PCR) أكثر شيوعًا وزاد معه حالات تشخيص عدوى الجهاز العصبي المركزي.[101]
توصف الكتب التقليدية حالة استنشاط فيروس جدري الماء النطاقي في الجهاز العصبي المركزي بأنَّها محدودة بالأشخاص ضعيفي المناعة وكبار السن؛ لكن وجدت دراسات لاحقة أنَّ معظم المرضى مُؤَهَّلون مَناعِيًّا، وأعمارهم أقل من 60. وتشير المراجع القديمة للطفح الوعائيّ (بالإنجليزية: vesicular rash) كعلامة مميزة، لكن وجدت دراسات أحدث أنَّ الطفح يظهر عند 45% فقط من الحالات.[101] علاوة على ذلك لا يعد الالتهاب الجهازيّ مؤشِّرًا يُعتدُّ به كما كان يعتقد سابقا؛ فالمعدَّل الوسطيّ للبروتين المتفاعل-C وخلايا الدم البيضاء يبقى ضمن المجال الطبيعيّ عند المرضى المُصابين بالتهاب السحايا بفيروس جدري الماء النطاقي.[102] وتكون قيم التصوير بالرنين المغناطيسي والتصوير المقطعي المحوسب طبيعية في حالات استنشاط فيروس جدري الماء النطاقي في الجهاز العصبي المركزي. ولقد اعتقد سابقًا أنَّ كثرة خلايا السائل النخاعي دليل قوي على التهاب الدماغ بفيروس جدري الماء النطاقي لكنه كان غائبا عند نصف مجموعة من المرضى المشخصين بواسطة تفاعل البوليميراز المتسلسل بالتهاب الدماغ بفيروس جدري الماء النطاقي.[101]
تحضر حالات لا يُستهان بها من عداوى الجهاز العصبي المركزي إلى قسم طوارئ المستشفى المجتمعي، وذلك يستوجب وجود وسائل التشخيص المُلائمة. لا يعتبر تفاعل البوليميراز المتسلسل وسيلة مضمونة النتائج في التشخيص، لكن رغم ذلك يُنصح به بسبب اتضاح أنَّ المؤشِّرات الأخرى لا يعتد بها في تشخيص عداوى فيروس جدري الماء النطاقي في الجهاز العصبي المركزي. لا يعتمد على فحص تفاعل البوليميراز المتسلسل السَلبيّ في استبعاد عدوى فيروس جدري الماء النطاقي، لكن في المقابل يمكن استعمال الفحص الإيجابيّ للتشخيص واعتمادًا عليه يمكن البدء بالعلاج المُلائم (كمثال: يمكن وصف المضادات الفيروسيّة عوضًا عن المضادات الحيوية).[101]
بفضل ظهور تقنيات تحليل الحَمْض الرِّيْبِيّ النَّوَوِي المَنْزُوع الأوكسِجين تبيَّن أنَّ بعض مُضاعفات الهربس النُّطاقيّ شائعة أكثر ممَّا كان يُعتقد سابقًا، فلقد كان يعتبر الْتِهابُ السَّحايا والدِّماغ الفُرادي نادرًا ومُرتبطًا أكثر بجدريري الماء الطفولي. لكن ما يزال يُعتقد بازديادٍ أنَّ التهاب السَّحايا والدِّماغ الذي يسببه الهربس النُّطاقيّ سَببٌ سائِدٌ لهذا الالتهاب عند مَنقوصي المناعة من البالغين في ظروف غير وبائيَّة.[103]
من الصَّعب تشخيص مُضاعفات الهربس النُّطاقيّ خصوصًا في حالات استنشاط المرض بعد عُقودٍ من الكمون، فيمكن أن يتواجد الطفح أو يغيب وقد تختلف الأعراض وتتشابه مع أعراض فيروس الهربس البسيط.[103]
يمكن أن تظهر الأعراض جليَّة ورغم ذلك قد تكون نتيجة التحليل سَلبيَّة حتَّى في ظل تقنيَّات تحليل الحَمْض الرِّيْبِيّ النَّوَوِي المَنْزُوع الأوكسِجين مثل تفاعل البوليميراز المتسلسل.[104] ورغم هذا العجز أدَّى استعمال تفاعل البوليميراز المتسلسل لتقدُّمٍ في فهم فيروسات الهربس ومن ضمنها فيروس الهربس النُّطاقيّ بين التسعينيَّات (~1990) والألفينيَّات (~2000). فعلى سبيل المثال، اعتقد الأطبَّاء في الماضي أنَّ التهاب الدِّماغ سببه فيروس الهربس البسيط وأنَّ المرضى دائمًا يموتون أو يحصل عندهم مشاكل وظيفيَّة طويلة الأمد. شُخِّص الناس عند تشريح الجثة أو بواسطة خزعة الدماغ، ولا تؤخذ خزعة الدِّماغ باستخفاف بل في الحالات الخطيرة فقط الَّتي لا يمكن تشخيصها بوسائل أقلّ عدوانيَّة. ولهذا السَّبب كانت المعرفة حول فيروسات الهربس هذه مقتصرة على الحالات الشديدة، ومَكَّنت تقنيَّات الحَمْض الرِّيْبِيّ النَّوَوِي المَنْزُوع الأوكسِجين من تشخيص الحالات «الخَفيفة» التي يسببها فيروس الهربس النُّطاقيّ أو فيروس الهربس البسيط وتشتمل أعراضها على الحُمَّى والصُّداع وتبدُّل الحالة العقليَّة. ومن الواضح أنَّ مُعدَّل الوفيَّات بين المرضى المُعالَجين في تناقص.[103]
التسمية
الهِربِس النِطاقِي1[ِ 1][ِ 2][ِ 3][ِ 4][ِ 5] ويُسمى أيضًا: الحلأ النِطاقِي،[ِ 6][ِ 5] الحلأ المِنْطَقي،[ِ 3][ِ 7] الهِربسُ المِنْطَقي،[ِ 8][ِ 4] القُوْباء المَنطِقِية،[ِ 9][ِ 10] داء المَنْطِقَة،[ِ 9][ِ 4] العُقبولة المَنطقية،[ِ 7] الزُونا،[ِ 11] داء الزُّنَّار.[ِ 10]
يُعرف الهربس النطاقي بين العامة باسم الحزام الناري؛[ِ 12] وذلك لأنهُ يُصيب قطاعًا جلديًا مُعينًا فيأخذُ شكل الحزام مع لونٍ أحمرٍ مُختلفٍ عن باقي الجسم، كما يُسبب ألمًا حارقًا شديدًا. ويُعرف أيضًا باسم زُّنَّار النار،[ِ 13] والزُّنَّار هو الحزام، حيثُ يُقال مثلًا حِزامُ (أو زُنّارُ) الحَوض.[ِ 14]
- اللغة العربية
سُميَّ بالهربس النِطاقي لأنهُ يحدثُ بسبب فيروس جدري الماء النطاقي وهو واحدٌ من الفيروسات الهربسية، كما يُسبب طفحًا جلديًا يأخذُ شكلَ النِطاق أو الحِزام، ويرتبط بمنطقةٍ جلديةٍ مُحددة ؛ وهو يأتي من تفرع عصبون مصاب بالفيروس من تحت الجلد ويظهر على الجلد كبثرات.
يُقال لغويًا حَلأَ الجلد أي قشره،[ِ 15] وبالتالي سُمي بالحلأ النطاقي لأنَّ الطفح الجلدي نطاقي/حزامي الشكل يُصبح في النهاية حويصليا ثم تسقط القشرةُ عنه ويلتئم الجلد (طالع العلامات والأعراض).
- اللغة الإنجليزية
يُشتق اسم العائلة لجميع الفيروسات الهربسية (herpesviridae) من الكلمة اليونانية herpein، والتي تعني الزحف أو التسرب أو التسلل،[105] وذلك إشارةً إلى كمون وتكرار حدوث العدوى في مجموعة الفيروسات هذه. أما كلمة (Zoster) فتشتقُ من الكلمة اليونانية zōstēr، والتي تعني الحزام أو النطاق، وذلك إشارةٍ إلى الطفح الجلدي شبيه النطاق/الحزام المُرتبط بقطاعٍ جلديٍ مُعين.[106] الاسم الإنجليزي الشائع لهذا المرض هو (shingles) وهو مُشتقٌ من الكلمة اللاتينية cingulus، وهي شكلٌ لاتيني لكلمة cingulum والتي تعني النِطاق أو الحِزام أو الزُنَّار.[107]
- لغات أخرى
يُعرف الهربس النطاقي باللغة الإسبانية باسم «الثعبان الصغير»، وفي اللغة الهندية باسم «الطفح الكبير».[108] كما يُعرف باللغة النوريجية باسم helvetesild والتي تعني «نار الجحيم».[109]
انظر أيضًا
المراجع
بِاللُغة الإنجليزيّة
- ^ أ ب ت ث ج ح خ د ذ ر ز س ش ص ض ط ظ ع غ ف ق ك ل Hamborsky J (2015). Epidemiology and Prevention of Vaccine-Preventable Diseases (PDF) (ط. 13). Washington D.C. Public Health Foundation. ص. 353–74. مؤرشف (PDF) من الأصل في 2017-01-20.
 تتضمن هذه المقالة نصًا من هذا المصدر المُتاح في الملكية العامة.
تتضمن هذه المقالة نصًا من هذا المصدر المُتاح في الملكية العامة.
- ^ أ ب ت ث "Shingles (Herpes Zoster) Signs & Symptoms". مراكز مكافحة الأمراض واتقائها (CDC). 1 مايو 2014. مؤرشف من الأصل في 2015-05-26. اطلع عليه بتاريخ 2015-05-26.
 تتضمن هذه المقالة نصًا من هذا المصدر المُتاح في الملكية العامة.
تتضمن هذه المقالة نصًا من هذا المصدر المُتاح في الملكية العامة.
- ^ أ ب ت ث ج Cohen، JI (18 يوليو 2013). "Clinical practice: Herpes zoster". نيو إنغلاند جورنال أوف ميديسين. ج. 369 ع. 3: 255–63. DOI:10.1056/NEJMcp1302674. PMC:4789101. PMID:23863052.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Kahan، Scott (2003). In a Page Medicine. Lippincott Williams & Wilkins. ص. 215. ISBN:9781405103251. مؤرشف من الأصل في 2019-12-17.
{{استشهاد بكتاب}}: الوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ GBD 2015 Mortality and Causes of Death Collaborators (8 أكتوبر 2016). "Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980–2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. ج. 388 ع. 10053: 1459–1544. DOI:10.1016/s0140-6736(16)31012-1. PMC:5388903. PMID:27733281.
- ^ Rajendran، Arya؛ Sivapathasundharam، B (2014). Shafer's textbook of oral pathology (ط. Seventh). ص. 351. ISBN:9788131238004. مؤرشف من الأصل في 2019-12-17.
{{استشهاد بكتاب}}: الوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ أ ب ت Gagliardi AM، Andriolo BN، Torloni MR، وآخرون (3 مارس 2016). "Vaccines for preventing herpes zoster in older adults". مكتبة كوكرين. ج. 3: CD008858. DOI:10.1002/14651858.CD008858.pub3. PMC:6516976. PMID:26937872. مؤرشف من الأصل في 2010-01-10.
- ^ أ ب ت ث ج ح خ Dworkin RH، Johnson RW، Breuer J، وآخرون (2007). "Recommendations for the management of herpes zoster". Clin. Infect. Dis. 44 Suppl 1: S1–26. DOI:10.1086/510206. PMID:17143845.
- ^ أ ب ت Johnson RW، Alvarez-Pasquin MJ، Bijl M، وآخرون (2015). "Herpes zoster epidemiology, management, and disease and economic burden in Europe: A multidisciplinary perspective". Therapeutic Advances in Vaccines. ج. 3 ع. 4: 109–20. DOI:10.1177/2051013615599151. PMC:4591524. PMID:26478818.
- ^ "Shingles (Herpes Zoster) Transmission". مراكز مكافحة الأمراض واتقائها (CDC). 17 سبتمبر 2014. مؤرشف من الأصل في 2015-05-06. اطلع عليه بتاريخ 2015-05-26.
 تتضمن هذه المقالة نصًا من هذا المصدر المُتاح في الملكية العامة.
تتضمن هذه المقالة نصًا من هذا المصدر المُتاح في الملكية العامة.
- ^ أ ب "Overview". مراكز مكافحة الأمراض واتقائها (CDC). 17 سبتمبر 2014. مؤرشف من الأصل في 2015-05-16. اطلع عليه بتاريخ 2015-05-26.
 تتضمن هذه المقالة نصًا من هذا المصدر المُتاح في الملكية العامة.
تتضمن هذه المقالة نصًا من هذا المصدر المُتاح في الملكية العامة.
- ^ أ ب ت ث Cunningham، AL (2016). "The herpes zoster subunit vaccine". Expert Opinion on Biological Therapy. ج. 16 ع. 2: 265–71. DOI:10.1517/14712598.2016.1134481. PMID:26865048.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Chen N، Li Q، Yang J، وآخرون (6 فبراير 2014). "Antiviral treatment for preventing postherpetic neuralgia". مكتبة كوكرين. ج. 2 ع. 2: CD006866. DOI:10.1002/14651858.CD006866.pub3. PMID:24500927.
- ^ أ ب Han Y، Zhang J، Chen N، وآخرون (28 مارس 2013). "Corticosteroids for preventing postherpetic neuralgia". مكتبة كوكرين. ج. 3 ع. 3: CD005582. DOI:10.1002/14651858.CD005582.pub4. PMID:23543541.
- ^ Honorio T. Benzon (2011). Essentials of Pain Medicine (ط. 3rd). London: Elsevier Health Sciences. ص. 358. ISBN:9781437735932. مؤرشف من الأصل في 2017-03-18.
- ^ Zamula E (مايو–June 2001). "Shingles: an unwelcome encore". FDA Consumer. ج. 35 ع. 3: 21–25. PMID:11458545. مؤرشف من الأصل في 2009-11-03. اطلع عليه بتاريخ 2010-01-05.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) Revised June 2005. - ^ أ ب ت ث ج Stankus SJ، Dlugopolski M، Packer D (2000). "Management of herpes zoster (shingles) and postherpetic neuralgia". Am. Fam. Physician. ج. 61 ع. 8: 2437–44, 2447–48. PMID:10794584. مؤرشف من الأصل في 2007-09-29.
- ^ أ ب Katz J، Cooper EM، Walther RR، وآخرون (2004). "Acute pain in herpes zoster and its impact on health-related quality of life". Clin. Infect. Dis. ج. 39 ع. 3: 342–48. DOI:10.1086/421942. PMID:15307000.
- ^ أ ب ت ث ج Hope-Simpson RE (1965). "The nature of herpes zoster: a long-term study and a new hypothesis". Proceedings of the Royal Society of Medicine. ج. 58 ع. 1: 9–20. DOI:10.1177/003591576505800106. PMC:1898279. PMID:14267505.
- ^ Furuta Y، Ohtani F، Mesuda Y، وآخرون (2000). "Early diagnosis of zoster sine herpete and antiviral therapy for the treatment of facial palsy". Neurology. ج. 55 ع. 5: 708–10. DOI:10.1212/WNL.55.5.708. PMID:10980741.
- ^ أ ب Gupta S، Sreenivasan V، Patil PB (2015). "Dental complications of herpes zoster: Two case reports and review of literature". Indian Journal of Dental Research. ج. 26 ع. 2: 214–19. DOI:10.4103/0970-9290.159175. PMID:26096121.
- ^ Samaranayake L (2 سبتمبر 2011). Essential Microbiology for Dentistry (ط. 4th). Elsevier Health Sciences. ص. 638–42. ISBN:978-0-7020-4695-7. مؤرشف من الأصل في 2017-09-08.
- ^ Shaikh S، Ta CN (2002). "Evaluation and management of herpes zoster ophthalmicus". Am. Fam. Physician. ج. 66 ع. 9: 1723–30. PMID:12449270. مؤرشف من الأصل في 2008-05-14.
- ^ أ ب ت Johnson RW، Dworkin RH (2003). "Clinical review: Treatment of herpes zoster and postherpetic neuralgia". المجلة الطبية البريطانية. ج. 326 ع. 7392: 748–50. DOI:10.1136/bmj.326.7392.748. PMC:1125653. PMID:12676845. مؤرشف من الأصل في 2008-01-31.
- ^ أ ب ت ث ج Chi، AC؛ Damm، DD؛ Neville، BW؛ Allen، CM؛ Bouquot، J (11 يونيو 2008). Oral and Maxillofacial Pathology. Elsevier Health Sciences. ص. 250–53. ISBN:978-1-4377-2197-3. مؤرشف من الأصل في 2017-09-08.
{{استشهاد بكتاب}}: الوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ أ ب ت ث ج Glick M (1 سبتمبر 2014). Burket's oral medicine (ط. 12th). coco. ص. 62–65. ISBN:978-1-60795-188-9. مؤرشف من الأصل في 2020-04-02. اطلع عليه بتاريخ أكتوبر 2020.
{{استشهاد بكتاب}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) - ^ Chai W, Ho MG-R. Disseminated varicella zoster virus encephalitis. Lancet Available online 3 July 2014(0). نسخة محفوظة 29 نوفمبر 2014 على موقع واي باك مشين.
- ^ Grahn A، Studahl M (سبتمبر 2015). "Varicella-zoster virus infections of the central nervous system – Prognosis, diagnostics and treatment". Journal of Infection. ج. 71 ع. 3: 281–93. DOI:10.1016/j.jinf.2015.06.004. PMID:26073188.
- ^ James, William D.؛ Berger, Timothy G.؛ وآخرون (2006). Andrews' Diseases of the Skin: Clinical Dermatology. Saunders Elsevier. ISBN:978-0-7216-2921-6.
- ^ أ ب Steiner I، Kennedy PG، Pachner AR (2007). "The neurotropic herpes viruses: herpes simplex and varicella-zoster". ذا لانسيت. ج. 6 ع. 11: 1015–28. DOI:10.1016/S1474-4422(07)70267-3. PMID:17945155.
- ^ أ ب Weinberg JM (2007). "Herpes zoster: epidemiology, natural history, and common complications". J. Am. Acad. Dermatol. ج. 57 ع. 6 Suppl: S130–35. DOI:10.1016/j.jaad.2007.08.046. PMID:18021864.
- ^ Gilden DH، Cohrs RJ، Mahalingam R (2003). "Clinical and molecular pathogenesis of varicella virus infection". Viral Immunol. ج. 16 ع. 3: 243–58. DOI:10.1089/088282403322396073. PMID:14583142.
- ^ Kennedy PG (2002). "Varicella-zoster virus latency in human ganglia". Rev. Med. Virol. ج. 12 ع. 5: 327–34. DOI:10.1002/rmv.362. PMID:12211045.
- ^ Kennedy PG (2002). "Key issues in varicella-zoster virus latency". J. Neurovirol. 8 Suppl 2 ع. 2: 80–84. CiteSeerX:10.1.1.415.2755. DOI:10.1080/13550280290101058. PMID:12491156.
- ^ Mitchell BM، Bloom DC، Cohrs RJ، وآخرون (2003). "Herpes simplex virus-1 and varicella-zoster virus latency in ganglia" (PDF). J. Neurovirol. ج. 9 ع. 2: 194–204. DOI:10.1080/13550280390194000. PMID:12707850. مؤرشف (PDF) من الأصل في 2008-05-17.
- ^ Donahue JG، Choo PW، Manson JE، وآخرون (1995). "The incidence of herpes zoster". Archives of Internal Medicine. ج. 155 ع. 15: 1605–09. DOI:10.1001/archinte.155.15.1605. PMID:7618983.
- ^ أ ب ت Thomas SL، Hall AJ (2004). "What does epidemiology tell us about risk factors for herpes zoster?". ذا لانسيت. ج. 4 ع. 1: 26–33. DOI:10.1016/S1473-3099(03)00857-0. PMID:14720565.
- ^ "Shingles". NHS.UK. مؤرشف من الأصل في 2017-09-26. اطلع عليه بتاريخ 2017-09-25.
- ^ Schmader K (2007). "Herpes zoster and postherpetic neuralgia in older adults". Clin. Geriatr. Med. ج. 23 ع. 3: 615–32, vii–viii. DOI:10.1016/j.cger.2007.03.003. PMC:4859150. PMID:17631237.
- ^ Davison، AJ، Scott، وآخرون (1986). "The complete DNA sequence of varicella-zoster virus". J. Gen. Virol. ج. 67 ع. 9: 1759–1816. DOI:10.1099/0022-1317-67-9-1759. PMID:3018124.
- ^ Koh MJ، Seah PP، Teo RY (فبراير 2008). "Zosteriform herpes simplex" (PDF). Singapore Med. J. ج. 49 ع. 2: e59–60. PMID:18301829. مؤرشف (PDF) من الأصل في 2014-06-02.
- ^ Kalman CM، Laskin OL (نوفمبر 1986). "Herpes zoster and zosteriform herpes simplex virus infections in immunocompetent adults". Am. J. Med. ج. 81 ع. 5: 775–78. DOI:10.1016/0002-9343(86)90343-8. PMID:3022586.
- ^ Oranje AP، Folkers E (1988). "The Tzanck smear: old, but still of inestimable value". Pediatr. Dermatol. ج. 5 ع. 2: 127–29. DOI:10.1111/j.1525-1470.1988.tb01154.x. PMID:2842739.
- ^ Chan J، Bergstrom RT، Lanza DC، وآخرون (2004). "Lateral sinus thrombosis associated with zoster sine herpete". Am. J. Otolaryngol. ج. 25 ع. 5: 357–60. DOI:10.1016/j.amjoto.2004.03.007. PMID:15334402.
- ^ Arvin AM (1996). "Varicella-zoster virus" (PDF). Clin. Microbiol. Rev. ج. 9 ع. 3: 361–81. DOI:10.1128/CMR.9.3.361. PMC:172899. PMID:8809466. مؤرشف (PDF) من الأصل في 2008-06-25.
- ^ Beards G، Graham C، Pillay D (1998). "Investigation of vesicular rashes for HSV and VZV by PCR". J. Med. Virol. ج. 54 ع. 3: 155–57. DOI:10.1002/(SICI)1096-9071(199803)54:3<155::AID-JMV1>3.0.CO;2-4. PMID:9515761.
- ^ De Paschale M، Clerici P (2016). "Microbiology laboratory and the management of mother-child varicella-zoster virus infection". World J Virol (Review). ج. 5 ع. 3: 97–124. DOI:10.5501/wjv.v5.i3.97. PMC:4981827. PMID:27563537.
- ^ Sampathkumar P، Drage LA، Martin DP (2009). "Herpes zoster (shingles) and postherpetic neuralgia". Mayo Clin Proc (Review). ج. 84 ع. 3: 274–80. DOI:10.4065/84.3.274. PMC:2664599. PMID:19252116.
- ^ Harpaz R، Ortega-Sanchez IR، Seward JF (6 يونيو 2008). "Prevention of herpes zoster: recommendations of the Advisory Committee on Immunization Practices (ACIP)". MMWR Recomm. Rep. ج. 57 ع. RR–5: 1–30, quiz CE2–4. PMID:18528318. مؤرشف من الأصل في 2009-11-17. اطلع عليه بتاريخ 2010-01-04.
 تتضمن هذه المقالة نصًا من هذا المصدر المُتاح في الملكية العامة.
تتضمن هذه المقالة نصًا من هذا المصدر المُتاح في الملكية العامة.
- ^ أ ب Kathleen M. Neuzil؛ Marie R. Griffin (15 سبتمبر 2016). "Preventing Shingles and Its Complications in Older Persons". N Engl J Med. ج. 375 ع. 11: 1079–80. DOI:10.1056/NEJMe1610652. PMID:27626522.[Free]
- ^ أ ب ت Shapiro M، Kvern B، Watson P، وآخرون (أكتوبر 2011). "Update on herpes zoster vaccination: a family practitioner's guide". Can. Fam. Physician. ج. 57 ع. 10: 1127–31. PMC:3192074. PMID:21998225.
- ^ "Shingrix". U.S. Food and Drug Administration. 19 سبتمبر 2018. مؤرشف من الأصل في 2019-04-23. اطلع عليه بتاريخ 2019-03-16.
 تتضمن هذه المقالة نصًا من هذا المصدر المُتاح في الملكية العامة.
تتضمن هذه المقالة نصًا من هذا المصدر المُتاح في الملكية العامة.
- ^ "Shingrix". وكالة الأدوية الأوروبية. 28 مارس 2018. مؤرشف من الأصل في 2019-12-05. اطلع عليه بتاريخ 2019-03-16.
- ^ "NHS England warning as vaccine programme extended". Health Service Journal. 18 أبريل 2018. مؤرشف من الأصل في 2019-11-15. اطلع عليه بتاريخ 2018-06-10.
- ^ "Shingles (Herpes Zoster) Vaccination". مراكز مكافحة الأمراض واتقائها (CDC). 25 أكتوبر 2018. مؤرشف من الأصل في 2020-01-16. اطلع عليه بتاريخ 2019-01-18.
 تتضمن هذه المقالة نصًا من هذا المصدر المُتاح في الملكية العامة.
تتضمن هذه المقالة نصًا من هذا المصدر المُتاح في الملكية العامة.
- ^ أ ب ت Tyring SK (2007). "Management of herpes zoster and postherpetic neuralgia". J. Am. Acad. Dermatol. ج. 57 ع. 6 Suppl: S136–42. DOI:10.1016/j.jaad.2007.09.016. PMID:18021865.
- ^ Helgason S، Petursson G، Gudmundsson S، وآخرون (2000). "Prevalence of postherpetic neuralgia after a single episode of herpes zoster: prospective study with long term follow up" (PDF). المجلة الطبية البريطانية. ج. 321 ع. 7264: 794–96. DOI:10.1136/bmj.321.7264.794. PMC:27491. PMID:11009518. مؤرشف من الأصل في 2009-02-09.
- ^ Baron R (2004). "Post-herpetic neuralgia case study: optimizing pain control". Eur. J. Neurol. 11 Suppl 1: 3–11. DOI:10.1111/j.1471-0552.2004.00794.x. PMID:15061819.
- ^ Bader MS (سبتمبر 2013). "Herpes zoster: diagnostic, therapeutic, and preventive approaches". Postgraduate Medicine. ج. 125 ع. 5: 78–91. DOI:10.3810/pgm.2013.09.2703. PMID:24113666.
- ^ Chen N، Li Q، Yang J، وآخرون (2014). He L (المحرر). "Antiviral treatment for preventing postherpetic neuralgia". مكتبة كوكرين. ج. 2 ع. 2: CD006866. DOI:10.1002/14651858.CD006866.pub3. PMID:24500927.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|name-list-format=تم تجاهله يقترح استخدام|name-list-style=(مساعدة) - ^ Uscategui T، Doree C، Chamberlain IJ، وآخرون (16 يوليو 2008). "Corticosteroids as adjuvant to antiviral treatment in Ramsay Hunt syndrome (herpes zoster oticus with facial palsy) in adults". مكتبة كوكرين ع. 3: CD006852. DOI:10.1002/14651858.CD006852.pub2. PMID:18646170.
- ^ Colin J، Prisant O، Cochener B، وآخرون (2000). "Comparison of the Efficacy and Safety of Valaciclovir and Acyclovir for the Treatment of Herpes zoster Ophthalmicus". Ophthalmology. ج. 107 ع. 8: 1507–11. DOI:10.1016/S0161-6420(00)00222-0. PMID:10919899.
- ^ Osterberg L، Blaschke T (2005). "Adherence to medication". نيو إنغلاند جورنال أوف ميديسين. ج. 353 ع. 5: 487–97. DOI:10.1056/NEJMra050100. PMID:16079372.
- ^ Paryani SG، Arvin AM (1986). "Intrauterine infection with varicella-zoster virus after maternal varicella". نيو إنغلاند جورنال أوف ميديسين. ج. 314 ع. 24: 1542–46. DOI:10.1056/NEJM198606123142403. PMID:3012334.
- ^ Enders G، Miller E، Cradock-Watson J، وآخرون (1994). "Consequences of varicella and herpes zoster in pregnancy: prospective study of 1739 cases". ذا لانسيت. ج. 343 ع. 8912: 1548–51. DOI:10.1016/S0140-6736(94)92943-2. PMID:7802767.
- ^ Sørensen HT، Olsen JH، Jepsen P، وآخرون (2004). "The risk and prognosis of cancer after hospitalisation for herpes zoster: a population-based follow-up study". Br. J. Cancer. ج. 91 ع. 7: 1275–79. DOI:10.1038/sj.bjc.6602120. PMC:2409892. PMID:15328522.
- ^ Ragozzino MW، Melton LJ، Kurland LT، وآخرون (1982). "Risk of cancer after herpes zoster: a population-based study". نيو إنغلاند جورنال أوف ميديسين. ج. 307 ع. 7: 393–97. DOI:10.1056/NEJM198208123070701. PMID:6979711.
- ^ Ismail A، Rao DG، Sharrack B (2009). "Pure motor Herpes Zoster induced brachial plexopathy". Journal of neurology ع. 8. DOI:10.1007/s00415-009-5149-8. PMID:19434442.
- ^ Roat MI (سبتمبر 2014). "Herpes Zoster Ophthalmicus". Merck Manual. مؤرشف من الأصل في 2016-08-12. اطلع عليه بتاريخ 2016-08-14.
- ^ Apisarnthanarak A، Kitphati R، Tawatsupha P، وآخرون (2007). "Outbreak of varicella-zoster virus infection among Thai healthcare workers". Infect. Control Hosp. Epidemiol. ج. 28 ع. 4: 430–34. DOI:10.1086/512639. PMID:17385149.
- ^ أ ب Araújo LQ، Macintyre CR، Vujacich C (2007). "Epidemiology and burden of herpes zoster and post-herpetic neuralgia in Australia, Asia and South America" (PDF). Herpes. ج. 14 ع. Suppl 2: 40A–44A. PMID:17939895. مؤرشف من الأصل (PDF) في 2019-12-05.
- ^ Brisson M، Edmunds WJ، Law B، وآخرون (2001). "Epidemiology of varicella zoster virus infection in Canada and the United Kingdom". Epidemiol. Infect. ج. 127 ع. 2: 305–14. DOI:10.1017/S0950268801005921. PMC:2869750. PMID:11693508.
- ^ Insinga RP، Itzler RF، Pellissier JM، وآخرون (2005). "The incidence of herpes zoster in a United States administrative database". J. Gen. Intern. Med. ج. 20 ع. 8: 748–53. DOI:10.1111/j.1525-1497.2005.0150.x. PMC:1490195. PMID:16050886.
- ^ Yawn BP، Saddier P، Wollan PC، وآخرون (2007). "A population-based study of the incidence and complication rates of herpes zoster before zoster vaccine introduction". Mayo Clin. Proc. ج. 82 ع. 11: 1341–49. DOI:10.4065/82.11.1341. PMID:17976353.
- ^ de Melker H، Berbers G، Hahné S، وآخرون (2006). "The epidemiology of varicella and herpes zoster in The Netherlands: implications for varicella zoster virus vaccination" (PDF). Vaccine. ج. 24 ع. 18: 3946–52. DOI:10.1016/j.vaccine.2006.02.017. hdl:10029/5604. PMID:16564115. مؤرشف من الأصل (PDF) في 2017-08-08.
- ^ Colebunders R، Mann JM، Francis H، وآخرون (1988). "Herpes zoster in African patients: a clinical predictor of human immunodeficiency virus infection". J. Infect. Dis. ج. 157 ع. 2: 314–18. DOI:10.1093/infdis/157.2.314. PMID:3335810.
- ^ Buchbinder SP، Katz MH، Hessol NA، وآخرون (1992). "Herpes zoster and human immunodeficiency virus infection". J. Infect. Dis. ج. 166 ع. 5: 1153–56. DOI:10.1093/infdis/166.5.1153. PMID:1308664.
- ^ Tsai SY، Chen HJ، Lio CF، وآخرون (22 أغسطس 2017). "Increased risk of herpes zoster in patients with psoriasis: A population-based retrospective cohort study". PLoS ONE. ج. 12 ع. 8: e0179447. Bibcode:2017PLoSO..1279447T. DOI:10.1371/journal.pone.0179447. ISSN:1932-6203. PMC:5567491. PMID:28829784.
- ^ Livengood JM (2000). "The role of stress in the development of herpes zoster and postherpetic neuralgia". Curr. Rev. Pain. ج. 4 ع. 1: 7–11. DOI:10.1007/s11916-000-0003-9. PMID:10998709.
- ^ أ ب ت ث Gatti A، Pica F، Boccia MT، وآخرون (2010). "No evidence of family history as a risk factor for herpes zoster in patients with post-herpetic neuralgia". J. Med. Virol. ج. 82 ع. 6: 1007–11. DOI:10.1002/jmv.21748. hdl:2108/15842. PMID:20419815.
- ^ Schmader K، George LK، Burchett BM، وآخرون (1998). "Racial and psychosocial risk factors for herpes zoster in the elderly". J. Infect. Dis. ج. 178 ع. Suppl 1: S67–S70. DOI:10.1086/514254. PMID:9852978.
- ^ Schmader K، George LK، Burchett BM، وآخرون (1998). "Race and stress in the incidence of herpes zoster in older adults". J. Am. Geriatr. Soc. ج. 46 ع. 8: 973–77. DOI:10.1111/j.1532-5415.1998.tb02751.x. PMID:9706885.
- ^ Hicks LD، Cook-Norris RH، Mendoza N، وآخرون (مايو 2008). "Family history as a risk factor for herpes zoster: a case-control study". Arch. Dermatol. ج. 144 ع. 5: 603–08. DOI:10.1001/archderm.144.5.603. PMID:18490586.
- ^ Marin M، Güris D، Chaves SS، وآخرون (22 يونيو 2007). "Prevention of varicella: recommendations of the Advisory Committee on Immunization Practices (ACIP)". MMWR Recomm. Rep. ج. 56 ع. RR–4: 1–40. PMID:17585291. مؤرشف من الأصل في 2011-09-04.
 تتضمن هذه المقالة نصًا من هذا المصدر المُتاح في الملكية العامة.
تتضمن هذه المقالة نصًا من هذا المصدر المُتاح في الملكية العامة.
- ^ Jumaan AO، Yu O، Jackson LA، وآخرون (2005). "Incidence of herpes zoster, before and after varicella-vaccination-associated decreases in the incidence of varicella, 1992–2002". J. Infect. Dis. ج. 191 ع. 12: 2002–07. DOI:10.1086/430325. PMID:15897984.
- ^ Whitley RJ (2005 من). "Changing dynamics of varicella-zoster virus infections in the 21st century: the impact of vaccination". J. Infect. Dis. ج. 191 ع. 12: 1999–2001. DOI:10.1086/430328. PMID:15897983.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|سنة=(مساعدة) - ^ Patel MS، Gebremariam A، Davis MM (ديسمبر 2008). "Herpes zoster-related hospitalizations and expenditures before and after introduction of the varicella vaccine in the United States". Infect. Control Hosp. Epidemiol. ج. 29 ع. 12: 1157–63. DOI:10.1086/591975. PMID:18999945.
- ^ Yih WK، Brooks DR، Lett SM، وآخرون (2005). "The incidence of varicella and herpes zoster in Massachusetts as measured by the Behavioral Risk Factor Surveillance System (BRFSS) during a period of increasing varicella vaccine coverage, 1998–2003". BMC Public Health. ج. 5: 68. DOI:10.1186/1471-2458-5-68. PMC:1177968. PMID:15960856.
- ^ Yawn BP، Saddier P، Wollan PC، وآخرون (2007). "A population-based study of the incidence and complication rates of herpes zoster before zoster vaccine introduction". Mayo Clin. Proc. ج. 82 ع. 11: 1341–49. DOI:10.4065/82.11.1341. PMID:17976353.
- ^ Volpi A (2007). "Severe complications of herpes zoster" (PDF). Herpes. ج. 14 ع. Suppl 2: 35A–39A. PMID:17939894. مؤرشف من الأصل (PDF) في 2019-01-27.
- ^ Coplan P، Black S، Rojas C، وآخرون (2001). "Incidence and hospitalization rates of varicella and herpes zoster before varicella vaccine introduction: a baseline assessment of the shifting epidemiology of varicella disease". Pediatr. Infect. Dis. J. ج. 20 ع. 7: 641–45. DOI:10.1097/00006454-200107000-00002. PMID:11465834.
- ^ Weaver BA (1 مارس 2007). "The burden of herpes zoster and postherpetic neuralgia in the United States". J. Am. Osteopath. Assoc. ج. 107 ع. 3 Suppl: S2–57. PMID:17488884. مؤرشف من الأصل في 2008-01-13.
- ^ Weller TH (2000). "Chapter 1. Historical perspective". Varicella-Zoster Virus: Virology and Clinical Management. Cambridge University Press. ISBN:978-0-521-66024-2.
- ^ Oaklander AL (أكتوبر 1999). "The pathology of shingles: Head and Campbell's 1900 monograph". Arch. Neurol. ج. 56 ع. 10: 1292–94. DOI:10.1001/archneur.56.10.1292. PMID:10520948.
- ^ Weller TH (1953). "Serial propagation in vitro of agents producing inclusion bodies derived from varicella and herpes zoster". Proc. Soc. Exp. Biol. Med. ج. 83 ع. 2: 340–46. DOI:10.3181/00379727-83-20354. PMID:13064265.
- ^ Holt LE، McIntosh R (1936). Holt's Diseases of Infancy and Childhood. D Appleton Century Company. ص. 931–33. مؤرشف من الأصل في 2019-12-17.
- ^ Weller TH (1997). "Varicella-herpes zoster virus". Viral Infections of Humans: Epidemiology and Control. Plenum Press. ص. 865–92. ISBN:978-0-306-44855-3.
- ^ Hope-Simpson RE (1965). "The nature of herpes zoster; a long-term study and a new hypothesis". Proceedings of the Royal Society of Medicine. ج. 58 ع. 1: 9–20. DOI:10.1177/003591576505800106. PMC:1898279. PMID:14267505.
- ^ Thomas SL، Wheeler JG، Hall AJ (2002). "Contacts with varicella or with children and protection against herpes zoster in adults: a case-control study". ذا لانسيت. ج. 360 ع. 9334: 678–82. DOI:10.1016/S0140-6736(02)09837-9. PMID:12241874.
- ^ Terada K، Hiraga Y، Kawano S، وآخرون (1995). "Incidence of herpes zoster in pediatricians and history of reexposure to varicella-zoster virus in patients with herpes zoster". Kansenshogaku Zasshi. The Journal of the Japanese Association for Infectious Diseases. ج. 69 ع. 8: 908–12. DOI:10.11150/kansenshogakuzasshi1970.69.908. ISSN:0387-5911. PMID:7594784.
- ^ أ ب ت ث Becerra JC، Sieber R، Martinetti G، وآخرون (يوليو 2013). "Infection of the central nervous system caused by varicella zoster virus reactivation: a retrospective case series study". International Journal of Infectious Diseases. ج. 17 ع. 7: e529–34. DOI:10.1016/j.ijid.2013.01.031. PMID:23566589. مؤرشف من الأصل في 2019-12-17.
- ^ Ihekwaba UK، Kudesia G، McKendrick MW (15 سبتمبر 2008). "Clinical features of viral meningitis in adults: significant differences in cerebrospinal fluid findings among herpes simplex virus, varicella zoster virus, and enterovirus infections" (PDF). Clinical Infectious Diseases. ج. 47 ع. 6: 783–9. DOI:10.1086/591129. ISSN:1058-4838. PMID:18680414. مؤرشف من الأصل (PDF) في 2020-04-06.
- ^ أ ب ت Pollak L، Dovrat S، Book M، وآخرون (أغسطس 2011). "Varicella zoster vs. herpes simplex meningoencephalitis in the PCR era. A single center study". Journal of the Neurological Sciences. ج. 314 ع. 1–2: 29–36. DOI:10.1016/j.jns.2011.11.004. PMID:22138027.
- ^ Kojima Y، Hashiguchi H، Hashimoto T، وآخرون (15 سبتمبر 2008). "Recurrent Herpes Simplex Virus Type 2 Meningitis: A Case Report of Mollaret's Meningitis" (PDF). Japanese Journal of Infectious Diseases. ج. 55 ع. 3: 85–8. ISSN:1344-6304. PMID:12195049. مؤرشف (PDF) من الأصل في 2013-01-22.
- ^ "Herpes | Define Herpes at Dictionary.com". مؤرشف من الأصل في 2011-02-25. اطلع عليه بتاريخ 2011-03-14.
- ^ "Online Etymology Dictionary". مؤرشف من الأصل في 2011-06-26. اطلع عليه بتاريخ 2011-03-14.
- ^ "Online Etymology Dictionary". مؤرشف من الأصل في 2011-06-26. اطلع عليه بتاريخ 2011-03-14.
- ^ Yawn BP، Gilden D (3 سبتمبر 2013). "The global epidemiology of herpes zoster". Neurology. ج. 81 ع. 10: 928–30. DOI:10.1212/wnl.0b013e3182a3516e. PMC:3885217. PMID:23999562.
- ^ "Helvetesild (Herpes zoster)". helsenorge.no. مؤرشف من الأصل في 2016-12-22. اطلع عليه بتاريخ 2016-12-22.
بِاللُغة العربيَّة
- ^ "ترجمة (shingles) في المعجم الطبي الموحد". مكتبة لبنان ناشرون. مؤرشف من الأصل في 2019-11-13. اطلع عليه بتاريخ 2019-11-13.
- ^ "ترجمة (shingles) في المعجم الصيدلي الموحد". مكتبة لبنان ناشرون. مؤرشف من الأصل في 2019-12-18. اطلع عليه بتاريخ 2019-11-23.
- ^ أ ب "ترجمة (shingles) في المعجم الطبي". مكتبة لبنان ناشرون. مؤرشف من الأصل في 2019-12-18. اطلع عليه بتاريخ 2019-11-23.
- ^ أ ب ت "ترجمة (shingles) في قاموس المعاني". قاموس المعاني. مؤرشف من الأصل في 2015-09-05. اطلع عليه بتاريخ 2019-11-23.
- ^ أ ب "ترجمة (shingles) في موقع القاموس". القاموس. مؤرشف من الأصل في 2019-12-17. اطلع عليه بتاريخ 2019-11-23.
- ^ يُوسف حِتّي؛ أحمَد شفيق الخَطيب (2008). قامُوس حِتّي الطِبي للجَيب. بيروت، لبنان: مكتبة لبنان ناشرون. ص. 381 + 189. ISBN:995310235X.
{{استشهاد بكتاب}}: الوسيط|تاريخ الوصولبحاجة لـ|مسار=(مساعدة) - ^ أ ب "ترجمة (shingles) في معجم تشخيص الأمراض". مكتبة لبنان ناشرون. مؤرشف من الأصل في 2019-11-23. اطلع عليه بتاريخ 2019-11-23.
- ^ "ترجمة (shingles) في معجم طب الأسنان الموحد". مكتبة لبنان ناشرون. مؤرشف من الأصل في 2019-12-18. اطلع عليه بتاريخ 2019-11-23.
- ^ أ ب "ترجمة (shingles) في Thorndike Dictionary". مكتبة لبنان ناشرون. مؤرشف من الأصل في 2019-12-18. اطلع عليه بتاريخ 2019-11-23.
- ^ أ ب "ترجمة (shingles) في المغني الأكبر". مكتبة لبنان ناشرون. مؤرشف من الأصل في 2019-11-23. اطلع عليه بتاريخ 2019-11-23.
- ^ "ترجمة (shingles) في المعجم الطبي". مكتبة لبنان ناشرون. مؤرشف من الأصل في 2019-11-23. اطلع عليه بتاريخ 2019-11-13.
- ^ د. رشا قباني (2017). موسوعة صحة الطفل، المجلد الثالث. لبنان: دار المعرفة للطباعة والنشر. ص. 38.
{{استشهاد بكتاب}}: الوسيط|تاريخ الوصولبحاجة لـ|مسار=(مساعدة) - ^ عمر محسن نور (2019). النسخة العربية من (Energy Medicine: Medical and Religious Study). ص. 283.
{{استشهاد بكتاب}}: الوسيط|تاريخ الوصولبحاجة لـ|مسار=(مساعدة) - ^ "معنى كلمة "زنَار" في القاموس الجديد للمصطلحات العلمية والتقنية". مكتبة لبنان ناشرون. مؤرشف من الأصل في 2019-12-18. اطلع عليه بتاريخ 2019-11-13.
- ^ "معنى كلمة "حلأ" في معاجم عربية مُتعددة". www.almougem.com. مؤرشف من الأصل في 2019-12-17. اطلع عليه بتاريخ 2019-11-13.
وصلات خارجية
| هربس نطاقي في المشاريع الشقيقة: | |
