|
تضامنًا مع حق الشعب الفلسطيني |
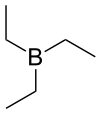
ثلاثي إيثيل البوران
| ثلاثي إيثيل البوران[1] | |
|---|---|
 |
 |
| الاسم النظامي (IUPAC) | |
Triethylborane |
|
| أسماء أخرى | |
ثلاثي إيثيل البورون |
|
| المعرفات | |
| الاختصارات | TEB |
| رقم CAS | 97-94-9 |
| بوب كيم (PubChem) | 7357 |
| الخواص | |
| الصيغة الجزيئية | C6H15B |
| الكتلة المولية | 98.00 غ/مول |
| المظهر | سائل عديم اللون إلى أصفر شاحب |
| الكثافة | 0.68 غ/سم3 |
| نقطة الانصهار | -93 °س |
| نقطة الغليان | 95 °س |
| الذوبانية في الماء | يتفاعل مع الماء |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
ثلاثي إيثيل البوران (أو ثلاثي إيثيل البورون) هو مركب بورون عضوي له الصيغة C2H5)3B)، يرمز له Et3B، بحيث أن Et ترمز لمجموعة الإيثيل، كما يرمز له اختصاراً TEB. يكون المركب على شكل سائل عديم اللون، يميل لونه أحياناً إلى الأصفر الشاحب.
التحضير
يحضر ثلاثي إيثيل البوران من تفاعل ثلاثي ميثيل البورات مع ثلاثي إيثيل الألومنيوم:[2]
حيث ترمز Et إلى مجموعة الإيثيل و Me إلى مجموعة الميثيل.
يكون الجزيء الناتج أحادي الجزئية (مونومر)، وذلك على العكس من المركب البادئ للبورانات H3B ومركب ثلاثي إيثيل الألومنيوم Et3Al، والتي تميل إلى تشكيل مركبات ثنائية الوحدات (ديمر).
يمكن أن يحضر المركب بطريقة أخرى من تفاعل ثنائي البوران، أو البوران المتناسق مع رباعي هيدرو الفوران، مع الإيثيلين.[3]
الخصائص
يكون ثلاثي إيثيل البوران في الشروط النظامية من الضغط ودرجة الحرارة عبارة عن سائل عديم اللون سهل الاشتعال، وسهل التطاير. يتفاعل Et3B مع الماء، لكنه ينحل في كل من رباعي هيدرو الفوران والهكسان، كما ينحل في ثنائي إيثيل الإيثر.[1]
إن لثلاثي إيثيل البوران بنية جزيئية ثلاثية مستوية،[2] وهو يتفكك إبّان التسخين.
الاستخدامات
مادة إشعال للوقود
استخدم ثلاثي إيثيل البوران في السابق من أجل إشعال وقود JP-7 في المحرك النفاث العنفي Pratt & Whitney J58 المستخدم في طائرات لوكهيد إس آر-71 بلاك بيرد،[4] وكذلك في طائرة لوكهيد إيه-12. يعد مركب ثلاثي إيثيل البوران مناسباً لهذا الغرض بسبب خاصية تلقائية الاشتعال لديه، خاصة أن احتراقه ناشر للحرارة.
في السابق كان ثلاثي إيثيل البوران يمزج مع 10-15% من ثلاثي إيثيل الألومنيوم من أجل استخدامه لإشعال المحرك الصاروخي F1 في صواريخ ساتورن 5.[5] وكذلك الأمر، فإن المزيج يستخدم في صواريخ فالكون 9 من شركة سبيس إكس.[6]
الكيمياء العضوية
يستخدم ثلاثي إيثيل البوران كبادئ جذري في التفاعلات الجذرية، ويكون فعّالاً حتى في درجات حرارة منخفضة، بحيث يمكن أن يحل محل مركبات القصدير العضوية المستخدمة لهذا الغرض.
يتفاعل ثلاثي إيثيل البوران مع إينولات الفلزات، حيث يعطي إينوكسي ثلاثي إيثيل البورات، والتي يمكن إجراء عملية ألكلة انتقائية لها بوجوده. يستخدم في تفاعل نزع أكسجين بارتون-ماكومبي Barton–McCombie deoxygenation من أجل نزع أكسجين مجموعة الهيدروكسيل في الكحولات، وبستخدم مع كاشف هيدريد ثلاثي رابعي بوتوكسي ألومنيوم الليثيوم LiAlH[OC(CH3)3]3 من أجل فصم الإيثرات.
يستخدم المركب من أجل تحريض أنواع محددة من تفاعل ريفورماتسكي Reformatsky reaction،[7] كما أنه يعد مركباً طليعيّاً لتحضير مركب ثلاثي إيثيل بوروهيدريد الليثيوم، والذي يعرف باسم الهيدريد الفائق، وذلك من خلال التفاعل مع هيدريد الليثيوم كما في المعادلة:
المراجع
- ^ أ ب صفحة بيانات المادة من شركة sigmaaldrich نسخة محفوظة 18 يونيو 2016 على موقع واي باك مشين.
- ^ أ ب Robert J. Brotherton, C. Joseph Weber, Clarence R. Guibert, John L. Little "Boron Compounds" in Ullmann's Encyclopedia of Industrial Chemistry 2000, Wiley-VCH. دُوِي:10.1002/14356007.a04_309
- ^ Buddrus، Joachim (2011)، Grundlagen Der Organischen Chemie، von Gruyter، ص. 172، ISBN:978-3110248944
- ^ "Lockheed SR-71 Blackbird". March Field Air Museum. مؤرشف من الأصل في 2014-01-05. اطلع عليه بتاريخ 2009-05-05.
- ^ A. Young (2008). The Saturn V F-1 Engine: Powering Apollo Into History. Springer. ص. 86.
- ^ Mission Status Center, June 2, 2010, 1905 GMT, SpaceflightNow, accessed 2010-06-02, Quotation: "The flanges will link the rocket with ground storage tanks containing liquid oxygen, kerosene fuel, helium, gaseous nitrogen and the first stage ignitor source called triethylaluminum-triethylborane, better known as TEA-TAB." نسخة محفوظة 14 نوفمبر 2015 على موقع واي باك مشين.
- ^ Yoshinori Yamamoto, Takehiko Yoshimitsu, John L. Wood, Laura Nicole Schacherer "Triethylborane" Encyclopedia of Reagents for Organic Synthesis. دُوِي:10.1002/047084289X.rt219.pub3
| ثلاثي إيثيل البوران في المشاريع الشقيقة: | |