|
تضامنًا مع حق الشعب الفلسطيني |
خلية دانيال

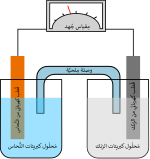
خلية دانيال (بالإنجليزية: Daniell Cell) هي نوع من الخلايا الكهروكيميائية التي تحول الطاقة الكيميائية إلى طاقة كهربائية، تتكون من ربط قطبين مختلفين هما قطب الخارصين (الانود) مغمور بمحلول كبريتات الخارصين وقطب النحاس (الكاثود) مغمور في محلول كبريتات النحاس، يصل بين محلوليهما جسر ملحي وهو عبارة عن انبوبة زجاجية تحتوي على محلول الكتروليتي لايتغير كيميائياً أثناء العمل ويساعد على انتقال الأيونات بين المحلولين ويكون مثبتا في الانبوبة بمادة صمغية طبيعية هي الأكار
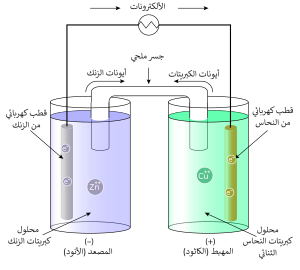
التفاعل
- Zn(s) → Zn2+(aq) + 2e−
- Cu2+(aq) + 2e− → Cu(s
اقرأ أيضا
| في كومنز صور وملفات عن: خلية دانيال |
مراجع
- ^ Borvon, Gérard (September 10, 2012). "History of the electrical units". Association S-EAU-S. نسخة محفوظة 12 أكتوبر 2016 على موقع واي باك مشين.
- ^ Hamer, Walter J. (January 15, 1965). Standard Cells: Their Construction, Maintenance, and Characteristics (PDF). National Bureau of Standards Monograph #84. US National Bureau of Standards. نسخة محفوظة 03 مارس 2016 على موقع واي باك مشين.
- ^ Spencer, James N.; Bodner, George M.; Rickard, Lyman H. (2010). Chemistry: Structure and Dynamics (Fifth Edition). John Wiley & Sons. p. 564. ISBN 9780470587119. نسخة محفوظة 10 ديسمبر 2017 على موقع واي باك مشين.