مكافئ (كيمياء)
المكافئ في الكيمياء هو الكتلة المكافئة من مادة لازمة لاتمام التفاعل مع 1 مول من أيونات الهيدروجين (H+) في وسط حامضي لتفاعل مع، أو لإتمام التفاعل مع 1 مول من الإلكترونات في تفاعل اختزالي.[1]*
مكافئ (كيمياء) |
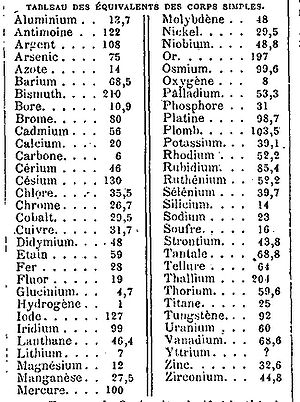
ويعبر عن الوزن المكافئ بوحدة الكتلة وهي تختلف عن الوزن الذري الذي ليست له وحدة . وقد عينت الأوزان المكافئة في الماضي أولا بطريق التجربة، والآن نستخدم عوضا عنها مول .
تاريخه
قام الكيميائي «كارل فينزيل» الألماني بنشر أول قائمة للأوزان المكافئة للأحماض والقواعد عام 1777. كما أعد الكيميائي يرينياس ريختر أيضا وبدون معرفته عمل فينزيل بنشر قائمة أكبر منها مبتدئا بعام 1792.[2]
وتضمنت قائمة جون دالتون التي نشرها عام 1808 وأشارت إلى العناصر : بأخذ كمية من الهيدروجين لتمثل وحدة الكتلة. ولكن نظرية دالتون لم تكن مقبولة في بداية القرن التاسع عشر. وكان سبب ذلك تفاعل الهيدروجين مع الاكسجين لإنتاج الماء. حيث يتفاعل 1 جرام من الهيدروجين مع 8 جرام من الأكسجين فينتجا 9 جرام ماء، فتقرر تحديد الوزن المكافئ للأكسجين ب 8 جرام.
وكانت صياغة التفاعل باستخدام أحجام الغازين طبقا لقانون جاي لوساك، وهي حجمان من الهيدروجين يتفاعلان نع حجم واحد من الأكسجين لينتجوا حجمين من الماء مما يعني أن والوزن الذري للأكسجين لابد وأن يكون 16.[2] وقام شارلز جيرهارد (1816–56), وهنري رينو (1810–78) وستانيسلاو كانيزارو (1826–1910) بمحاولات لتفسير ذلك التناقض وتناقضات أخرى مماثلة، ولكن مناثشة الموضوع استمرت حتى عام مؤتمر كارلسروهه 1860.[3]
ولم يكن اتخاذ حجم الهيدروجين عمليا حيث لا تتفاعل معظم العناصر بطريقة مباشرة مع الهيدروجين. إلا أنه من الثابت أن 1 جرام من الهيدروجين يتفاعل مع 8 جرام من الأكسجين لإنتاج الماء، أو يتفاعل 1 جرام من الهيدروجين مع 5و35 جرام من الكلور لإنتاج كلوريد الهيدروجين. وعلى ذلك فيمكن اعتبار 8 جرام من الأكسجين وبالتالي 5و35 جرام كلور مكافئة ل 1 جرام من الهيدروجين. ثم طُبق النظام على بقية الأحماض والقواعد.[2]
الاستخدام في الكيمياء
استعيض في الكيمياء عن استخدام الوزن المكافئ بالكتلة المولية . ويمكن حساب الأوزان المكافئة من الكتلة المولية إذا عرفت الخواص الكيميائية للمواد :
- حامض الكبريتيك له كتله مولية 98.078 g mol−1, وينتج 2 مول من أيونات الهيدروجين لكل 1 مول من حامض الكبريتيك. بذلك يصبح وزنه المكافئ =49.039 جرام.
- برمنجنات البوتاسيوم له وكتلة موليه 158.034 جرام، ويتفاعل مع 5 مول من الإلكترونات لكل مول من برمنجنات البوتاسيوم، بهذا يكون الوزن المكافئ للبوتاسيوم 31.6608 جرام.
- ومن الوجهة التاريخية، فكان تعيين الوزن المكافئ للعناصر يتم تجريبيا بدراسة تفاعل كل منممه الأكسجين. وعلى سبيل المثال : 50 جرام من الزنك تتفاعل مع 2الأكسجين لإنتاج 2و62 جرام من اكسيد الزنك مما يدل على أن الزنك قد تفاعل مع 2و12 جرام من الأكسجين (و1لك طبقا لقلنون بقاء المادة) :بذلك يصبح الوزن المكافئ للزنك هو الكتلة التي تتفاعل مع 8 جرام من الأكسجين، وبالتالي =
50nbsp;g × 8 g/12.24 g = 32.7 g.
المراجع
- ^ الاتحاد الدولي للكيمياء البحتة والتطبيقية (1998). Compendium of Analytical Nomenclature (definitive rules 1997, 3rd. ed.). Oxford: Blackwell Science. ISBN 0-86542-615-5. section 6.3.
- ^ أ ب ت "Atome"، Grand dictionnaire universel du XIXe siècle، Paris: بيير لاروس، ج. 1، 1866، ص. 868–73. (بالفرنسية)
- ^ See Charles-Adolphe Wurtz's report on the Karlsruhe Congress. نسخة محفوظة 16 ديسمبر 2017 على موقع واي باك مشين.