|
تضامنًا مع حق الشعب الفلسطيني |
كبريتات لوريل الأمونيوم
| كبريتات لوريل الأمونيوم | |
|---|---|
| الاسم النظامي (IUPAC) | |
كبريتات لوريل الأمونيوم |
|
| أسماء أخرى | |
• monododecyl ester, ammonium salt |
|
| المعرفات | |
| رقم CAS | 2235-54-3 |
| بوب كيم (PubChem) | 16700 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| الخواص | |
| الصيغة الجزيئية | C12H29NO4S |
| الكتلة المولية | 283.43 غ/مول |
| المظهر | سائل أصفر لزج |
| الكثافة | 1.02 غ/سم3 |
| نقطة الغليان | 418 °س، 691 °ك، 784 °ف |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
كبريتات لوريل الأمونيوم (أمونيوم لوريل سلفات اختصاراً ALS) هو الاسم الشائع لكبريتات دوديسيل الأمونيوم CH3(CH2)10CH2OSO3NH4. يتكون الأنيون من سلسلة هيدروكربونية غير قطبية ومجموعة نهائية قطبية كبريتات. يمنح الجمع بين المجموعات غير القطبية والمجموعات القطبية خصائص الفاعل بالسطح للأنيون: فهو يسهل إذابة المواد القطبية وغير القطبية. يصنف ALS على أنه إستر كبريتات . يوجد بشكل أساسي في الشامبو وغسول الجسم كعامل رغوي.[1] / [2] كبريتات اللوريل عبارة عن مواد خافضة للتوتر السطحي عالية الرغوة تعطل التوتر السطحي للماء جزئيًا عن طريق تكوين المذيلات عند السطح البيني للهواء.
التركيب الكيميائي والصيغة الجزيئية
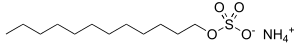
يلاحظ في الصيغة البنائية أن أحد طرفي الجزيء عبارة عن سلسلة طويلة من الكربون والهيدروجين، في حين أن الطرف الآخر هو ملح حامض الكبريتيك والأمونيا. وهذا هو سبب كون هذه المادة عامل رغوة قوي؛ حيث تلعب دورًا فعالًا في عملية التنظيف، وذلك لوجود طرف غير قطبي (كاره للماء ومحب للأوساخ التي غالبًا ما تكون دهون) والطرف الآخر «أيون الكبريتات» (محب للماء ويذوب فيه)؛ مما يجعل هذه المادة توجد في غالب منتجات التنظيف كعامل رغوة.
مستحضرات التجميل
توجد كبريتات لوريل الأمونيوم في أنواع المنتجات الأتية: شامبو غسول الجسم، بعض الصوابين السائلة [3]، بعض معاجين الأسنان، بعض منظفات البشرة، بعض منظفات الشعر (الشامبو)، كما توجد المادة أيضًا في (الشامبو) الشعر حيث اغلب منتجات تنظيف الشعر تحتوي على الامونيوم لوريال سلفات وهي تتفاعل مع إفرازات زيت الشعر وذرات الغبار والميكروبات، وتكون منها (مركبات كيميائية) كبيرة الحجم ولكن يسهل التخلص منها أثناء غسيل الشعر (بالماء) [4] وتوجد الامونيوم لوريال سلفات في (مستحضرات التجميل) وهي مهيجة بتركيز من 2 بالمئة أو أكثر كما يجب في (مستحضرات التجميل) أن لا تحتوي على تركيز أكبر من 1 بالمئة من الامونيوم لوريال سلفات [3]
السلامة
في تقرير يعود إلى عام 1983 من قبل مراجعة مكونات مستحضرات التجميل (Cosmetic Ingredient Review) أن الشامبو الذي يحتوي على ما يصل إلى 31٪ ALS سجل 6 شكاوى صحية من 6.8 مليون وحدة مباعة. وشملت هذه الشكاوى اثنين من حكة فروة الرأس ، واثنين من ردود الفعل التحسسية ، وتلف في الشعر ، وشكوى واحدة من تهيج العين.[5] [6]
خلص تقرير CIR إلى أن كلاً من كبريتات لوريل الصوديوم والأمونيوم «تبدو آمنة في التركيبات المصممة للاستخدام المتقطع والمتقطع متبوعًا بشطف سطح الجلد جيدًا. في المنتجات المعدة للاستخدام لفترات طويلة ، يجب ألا تتجاوز التركيزات 1٪».
أجرى مشروع تقييم المخاطر البشرية والبيئية (HERA) تحقيقًا شاملاً لجميع كبريتات الألكيل ، حيث أن النتائج التي توصلوا إليها تنطبق مباشرةً على ALS. تُظهر معظم كبريتات الألكيل سمية منخفضة حادة عن طريق الفم ، ولا توجد سمية من خلال التعرض للجلد ، وتهيج الجلد المعتمد على التركيز ، وتهيج العين المعتمد على التركيز. إنها لا تسبب حساسية للجلد ولا يبدو أنها مسرطنة في دراسة استمرت عامين على الفئران. وجد التقرير أن سلاسل الكربون الأطول (16-18) كانت أقل تهيجًا للجلد من السلاسل التي يبلغ طولها 12-15 كربونًا. بالإضافة إلى ذلك ، كانت التركيزات التي تقل عن 1٪ بشكل أساسي غير مزعجة بينما أدت التركيزات التي تزيد عن 10٪ إلى تهيج متوسط إلى قوي للجلد.[7]
أضرارها
أثبتت الدراسات الحديثة أن هذه المادة الكيميائية قد تضر ببصيلات الشعر؛ إذا أستعملت بشكل متكرر أو إذا احتوى المنتج على تركيزات عالية منها، كما تشير الدراسات بأن التركيزات العالية من الامونيوم لوريال سلفات يمكن أن تسبب نوع من التحسس في (الجلد) أو تهيج (العينين) وعلى المدى البعيد قد تسبب سرطان في الجسم[4]، ففي تقرير عام 1983 من قبل لجنة تقييم مكونات مستحضرات التجميل والشامبو تحتوي على ما يصل إلى 31٪ ALS كما سجلت 6 شكاوى صحية من 6.8 مليون وحدة مباعة. وتضمنت هذه الشكاوى اثنين من حكة فروة الرأس، واثنين من أمراض الحساسية، وتلف الشعر وشكوى واحدة من تهيج العين. وخلص التقرير إلى أن الامونيوم لوريل كبريتات «تظهر أن تكون آمنة في الصياغات التي صممت للاستعمال القصير المتقطع وتليها شامل الشطف من سطح الجلد. وفي المنتجات المعدة للاستخدام لفترات طويلة، يجب ان يكون تركيزها لايتجاوز 1٪».
البيئة
أجرى مشروع HERA أيضًا مراجعة بيئية لكبريتات الألكيل التي وجدت أن جميع كبريتات الألكيل قابلة للتحلل الحيوي بسهولة وأن عمليات معالجة مياه الصرف القياسية أزيلت 96-99.96٪ من كبريتات الألكيل قصيرة السلسلة (12-14 كربونًا). حتى في الظروف اللاهوائية ، يتحلل ما لا يقل عن 80٪ من الحجم الأصلي بيولوجيًا بعد 15 يومًا مع تحلل 90٪ بعد 4 أسابيع.[8]
انظر أيضا
مراجع
- ^ "Household Products Database – Ammonium Lauryl Sulfate". مؤرشف من الأصل في 2017-01-21. اطلع عليه بتاريخ 2007-01-25.
- ^ موسوعة أولمان للكيمياء الصناعية، فاينهايم: وايلي-في سي إتش، 2005
- ^ أ ب Dangers of Sodium Lauryl Sulfate | LIVESTRONG.COM نسخة محفوظة 08 مايو 2018 على موقع واي باك مشين.
- ^ أ ب موقع الطبي للمعلومات الطبية والصحية | أمراض وعلاج وأدوية نسخة محفوظة 13 أبريل 2018 على موقع واي باك مشين.
- ^ "Chemical Information Sheet – Ammonium Lauryl Sulfate" (PDF). مؤرشف من الأصل (PDF) في 2006-08-23. اطلع عليه بتاريخ 2007-01-25.
- ^ "Final Report on the Safety Assessment of Sodium Lauryl Sulfate and Ammonium Lauryl Sulfate". JACT, CIR Publication. ج. 2 ع. 7: 127–81. 1983.
- ^ "Human and Environmental Risk Assessment – Health Risks of Alkyl Sulfates" (PDF). مؤرشف من الأصل (PDF) في 2016-03-03. اطلع عليه بتاريخ 2007-01-25.
- ^ "Human and Environmental Risk Assessment for Alkyl Sulphates" (PDF). مؤرشف من الأصل (PDF) في 2006-11-07. اطلع عليه بتاريخ 2007-01-25.
| كبريتات لوريل الأمونيوم في المشاريع الشقيقة: | |

