|
تضامنًا مع حق الشعب الفلسطيني |
رابطة هيدروجينية متناظرة
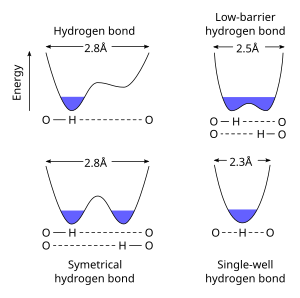
الرابطة الهيدروجينية المتماثلة هي نوع خاص من الرابطة الهيدروجينية ويعرف بانه يوجد فيه بروتون في منتصف المسافة تماما بين اثنين من الذرات المتطابقة . قوة الرابطة بين الذرتين متساوية وهي مثال للرابطة (بالإنجليزية: 3-center 4-electron bond). هذا النوع من الروابط اقوى بكثير من الرابطة الهيدروجينية العادية. في الحقيقة قوتها أشبه بالرابطة التساهمية . وذلك يظهر في الثلج تحت الضغط عند تجمد الماء (جليد), وكذلك في الطور الصلب لكثير من الأحماض اللامائية مثل : حمض الهيدروفلوريك وحمض الفورميك تحت ضغط عال. كما أيضا يلاحظ ذلك ايون الفلورايد الثنائي F-H-F
تستخدم أيضا للروابط الاحادية . هنالك جهود كبيرة عملت لبرهان مكانيكا كم الرباطة الهيدروجينية المتماثلة نجد ان البروتون محاط بأربعة الكترونات وبسبب هذه ، بعضهم يرى أن أن تكون رابطة أيونية.
تجمد الماء
- تتجمد السوائل عادة من الأسفل نحو الأعلى لكن الماء على العكس فهو يتجمد من الأعلى نحو الأسفل ، وهذه أول خاصية غير مألوفة للماء .
- عند تبيرد الماء يتزايد الماء في ثقله حتى تصل درجة حرارته إلى (4س) وعند تلك النقطة يحدث تغير مفاجئ ، فبدلاً من حدوث تقلص للماء فإنه يبدأ بالتمدد ويصبح وزنه أخف مع هبوط درجة الحرارة ،
- وهذا لأن جزيئات الماء تفقد طاقتها، وتقل حركتها، ويزيد ترابطها بالروابط الهيدروجينية المتماثلة ، بما يزيد من الفراغات بين جزيئات الماء.
- ويرتبط كل جزيء مادة في هذه الحالة ، بأربعة جزيئات مجاورة بروابط هيدروجينية في شكل ثلاثي الأبعاد .
- والنتيجة هي أن الماء ذي الدرجة (4س) يبقى في الأسفل والماء ذي الدرجة (3س) يكون اعلاه وماء الدرجة (2س) فوق منه وهكذا بالتدريج حتى الوصول إلى السطح ،
- عندئذ تكون درجة حرارته هي الصفر المئوية فقط وهنا يحدث التجمد، أي أن السطح فقط هو الذي يتجمد.
- أما طبقة الماء ذا الدرجة (4س ) فإنها تبقى سائلة تحت الجليد، وهي كافية لاستمرار حياة المخلوقات والنباتات تحت سطح الماء .
المراجع
- ^ Steiner، Thomas (2002). "The Hydrogen Bond in the Solid State". Angewandte Chemie International Edition. ج. 41: 48. DOI:10.1002/1521-3773(20020104)41:1<48::AID-ANIE48>3.0.CO;2-U.