محلول
المزيد من اللغات
المزيد من الإجراءات

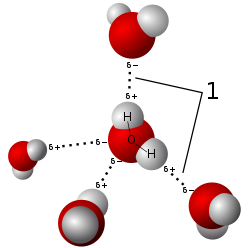
في الكيمياء، المحلول هو مزيج متجانس من مادتين نقيتين أو أكثر و لا يمكن عزلهما عن بعضهما البعض ، كالترشيح مثلاً ويتكون من مذيب ومذاب وغالبا يكون المذيب أكبر من المذاب مثل محلول السكر في الماء.[1][2][3] وعملية التحللّ أو التفكك تُسمّى أيضًا الذوبان. يمكن فصلهما عن طريق التبخير مثلا بحيث لا يتسبب في أي تفاعل كيميائي بين المادتين ، مثال على ذلك محلول ملح الطعام في الماء.
أنواع المحاليل
هناك ثلاثة أنواع رئيسية من المحاليل:
المحلول السائل
ينتج عن ذوبان صلب في سائل آخر، وكما ينتج عن ذوبان شيء صلب أو غازي في سائل. ومن أمثلته: ذوبان الملح في الماء، وذوبان السكر في الشاي.
المحلول الغازي
هو المحلول الذي ينشأ بإذابة المادة الصلبة أو السائلة أو الغازية في المادة السائلة، وينتج عن اختلاط الغازات. فالهواء مثلاً هو محلول غازي، يتكون من مزيج من النيتروجين والأكسجين، مع كميات ضئيلة من الأرجون وثاني أكسيد الكربون.
السبائك
تعتبر مصهورات المعادن محاليلا وتسمى سبائك . وعادة تتكون السبيكة من عدة فلزات و لا فلزات ، مثل بعض أنواع مصهورات الفولاذ ، فهو يتكون من كروم وفاناديوم وكربون ذائبة في الحديد.
طرق التعبير عن تركيز أي محلول
- المولار ويعرف على أنه إذابة 1 مول من المادة في 1 لتر من الماء.
أو:
- المولارية (M)= عدد مولات المادة المذابة ÷ حجم المحلول باللتر
أو:
- المولالية (M)= وزن المادة المذابة / (الوزن الجزيئي للماده * الحجم المحلول بالتر)
مثـــــــال:
بالنسبة إلى مركب مثل كلوريد الصوديوم : الوزن الذري للكلور (4و35 جرام) و الوزن الذري للصوديوم (23 جرام) ، ونظرا لأن تركيب الجزييء NaCl (أي 1 صوديوم متحد مع 1 كلور) ، فيكون 1 مول من كلوريد الصوديوم هو 4و58 جرام.
أي إذا أذبنا 4و58 جراما من ملح الطعام في 1 لتر ماء أصبح لدينا محلولا منه ذو مولارية 1.
- عندما نذيب 2و29 جراما من كلوريد الصوديوم في 1/2 لتر ماء يصبح لدينا محلولا منه ذو مولارية 1.
- وعندما نذيب 6و14 جراما من كلوريد الصوديوم في 1/4 لتر ماء يصبح لدينا أيضا محلولا مولاريته 1.
تعريفات أخرى للمحاليل:
يستخدم الكيميائيون محاليلا ذات تسميات أخرى ، مثل النورماليتي:
- النورملتى N = المولارية / تكافؤ المادة
وتعرف النورملتى Normality للماده بأنها عدد المولات من المادة الذائبة في 1 لتر ماء مقسومه على تكافؤ المادة.
- الكسر الجزيئي
- النسبة المئوية
الأصناف
تصنف المحاليل السائلة من حيث حالة الجزيئات المذابة كالتالي :
- محاليل حقيقية : وهي التي لاتترشح فيها جزيئات المذاب ولاتنفصل عن طريق الترشيح. لا يمكن تمييز دقائق المذاب بالعين المجردة أو بالمجهر - لا يمكن فصل مكوناته بالترويق أو الترشيح - متجانسs - مثل السكر في الماء
- محاليل غروية : وهي التي تكون فيها جزيئات المذاب غير مذاب تماما في المذيب ويمكن رؤيتها بشكل واضح في المحلول. يمكن تمييز دقائق المذاب بالمجهر الإلكتروني - لا يمكن فصل مكوناته بالترويق أو الترشيح - متجانس - مثل الحليب في الدم
- محاليل معلقة : وهي التي تتم فيها ترسب جزيئات المذاب مثل : الماء والرمل . يمكن تمييز دقائق المذاب بالعين - يمكن فصل مكوناته بالترويق أو الترشيح - غير متجانس -مثل الطباشير في الماء
- المحلول المستحلبات: المستحلبات Emulsions شكل صيدلاني سائل لزج ذو مظهر حليبي معـد للاستعمال الداخلي عن طريق الفم. يتكون من طورين يتم توزيع أحدهما داخل الآخر لتكوين المستحلب. وباستعمال عامل الاستحلاب Emulsifying، يسمى السائل المعلق بشكل قطيرات بالطور المبعثر Dispersed phase، أو الطور الداخلي Internal phase، أما السائل الذي تتبعثر فيه القطيرات الدقيقة فيسمى بالطور المستمر Continueos phase، أو الطور المبعثر Dispersing phase، أو الطور الخارجي External phase.
- مزايا المستـحلبات 1. إن تجزئة المـواد الدوائـية إلى قطيـرات صغيـرة تـزيد من مـعدل امتصاصها في الأمـعاء. 2. إخفاء الطعم والرائـحة غيـر المقبـولين للـزيت كمـا في مستـحلبات زيـت الخـروع. 3. إطالة مفـعول الـدواء وتـزيد من تأثيـره العطـري تبـعاً لصيغتها. 4. إن الماء سـواغ رخيـص الكلـفة ولـه قـدرة عـالية على حـل المـواد الـدوائية.
- أنواع المـستحلبات تـصنف المـستحلبات حسـب مـحتويات أطـوارها من الـسوائل إلى نوعـين: 1. مسـتحلبات زيـت في مـاء (ز/م) حيـث يكـون الطـور الخـارجي المـاء والطـور الداخـلي هو الزيـت ومـثال ذلك الحـليب، ولتحضيـر مثـل هذا النوع يستـعمل عـوامل إسـتحلاب محـبة للمـاء مثـل الصـمغ العـربي وصـمغ الكـثيراء وغـيرها. 2. مسـتحلبات مـاء في زيـت (م/ز) حيـث يكـون الطـور الخـارجي الـزيت والطـور الداخـلي هو المـاء ومثـال ذلك الزبـدة، ولتحـضير مثـل هـذا النـوع يسـتعمل عـوامل إسـتحلاب محـبة للزيـت مثـل دهـن الصوف Wool Fat وشمـع العسـل Beezwax وغيـرها.
- أمثلة على المستحلبات 1. مسـتحلب زيـت الخـروع الذي يسـتعمل مسـهلاً شـديداً بـجرعة 50-100مل، وفي التصـوير الشـعاعي للـجهاز الهـضمي بمـقدار 120مل دفعـة واحـدة. 2. مسـتحلب زيـت البـرافين الذي يسـتعمل مسـهلاً ومليـناً بمقـدار 30مل. 3. مسـتحلب زيـت كبـد الحـوت الذي يسـتعمل مصـدراً لفيـتامـين (أ) وفيـتاميـن (د) بمقـدار 15مل.
التشبع
وتصنف أيضا على حسب نسبة تركيز جزيئات المذاب في المذيب مذيب كالتالي :
- محاليل مشبعة:
تعتمد كمية المادة التي يمكن أن تذوب في مذيب على ذوبانها في هذا المذيب . وإذا أذبنا أكبر كمية ممكنة من المذاب في مذيب أصبح المحلول محلولا مشبعا . أي إذا أضفنا من المادة المذابة إلى مثل هذا المحلول فإنها تترسب ولا تذوب.
- محاليل غير مشبعة:
المحلول الذي يحتوي على كمية من المذاب أقل من الكمية التي توصله إلى حد التشبع.
- محاليل فوق مشبعة:
يتسم المحلول المشبع بهذه الخاصية عند درجة حرارة معينة ، ويعتمد تشبعه على درجة الحرارة ، أي إذا رفعنا درجة حرارة محلول مشبع درجتين مئويتين فإنه يذيب من المادة المذابة كمية أكبر عند تلك الدرجة العالية . ولو افترضنا أن لدينا محلولا مشبعا بملح الطعام عند درجة حرارة 82 درجة مئوية ، فإذا قمنا بتخفيض درجة الحرارة فجأة إلى 81 درجة مئوية مثلا أصبح المحلول «فوق مشبع» لفترة وجيزة ، ثم يترسب الملح الزائد .
حالات خاصة
لا يعتبر «ذوبان» فلز في حمض ذوبانا وإنما هو تفاعل كيميائي .
ولكن توجد حالات خاصة تتم فيها تفاعل كيميائي عكوسي و ذوبان في نفس الوقت ، مثل :
- ذوبان الصوديوم في سائل الأمونيا .
- ذوبان ثاني أكسيد الكربون في الماء ، حيث يحدث توازن بتكوين حمض الكربونيك و جزيئاته المفككة (أيونات بيكربونات و ايونات كربونات ) والتي تختفي عند مغادرة ثاني أكسيد الكربون المحلول (مثل طرده من المحلول بواسطة غاز آخر) .
المحاليل المركزة في الاستخدام المخبري
محلول المخزون هو محلول مركز يتم تخفيفه إلى تركيز أقل للاستخدام الفعلي ويُستخدم محلول المخزون لتوفير وقت التحضير والحفاظ على المواد وتقليل مساحة التخزين وتحسين الدقة التي يتم بها إعداد المحلول المستخدم منخفض التركيز.
في الكيمياء، يكون محلول المخزون عبارة عن حجم كبير من كاشف شائع بتركيز معياري مثل حمض الهيدروكلوريك أو هيدروكسيد الصوديوم. يستخدم هذا المصطلح بشكل شائع في الكيمياء التحليلية مثل المعايرةحيث من المهم استخدام التركيزات الدقيقة للحلول، لا تتكون تركيزات محلول المخزون بالضرورة من أرقام بسيطة فعلى سبيل المثال يمكن أن يكون المحلول 0.1 M حمض الهيدروكلوريك.
في الكيمياء الحيوية، غالبًاما يُستخدم المصطلح للإشارة إلى المحاليل المركزة ، والتي يمكن للشخص أن يخفف منها إلى تركيز المستخدم من المحلول.
انظر أيضًا
مراجع
- ^ الاتحاد الدولي للكيمياء البحتة والتطبيقية. "Concentration". Compendium of Chemical Terminology Internet edition.
- ^ الاتحاد الدولي للكيمياء البحتة والتطبيقية. "volume fraction". Compendium of Chemical Terminology Internet edition.
- ^ الاتحاد الدولي للكيمياء البحتة والتطبيقية. "fraction". Compendium of Chemical Terminology Internet edition.
| في كومنز صور وملفات عن: محلول |




