|
تضامنًا مع حق الشعب الفلسطيني |
فولدمير
هذه مقالة غير مراجعة. (نوفمبر 2020) |
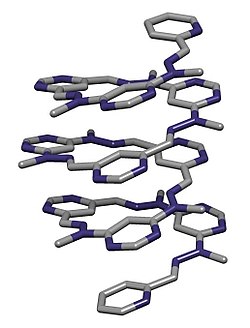
في الكيمياء، foldamer هو جزيء سلسلة منفصلة أو الأوليغومر (قليل الوحدات ) يتم ثنيه بشكل مرتب في المحلول. حيث أنها جزيئات اصطناعية تحاكي قدرة البروتينات والأحماض النووية والبولاسكاريد (متعدد السكريات) على الثني في اشكال محددة بشكل جيد، مثل لولب ثلالي الأبعاد helices وصفائح بيتا β-sheets. يتم تثبيت بنية الفولمميرمن خلال التفاعلات غير التساهمية بين المونومرات الغير متجاورة.[2][3] هدف دراسة (Foldamers) الأساسي هو تصميم جزيئات كبيرة ذات هياكل يمكن التنبؤ بها. كما ترتبط الدراسة بمواضيع التجميع الذاتي الجزيئي، والاعتراف الجزيئي، وكيمياء ضيف-مضيف.
التصميم

يمكن أن تختلف ال Foldamers من حيث الحجم، ولكن يتم تعريفها بوجود تفاعلات غير تساهمية وغير متجاورة. يستثني هذا التعريف الجزيئات مثل بولي أيزوسيانات المعروف عادة باسم (البولي يوريثان) و (بولي برولين) -اللولب متعدد البرولين- حيث أنها تنثني إلى حلزونات بشكل معتمد بسبب التفاعلات التساهمية المجاورة.[4] تحتوي ال Foldamers على تفاعل ديناميكي قابل للطي [غير مطوي ← مطوي] ، حيث ينتج الطي المجهري الكبير من خلال تأثيرات المذيبات (hydrophobic collapse) ، في حين أن حالة الطاقة النهائية لل Foldamers ترجع إلى التفاعلات الغير تساهمية. وتعمل هذه التفاعلات بشكل تعاوني لتكوين بنية ثلاثية أكثراستقراراً، حيث أن تكون الحالات المطوية بالكامل وغير المطوية أكثر استقرارًا من أي حالة مطوية جزئيًا.[5]
توقع الثني
يمكن التنبؤ ببنية ال foldamer في كثير من الأحيان من تسلسلها الأساسي. وتتضمن هذه العملية محاكاة ديناميكية للتوازنات القابلة للطي على المستوى الذري في ظل ظروف مختلفة. وقد يتم تطبيق هذا النوع من التحليل على بروتينات صغيرة، ولكن التكنولوجيا الحسابية غير قادرة على محاكاة كل التسلسلات باستثناء أقصرها.[6]
يمكن تحديد مسار الثني لل foldamer عن طريق قياس التباين عن الهيكل المفضل المحدد تجريبياً في ظل ظروف ديناميكية حرارية وحركية مختلفة.ويتم قياس التغير في الهيكل عن طريق حساب جذر متوسط الانحراف التربيعي عن موضع هيكل اساس البروتين المفصّل (Protein backbone).يمكن تحديد بنية الfoldamer في ظروف مختلفة حسابياً ومن ثم إثباتها تجريبياً.يمكن أن تنتج التغيرات في درجة الحرارة، لزوجة المذيبات، الضغط، الرقم الهيدروجيني (pH)، وتركيز الملح، معلومات قيمة حول بنية الفولمير. يسمح قياس حركية الثني وتوازنه للمرء بملاحظة تأثيرات هذه الظروف المختلفة على هيكل الfoldamer.[6]
غالبًا ما يؤثر المذيب على الثني. على سبيل المثال، قد يتم ثني مسار ينطوي على انهيار هيدروفوبكي (دفوع الماء) بشكل مختلف في محلول مذيب غير قطبي. سبب هذا الاختلاف هوحقيقة أن المذيبات المختلفة تستقر في وسط مختلف من مسار الثني، وكذلك مختلف هياكل مجسم ال(foldamer) النهائي القائم على التفاعلات بين الجزيئات الغير تساهمية.[6]
التفاعلات الغير تساهمية
االتفاعلات بين الجزيئات غير التساهمية، وإن كانت صغيرة بشكل فردي، فإن الجمع بينها يغير التفاعلات الكيميائية بشكل رئيسي. في ما يلي القوى المشتركة بين الجزيئات التي استخدمها الكيميائيون في تصميم الfoldamers.
- الرابطة الهيدروجينية (خاصة مع روابط الببتيد )
- تكديس Pi
- التأثيرات الكارهة للذوبان، والتي تؤدي إلى انهيار مسعور
- قوات فان دير فال
- جذب كهرباء
التصاميم المشتركة
يتم تصنيف ال Foldamers إلى ثلاث فئات مختلفة: بيبتى دوميمتيك، نيلكوتايدم، واللاأحيائية. الببتيدوميمتيك هي جزيئات اصطناعية تحاكي بنية البروتينات أما النيلكوتايدم فهي تستند إلى التفاعلات في الأحماض النووية. يتم تثبيت اللاأحيائية عن طريق التفاعلات العطرية وتفاعلات نقل الشحنة التي لا توجد بشكل عام في الطبيعة.[7] تعرف التصاميم الثلاثة الموصوفة أدناه عن تعريف مور الصارم لـ foldamer ، والذي يستبعد الطيات الحلزونية.
الببتيدوميتيك
غالبًا ما تكسر طيات المحاكاة الببتيدية التعريف المذكور سابقًا لألعاب الطية لأنها غالبًا ما تعتمد هياكل حلزونية . إنها تمثل معلمًا رئيسيًا لبحوث فولدمير نظرًا لتصميمها وقدراتها.[8][9] تتكون أكبر مجموعات محاكيات الببتيدات من β - ببتيدات ، γ - ببتيدات و δ - ببتيدات، ومجموعات أحادية محتملة. تختلف الأحماض الأمينية لهذه الببتيدات فقط بمقدار واحد () أو اثنين (γ) أو ثلاثة (δ) من كربون الميثيلين، ومع ذلك كانت التغييرات الهيكلية عميقة. تمت دراسة تسلسلات الببتيد هذه بشكل كبير حيث يؤدي التحكم في التسلسل إلى تنبؤ موثوق به. بالإضافة إلى ذلك، مع العديد من الميثيلين الكربون بين الكربوكسيل والأمينية ترميني من السندات الببتيد المرافقة، تتفاوت R السلاسل الجانبية المجموعة يمكن أن تكون مصممة. يمكن رؤية أحد الأمثلة على حداثة β-peptides في نتائج Reiser وزملائه في العمل.[10] باستخدام ببتيد مغاير يتألف من أحماض أمينية ألفا وأحماض كربوكسيلية cis-β-aminocyclopropanecarboxulic (cis-β-ACCs) ، وجدوا تكوين متواليات حلزونية في أوليغومرات قصيرة مثل سبعة بقايا وتشكل محدد في خمسة بقايا ؛ جودة تنفرد بها الببتيدات التي تحتوي على أحماض بيتا-أمينية دورية.[11][12][13][14]
نيوكليوتيدوميمتيك
لا تعتبر مقلدات النيوكليوتيد عمومًا مؤهلة كطابات. تم تصميم معظم لقواعد تقليد واحد DNA، النيوكليوسيدات ، أو النيوكليوتيدات من أجل nonspecifically DNA الهدف.[15][16][17] لهذه الأدوية عدة استخدامات طبية مختلفة بما في ذلك التطبيقات المضادة للسرطان والفيروسات والفطريات .
لاأحيائية

الطيات اللاأحيائية هي مرة أخرى جزيئات عضوية مصممة لإظهار الطي الديناميكي. إنهم يستغلون واحدًا أو عددًا من التفاعلات الأساسية المعروفة بين الجزيئات، على النحو الأمثل من خلال تصميمهم. أحد الأمثلة على ذلك هو oligopyrroles التي تنظم عند ربط الأنيونات مثل الكلوريد من خلال الرابطة الهيدروجينية (انظر الشكل). يتم تحفيز الطي في وجود أنيون: مجموعات البوليبيرول لديها القليل من القيود التوافقية بخلاف ذلك.[18][19]
أمثلة أخرى
- m - يتم دفع أوليغومرات إيثيلين إيثيلين فينيل إلى الطي في شكل حلزوني بواسطة قوى مقاومة الذوبان وتفاعلات التراص العطرية .
- β- الببتيدات تتكون من أحماض أمينية تحتوي على CH2 إضافيCH2</br> CH2 وحدة بين الأمين وحمض الكربوكسيل . فهي أكثر ثباتًا في حالة التحلل الإنزيمي وقد ثبت أن لها نشاطًا مضادًا للميكروبات.
- Peptoids عبارة عن polyglycines مستبدلة بـ N والتي تستخدم تفاعلات ستريكية للانحناء في هياكل حلزونية تشبه البولي برولين من النوع الأول.[20]
- Aedamers التي تطوى في المحاليل المائية مدفوعة بتفاعلات التكديس العطرية والطارئة للماء
- مجلدات Oligoamide العطرية هذه الأمثلة هي بعض من أكبر المجلدات وأكثرها تميزًا من الناحية الهيكلية.[21]
- طيات الأريلاميد، [22] مثل Brilacidin
المراجع
- ^ Lehn، Jean-Marie؛ وآخرون (2003). "Helicity-Encoded Molecular Strands: Efficient Access by the Hydrazone Route and Structural Features". Helv. Chim. Acta. ج. 86 ع. 5: 1598–1624. DOI:10.1002/hlca.200390137.
- ^ "Foldamers: Structure, Properties, and Applications" Stefan Hecht, Ivan Huc Eds. Wiley-VCH, Weinheim, 2007. (ردمك 9783527315635)
- ^ Hill، D. J.؛ Mio, M. J.؛ Prince, R. B.؛ Hughes, T. S.؛ Moore, J. S. (2001). "A field guide to foldamers". Chem. Rev. ج. 101 ع. 12: 3893–4012. DOI:10.1021/cr990120t. PMID:11740924.
- ^ Green، M. M.؛ Park, J.؛ Sato, T.؛ Teramoto, A.؛ Lifson, S.؛ Selinger, R. L. B.؛ Selinger, J. V. (1999). "The Macromolecular Route to Chiral Amplification". Angew. Chem. Int. Ed. ج. 38 ع. 21: 3138–3154. DOI:10.1002/(SICI)1521-3773(19991102)38:21<3138::AID-ANIE3138>3.0.CO;2-C.
- ^ Gellman، S.H. (1998). "Foldamers: A Manifesto". Acc. Chem. Res. ج. 31 ع. 4: 173–180. DOI:10.1021/ar960298r.
- ^ أ ب ت van Gunsteren، Wilfred F. (2007). Foldamers: Structure, Properties, and Applications; Simulation of Folding Equilibria. Wiley-VCH Verlag GmbH & Co. KGaA. ص. 173–192. DOI:10.1002/9783527611478.ch6.
- ^ "Foldamers: Structure, Properties, and Applications" Stefan Hecht, Ivan Huc Eds. Wiley-VCH, Weinheim, 2007. (ردمك 9783527315635)ISBN 9783527315635
- ^ Anslyn and Dougherty, Modern Physical Organic Chemistry, University Science Books, 2006, (ردمك 978-1-891389-31-3)
- ^ Martinek، T.A.؛ Fulop, F. (2012). "Peptidic foldamers: ramping up diversity". Chem. Soc. Rev. ج. 41 ع. 2: 687–702. DOI:10.1039/C1CS15097A. PMID:21769415.
- ^ De Pol، S.؛ Zorn, C.؛ Klein, C.D.؛ Zerbe, O.؛ Reiser, O. (2004). "Surprisingly Stable Helical Conformations in alpha/beta-Peptides by Incorporation of cis-beta-Aminocyclopropate Carboxylic Acids". Angew. Chem. Int. Ed. ج. 43 ع. 4: 511–514. DOI:10.1002/anie.200352267. PMID:14735548.
- ^ Seebach, D.; Beck, A.K.; Bierbaum, D. J.; Chem. Biodiv., 2004, 1, 1111-1239.
- ^ Seebach، D.؛ Beck, A.K.؛ Bierbaum, D.J. (2004). "Chemical and Biological Investigations of B-Oligoarginines". Chemistry & Biodiversity. ج. 1 ع. 1: 1111–1239. DOI:10.1002/cbdv.200490014. PMID:17191776.
- ^ Nizami, Bilal. "FoldamerDB: Database of foldamers". foldamerdb.ttk.hu (بEnglish). Archived from the original on 2020-07-06. Retrieved 2020-07-06.
- ^ Nizami, Bilal; Bereczki-Szakál, Dorottya; Varró, Nikolett; el Battioui, Kamal; Nagaraj, Vignesh U.; Szigyártó, Imola Cs; Mándity, István; Beke-Somfai, Tamás (8 Jan 2020). "FoldamerDB: a database of peptidic foldamers". Nucleic Acids Research (بEnglish). 48 (D1): D1122–D1128. DOI:10.1093/nar/gkz993. ISSN:0305-1048. Archived from the original on 2020-07-06.
- ^ Longley، DB؛ Harkin DP؛ Johnston PG (مايو 2003). "5-fluorouracil: mechanisms of action and clinical strategies". Nat. Rev. Cancer. ج. 3 ع. 5: 330–338. DOI:10.1038/nrc1074. PMID:12724731.
- ^ Secrist، John (2005). "Nucleosides as anticancer agents: from concept to the clinic". Nucleic Acids Symposium Series. ج. 49 ع. 49: 15–16. DOI:10.1093/nass/49.1.15. PMID:17150610.
- ^ Rapaport، E.؛ Fontaine J (1989). "Anticancer activities of adenine nucleotides in mice are mediated through expansion of erythrocyte ATP pools". Proc. Natl. Acad. Sci. USA. ج. 86 ع. 5: 1662–1666. Bibcode:1989PNAS...86.1662R. DOI:10.1073/pnas.86.5.1662. PMID:2922403.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ Sessler، J.L.؛ Cyr, M.؛ Lynch, V. (1990). "Synthetic and structural studies of sapphyrin, a 22-.pi.-electron pentapyrrolic "expanded porphyrin"". J. Am. Chem. Soc. ج. 112 ع. 7: 2810. DOI:10.1021/ja00163a059.
- ^ Juwarker، H.؛ Jeong, K-S. (2010). "Anion-controlled foldamers". Chem. Soc. Rev. ج. 39 ع. 10: 3664–3674. DOI:10.1039/b926162c. PMID:20730154. مؤرشف من الأصل في 2020-11-21.
- ^ Angelici، G.؛ Bhattacharjee، N.؛ Roy، O.؛ Faure، S.؛ Didierjean، C.؛ Jouffret، L.؛ Jolibois، F.؛ Perrin، L.؛ Taillefumier، C. (2016). "Weak backbone CH⋯O=C and side chain tBu⋯tBu London interactions help promote helix folding of achiral NtBu peptoids". Chemical Communications. ج. 52 ع. 24: 4573–4576. DOI:10.1039/C6CC00375C. PMID:26940758.
- ^ Delsuc، Nicolas؛ Massip، Stéphane؛ Léger، Jean-Michel؛ Kauffmann، Brice؛ Huc، Ivan (9 مارس 2011). "Relative Helix−Helix Conformations in Branched Aromatic Oligoamide Foldamers". Journal of the American Chemical Society. ج. 133 ع. 9: 3165–3172. DOI:10.1021/ja110677a. PMID:21306159.
- ^ De novo design and in vivo activity of conformationally restrained antimicrobial arylamide foldamers. Choi. 2009 نسخة محفوظة 25 يناير 2019 على موقع واي باك مشين.
قراءة إضافية
- Ivan Huc؛ Stefan Hecht (2007). Foldamers: Structure, Properties, and Applications. Weinheim: Wiley-VCH. ISBN:978-3-527-31563-5. مؤرشف من الأصل في 2022-11-29.
- "Foldamers as versatile frameworks for the design and evolution of function". Nat. Chem. Biol. ج. 3 ع. 5: 252–62. 2007. DOI:10.1038/nchembio876. PMID:17438550.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة)
المراجع
- ^ Gellman, S.H. (1998). "Foldamers: a manifesto" (PDF). Acc. Chem. Res. ج. 31 ع. 4: 173–180. DOI:10.1021/ar960298r. مؤرشف من الأصل (PDF) في 2008-05-13.
- ^ "Aromatic Amide Foldamers: Structures, Properties, and Functions". Chem. Rev. ج. 112 ع. 10: 5271–5316. 2012. DOI:10.1021/cr300116k. PMID:22871167.
- ^ Juwarker، H.؛ Jeong, K-S. (2010). "Anion-controlled foldamers". Chem. Soc. Rev. ج. 39 ع. 10: 3664–3674. DOI:10.1039/b926162c. PMID:20730154. مؤرشف من الأصل في 2020-11-21.