طية عصبية
المزيد من اللغات
المزيد من الإجراءات
| Neural fold | |
|---|---|
| الاسم العلمي plica neuralis |
|
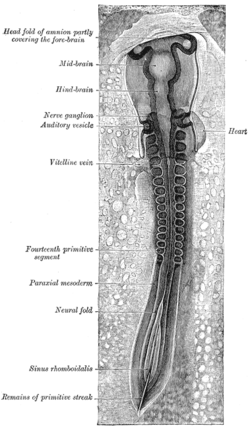
جنين دجاجة عمر ثلاث وثلاثين ساعة من الحضانة، ينظر إليها من الجانب الظهري. 30 ×. (طية عصبية معلمة في الوسط اليسار، الثالثة من الأسفل.)
| |
| تفاصيل | |
| مراحل كارنيجي | 9 |
| سلف | صفيحة عصبية |
| تعديل مصدري - تعديل | |
الطَّيَّةُ العَصَبِيَّة هي بنية تُنشأ أثناء تكون الخلايا العصبية في التطور الجنيني لكل من الطيور والثدييات من بين الكائنات الحية الأخرى.[1] ترتبط هذه البنية بالخلايا العصبية الأولية، مما يعني أنها تتشكل من خلال تجميع طبقات الأنسجة معًا، بدلاً من التجميع، والتفريغ اللاحق للخلايا الفردية (المعروفة باسم الخلايا العصبية الثانوية). عند البشر تكون الطيِّات العصبية مسؤولة عن تشكيل الطرف الأمامي للأنبوب العصبي. تُشتق الطيات العصبية من الصفيحة العصبية، وهي بنية أولية تتكون من خلايا الأديم الظاهر الممدودة. تؤدي الطيات إلى ظهور خلايا العرف العصبي، وكذلك تؤدي إلى تكوين الأنبوب العصبي.[2]
التطور
تنشأ الطيات العصبية عند الجنين من المنطقة التي تتلاقى فيها الصفيحة العصبية والأديم الظاهر المحيط. تتشكل هذه المنطقة من الجنين بعد تكون المعيدة، وتتكون من نسيج ظهاري. تستطيل الخلايا الظهارية عبر بلمرة الأنيبيبات الدقيقة، مما يزيد من ارتفاعها. توضح الصورة المصغرة أدناه هذه العملية. يتشكل لاحقًا العرف العصبي والأنبوب العصبي، الذي ينشأ من انضمام الطيات العصبية على بعضها البعض.[3]
الطي
يبدأ تكوين الطية العصبية بإطلاق الكالسيوم من داخل الخلايا. يتفاعل الكالسيوم المنطلق مع البروتينات التي تعدل خيوط الأكتين في النسيج الظهاري الخارجي، أو الأديم الظاهر؛ من أجل تحفيز حركات الخلية الديناميكية اللازمة لتكوين الطية.[4] تجتمع هذه الخلايا معًا عن طريق بروتين الكاديرين (خاصة الكاديرين E وN)، وهي أنواع من بروتين الربط بين الخلايا. عندما تقترب الخلايا الموجودة في قمم الطيات العصبية من بعضها البعض، سيؤدي التقارب بين جزيئات الكاديرين المتشابهة (النوع N) إلى ارتباطها ببعضها البعض. وهكذا، عندما تبدأ الخلايا السليفة للأنبوب العصبي في التعبير عن الكاديرين N بدلًا من الكاديرين E، سيتكون الأنبوب العصبي وينفصل عن الأديم الظاهر.[5] تحدث الكثير من الأمراض الخطيرة عندما تفشل الخلايا في الارتباط في مسارها الطبيعي من التطور.
نظرة عامة حول عملية الطي
تبدأ عملية الطي عندما ترتبط الخلايا الموجودة في المنطقة الوسطى من الصفيحة العصبية، وهي خلايا نقطة المفصلة الوسطى، بالحبل الظهري الموجود تحتها. وبذلك تتشكل نقطة مركزية لحدوث عملية الطي، ويبدأ الأخدود العصبي بالتشكل. مع استمرار تمدد الطي العصبي، تتشكل نقاط المفصلة الظهرية الوحشية، مما يسمح للطيات بالانحناء وتشكيل هيكل يشبه الأنبوب. عندما تتلامس قمم الطيات (المعروفة باسم مناطق العرف العصبي)، ستندمج وتلتف، مكونة الأنبوب العصبي تحت طبقة البشرة المتشكلة حديثًا.[6]
الآلية
تكمن الآلية الجزيئية وراء هذه العملية في قمع أو زيادة التعبير عن البروتينات المكونة للعظام (BMPs). البروتينات المكونة للعظام هي عائلة واسعة من البروتينات التي تؤدي وظائف عديدة في نمو الجنين، بما في ذلك تحفيز نمو الغضاريف والعظام. تحتاج الأنسجة العصبية السليفة إلى تقليل التعبير عن هذه البروتينات، وتحديدًا على طول الخط الإنسي، حيث سيتشكل الأخدود العصبي قريبًا. وذلك على عكس سلائف العظام أو أنسجة الغضاريف التي تحتاج إلى زيادة التعبير عن هذه البروتينات. تمنع البروتينات المنتجة من جينات نوجين وكوردين التعبير عن البروتينات المكونة للعظام، وتسمح بذلك بالتعبير عن الجينات العصبية، مثل جين SOX. ترمز هذه الجينات عوامل النسخ التي تغير التعبير الجيني لهذه الخلايا، وتعززها على طول مسار تطور الخلايا العصبية.[7] يسمح تثبيط البروتينات المكونة للعظام بتثبيت خلايا نقطة المفصلة الإنسية، مما يجعل الطيات العصبية جاهزة لحدوث الطي والإغلاق. تملك جينات نوجين وكوردين أدوارًا أخرى في عملية الطي، بما في ذلك تحفيز خلايا العرف العصبي للهجرة من الأنبوب العصبي حديث التكوين.[8][9] يلعب جين سونيك هيدجهوك أيضًا دورًا في تخفيف التعبير عن البروتينات المكونة للعظام، وتشكيل نقطة المفصلة الإنسيّة مع تثبيط تكوين نقاط المفصلة الظهرية الوحشية، وفي ضمان الإغلاق المناسب للطيات العصبية.[10] يُعتقد أن الصفيحة القردودية المقدمة، والحبل الظهري، والأديم الظاهر غير العصبي هي أنسجة محفزة مهمة تطلق هذه الإشارات الكيميائية، بهدف تحفيز طي الصفيحة العصبية.[7]
يرجع الالتصاق النهائي للطيات العصبية المتقاربة إلى عدة أنواع مختلفة من بروتينات الربط بين الخلايا. فمثلًا، الكاديرين وجزيئات مستقبلات كام الخاصة بها موجودة في نوعين في نسيج السلائف العصبية. يحافظ الكاديرين E على التصاق خلايا الصفيحة العصبية والأديم الظاهر المحيط ببعضهما البعض، بينما يقوم الكاديرين N بنفس الوظيفة مع خلايا الطية العصبية. تكون فقط الخلايا التي تعبر عن نفس نوع الكاديرين قادرة على الارتباط ببعضها البعض. وبما أن قمم الطيات العصبية هي التي تعبر عن الكاديرين N، فهي قادرة على الاندماج في تشكّل ورقي متصل من الخلايا. وبالمثل، فإن هذا التقارب المتناقص بين الخلايا التي تعبر عن أنواع مختلفة من الكادرين هو الذي يسمح للخلايا الأولية للأنبوب العصبي بالانفصال عن الأديم الظاهر، وتشكيل الأنبوب العصبي على الجزء الداخلي من الجنين والبشرة على السطح الخارجي. يوجد مجموعة أخرى من الجزيئات المشاركة في دمج الطيات العصبية هي جزيئات الإيفرين ومستقبلات الإيفرين التي تلتصق بطريقة مماثلة لجزيئات الكاديرين التي نوقشت أعلاه. [7]
انظر أيضًا
المراجع
- ^ "Towards a cellular and molecular understanding of neurulation". Developmental Dynamics. ج. 221 ع. 2: 117–45. يونيو 2001. DOI:10.1002/dvdy.1144. PMID:11376482.
- ^ "How to form and close the brain: insight into the mechanism of cranial neural tube closure in mammals". Cellular and Molecular Life Sciences. ج. 70 ع. 17: 3171–86. سبتمبر 2013. DOI:10.1007/s00018-012-1227-7. PMID:23242429.
{{استشهاد بدورية محكمة}}: الوسيط غير المعروف|PMCID=تم تجاهله يقترح استخدام|pmc=(مساعدة) - ^ Lawson A، Anderson H، Schoenwolf GC (فبراير 2001). "Cellular mechanisms of neural fold formation and morphogenesis in the chick embryo". The Anatomical Record. ج. 262 ع. 2: 153–68. DOI:10.1002/1097-0185(20010201)262:2<153::AID-AR1021>3.0.CO;2-W. PMID:11169910.
- ^ Ferreira MC، Hilfer SR (أكتوبر 1993). "Calcium regulation of neural fold formation: visualization of the actin cytoskeleton in living chick embryos". Developmental Biology. ج. 159 ع. 2: 427–40. DOI:10.1006/dbio.1993.1253. PMID:8405669.
- ^ Gilbert، Scott F. (2010). Developmental biology (ط. 9th). Sunderland, Mass.: Sinauer Associates. ISBN:978-0878933846.[بحاجة لرقم الصفحة]
- ^ Rocky S. Tuan؛ Cecilia W. Lo، المحررون (2000). "15". Developmental biology protocols, Volume 136. Humama. ص. 125–134. ISBN:9781592590650. اطلع عليه بتاريخ 2013-04-01.
- ^ أ ب ت Khong، Hrsg. Jean W. Keeling; Hrsg. T. Yee (2007). Fetal and Neonatal Pathology (ط. 4th). Godalming: Springer London. ص. 702–704. ISBN:978-1846285240.
{{استشهاد بكتاب}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Anderson RM، Stottmann RW، Choi M، Klingensmith J (سبتمبر 2006). "Endogenous bone morphogenetic protein antagonists regulate mammalian neural crest generation and survival". Developmental Dynamics. ج. 235 ع. 9: 2507–20. DOI:10.1002/dvdy.20891. PMC:6626635. PMID:16894609.
- ^ Stottmann RW، Berrong M، Matta K، Choi M، Klingensmith J (يوليو 2006). "The BMP antagonist Noggin promotes cranial and spinal neurulation by distinct mechanisms". Developmental Biology. ج. 295 ع. 2: 647–63. DOI:10.1016/j.ydbio.2006.03.051. PMC:3001110. PMID:16712836.
- ^ Kirillova I، Novikova I، Augé J، وآخرون (مايو 2000). "Expression of the sonic hedgehog gene in human embryos with neural tube defects". Teratology. ج. 61 ع. 5: 347–54. DOI:10.1002/(SICI)1096-9926(200005)61:5<347::AID-TERA6>3.0.CO;2-#. PMID:10777830.