|
تضامنًا مع حق الشعب الفلسطيني |
اقتران بكتيري
الاقتران البكتيري (بالإنجليزية: bacterial conjugation) كناية عن انتقال المادة الجينية بين الخلايا البكتيرية من خلال الاتصال المباشر بين خلية وأخرى أو عبر اتصال يشابه الجسر ويصل بين خليتين. حيث اكتشف كل من جوشوا ليديربرغ وإدوارد تاتوم هذا الاقتران في عام 1946، [1] والاقتران هو عبارة عن آلية انتقال جيني أفقي كما في التحويل والانتقال، مع أن هاتين العمليتين لا تجريان وفق الاتصال المباشر من خلية لأخرى.[2]
وفي أغلب الأحيان، يعتبر الاقتران البكتيري بشكل خاطئ مكافئا بكتيريا لإعادة الإنتاج الجنسي أو التزاوج بما أنه يتضمن تغيرا في المادة الجينية. خلال عملية الاقتران، تقوم الخلية المتبرعة بتقديم عنصر جيني مقرن أو تعبوي يكون في أغلب الأحيان إما بلازميد أو سلسلة ترانزبوسون.[3][4] كما تمتلك معظم البلازميدات المقرنة أنظمة تضمن عدم احتواء الخلية المستقبلة أصلا على عنصر مشابه.
إلى ذلك، فإن غالبا ما تكون المعلومات المنتقلة جينيا مفيدة للخلية المستقبلة. حيث يمكن لهذه الفوائد أن تشتمل على المقاومة الحيوية وتحمل مادة الإكسنبيوتك (أو مادة البيولوجيا الأجنبية الكيماوية) أو القدرة على استخدام مواد جديدة من الأيض. ومثل هذه البلازميدات المفيدة قد تعتبر حشرات إندوسيميونتس بكتيرية. أما العناصر الأخرى، على أية حال، فقد يتم إظهارها على أنها طفيليات بكتيرية، حيث يتطور الاقتران من خلالها كآلية عبر السماح بانتشارهم.
الآلية
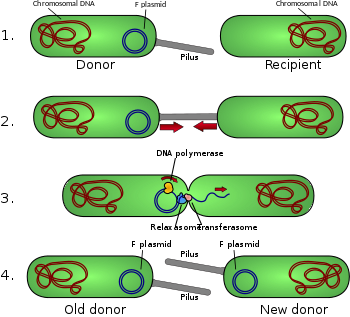
1- الخلية المتبرعة تنتج الأشعار. 2- الإشعار تتصل مع الخلية المستقبلة وتجمع خليتين سوية. 3- البلازميد المحمول يلحق ثم يحول بعد ذلك حبلا واحدا من الحمض النووي للخلية المستقبلة. 4- كلتا الخليتين تشكلان خيطا مكملا لإنتاج البلازميد المزدوج المعمم المعزول، إضافة إلى إنتاج الشعرة، كلتا الخلايتين أصبحتا الآن من الخلايا المانحة الصالحة
إن البلازميد المقرن النموذجي هو من طراز البلازميد -اف أو العامل –اف. وإن البلازميد – اف عبارة عن يصبوغ (أي البلازميد الذي يستطيع أن يدمج نفسه في الكروموسوم البكتيري من خلال إعادة تركيب متماثل) بطول يبلغ حوالي 100 كيلو بايت. كما أنه يحمل أصل التكرار أو النسخ المتماثل الخاص به، أو ما يسمى أوري في وبالإنكليزية oriV، كما يحمل أصل النقل، الذي يسمى بدوره أوري تي أو oriT بالإنكليزية.[3] ويمكن أن تتواجد نسخة واحدة فقط من البلازميد – اف في البكتيريا المعطاة، وإما أن تكون حرة أو مدمجة، حيث تدعى البكتيريا التي تحوز النسخة إف – بوزيتيف أو إيجابية العامل–اف، أو اف بلس (ويشار إليه بالرمز F+). أما الخلايا التي لا تحتوي على البلازما اف فتدعى اف – نيغاتيف أو سلبية العامل–اف، أو اف مينوس (ويشار إليها بالرمز F-) حيث يمكن لمثل هذه الخلايا أن تقوم بعمل المستقبلات.
ومن بين المعلومات الجينية الأخرى، يحمل البلازميد –اف موضع التي آر إي أو بالإنكليزية tra والتي آر بي أو trb، التي يبلغ طولهما معا حوالي 33 كيلو ويتألف مما يقارب 40 مورث. يتضمن موضع التي آر إي مورث البايلين وجينات تتظيمية، تشكل معا الأشعار أو بيلي على سطح الخلية. كما يتضمن الموضع أيضا جينات من أجل البروتينات التي تصل نفسها على سطح البكتيريا – F- وتبدأ عملية الاقتران. رغم ذلك، ثمة جدل قائم بشأن الآلية الدقيقة للاقتران حيث يبدو أن الأشعار ليست البنى التي يحدث تبادل الحمض النووي من خلالها. وقد تم إظهار ذلك في الاختبارات حيث سمح للشعرة بالاتصال، ثم شوبت فيما بعد بواسطة الاس دي اس، ومع ذلك فإن تحول الحمض النووي لا زال مستمرا. إلى ذلك، يبدو أن العديد من البروتينات المرمزة وفقا لموضع التي آر إي أو التي آر بي تقوم بفتح قناة بين البكتيريا وبذلك يبدأ إنزيم التي آر إي دي، المستقر في قاعدة الشعرة، يبدأ بانشطار الغشاء.
عندما يستهل الاقتران عبر إشارة، يخلق إنزيم ريلاكساس ملحق في أحد مقاطع بلأزمات الاقتران في أوري تي أو oriT. وقد يعمل ريلاكساس بشكل مفرد أو ضمن مجموعة مكونة من أكثر من دزينة من البروتينات المعروفة بمجموعها باسم ريلاكسوسوم.. هذا ويدعى إنزيم ريلاكساس في نظام البلازما – اف بالتي آر أي آي، حيث يتضمن ريلاكسوسوم كلا من التي آر أي آي، والتي آر أي واي، إضافة إلى التي آر أي ام والعامل المضيف المدمج وهو الآي اتش اف. أما المقطع الملحق، أو مقطع –تي أو T-strand، يفك بعدها من المقطع الذي لم يكسر بعد وينقل إلى الخلية المستقبلة في اتجاه من النهاية الخامسة إلى النهاية الثالثة. أما المقطع المتبقي فيتم تكراره إما بسلوك مقرن مستقل (ستنساخ خامل يبدأ عند أوري في) أو من خلال انسجام مع الاقتران (استنساخ اقتراني مشابه لاستنساخ الدائرة من lambda phage). هذا وقد يتطلب الاستنساخ المقرن ملحقا آخر قبل أن يستطيع الانتقال الناجح الحدوث، ويدعي تقرير آخر بمنع حدوث اقتران بواسطة مواد كيميائية عملت على تقليد خطوة الوسيط في هذا الحدث الملحق الثاني.[5]
إذا ما تم إدماج البلازما – اف الذي نقل في وقت سابق مع المورث المتبرع، فإن بعض الحمض النووي الصبغي للمتبرع قد ينتقل أيضا مع الحمض النووي البلازمي.[2] أما كمية الحمض النووي الصبغي الذي انتقل فهو يعتمد على مدى طول البكتيريتين المقترنتين اللتين بقيتا على اتصال. وفي المختبر الشائع، فإن سلاسل الإي. كولاي وبالإنكليزية إشريكية قولونية، تأخذ حوالي 100 دقيقة في تنقل كامل الكروموسوم البكتيري، وعندها يمكن للحمض النووي المنتقل أن يتحد ضمن المورث المستقبل عبر إعادة تركيب متشابه.
وعادة ما تتضمن بنية الخلية التي تحوي مع باقي مجموعات الخلايا على البلازميدات- اف الغير متكاملة، عادة ما تتضمن كذلك بعض الخلايا التي دمجت مصادفة بلازميداتها. وفي هذه الخلايا المسؤولة عن نقل مورث الكروموسوم ذي التردد المنخفض والمتسبب في مثل هذه البنى. كما يمكن لبعض سلاسل البكتيريا التي تحتوي على البلازميدات -اف المتكاملة أن تنعزل وتنمو في مثل هذه البنى النقية. ولأن مثل هذه السلاسل تقوم بنقل المورثات الكرموسومية بطريقة فعالة للغاية فإنها تدعى اتش اف آر(إعادة التركيب بتردد عال) Hfr. وقد تم تخطيط مورث الإي. كولاي في الأصل عن طريق اختبارات التزاوج التي تم توقيفها، حيث قصمت خلايا الاتش اف آر المختلفة في عملية الاقتران من قبل المستقبلات بعد أقل من 100 دقيقة (باستخدام خلاط وارنج بشكل مبدئي). هذا وإن المورثات التي تم تحويلها.
النقل ضمن المملكة
النتروجين المصلح ل الوزن الرطب، هو عبارة عن حالة مثيرة للاهتمام في الاقتران ضمن المملكة.[6] على سبيل المثال، إن الورم (Ti) المحفز لبلازميد الأجرعية وو جذر الورم (Ri) المحفز لبلازميد إي. ريزوجينز التي تحتوي على مورثات قادرة على الانتقال إلى خلايا النبات. وإن أسلوب هذه الجينات أو المورثات ينقل بشكل فعال خلايا النبات إلى مصانع إنتاج أحادية. هذا وتستخدم البكتيريا كمصادر للنتروجين والطاقة. أما الخلايا المصابة جراء الصفراء أو أورام الجذر، على التوالي، بذلك تكون كل من بلازميدات التي آي والآر آي بمثابة طفيليات في البكتيريا، وهي بدورها يمثابة أو طفيليات تتواجد في النبات المصاب.
كما يمكن لبلازميدات التي آي والآر آي أن تنتقل بين البكتيريا مستخدمة نظاما (سواء التي آر إي، أو التحول، أو أوبرنون) وهو نظام مختلف ومستقل عن النظام المستخدم في التحول ضمن المملكة، ومثل هذه التحولات تخلق سلاسل خبيثة من السلاسل الخبيثة السابقة.
تطبيقات الهندسة الوراثية
إن الاقتران عبارة عن وسيلة ملائمة لنقل المواد الجينية إلى العديد من الأهداف. وقد تم الإبلاغ عن تنقلات مخبرية ناجحة من البكتيريا إلى الخميرة، [7] والنبات، وخلايا الثدييات، [8][9] إضافة إلى الحبيبات الخيطية الثديية المعزولة.[10] هذا وقد تحسن الاقتران من خلال أشكال أخرى من التحول الجيني تتضمن حدا أدنى من انفصال مغلف الهدف الخلوي، والقدرة على نقل كميات كبيرة نسبيا من المادة الوراثية (انظر المناقشة الواردة أعلاه عن نقل كروموسوم الإي. كولاي). أما في الهندسة النباتية، فإن الأجرعية المماثلة للاقتران تكمل المركبات القياسية الأخرى مثل فيروس موزاييك التبغ (TMV). وبينما فيروس موزاييك التبغ يمتلك القدرة على التأثير في العديد من عائلات النبات، فإن هذه بشكل رئيسي تكون مشابهة إلى الفراش العشبي. وإن الأجرعية المشابهة للاقتران تستخدم أيضا في المقام الأول للفراش، ولكن مستقبلات المونوكوت النباتية لا تعتبر غير شائعة.
انظر أيضا
المراجع
- ^ Lederberg J, Tatum EL (1946). "Gene recombination in E. coli". Nature. ج. 158 ع. 4016: 558. DOI:10.1038/158558a0.
- ^ أ ب Griffiths AJF؛ وآخرون (1999). An Introduction to genetic analysis (ط. 7th). San Francisco: W.H. Freeman. ISBN:0-7167-3520-2. مؤرشف من الأصل في 2009-02-02.
{{استشهاد بكتاب}}: Explicit use of et al. in:|مؤلف=(مساعدة) - ^ أ ب Ryan KJ, Ray CG (editors) (2004). Sherris Medical Microbiology (ط. 4th). McGraw Hill. ص. 60–4. ISBN:0838585299.
{{استشهاد بكتاب}}:|مؤلف=باسم عام (مساعدة) - ^ Russi؛ وآخرون (2008). "Molecular Machinery for DNA Translocation in Bacterial Conjugation". Plasmids: Current Research and Future Trends. Caister Academic Press. ISBN 978-1-904455-35-6.
{{استشهاد بكتاب}}: Explicit use of et al. in:|مؤلف=(مساعدة) - ^ Lujan SA, Guogas LM, Ragonese H, Matson SW, Redinbo MR (2007). "Disrupting antibiotic resistance propagation by inhibiting the conjugative DNA relaxase". PNAS. ج. 104 ع. 30: 12282–7. DOI:10.1073/pnas.0702760104. JSTOR:25436291. PMC:1916486. PMID:17630285.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Pan SQ, Jin S, Boulton MI, Hawes M, Gordon MP, Nester EW (يوليو 1995). "An Agrobacterium virulence factor encoded by a Ti plasmid gene or a chromosomal gene is required for T-DNA transfer into plants". Mol. Microbiol. ج. 17 ع. 2: 259–69. DOI:10.1111/j.1365-2958.1995.mmi_17020259.x. PMID:7494475.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Heinemann JA, Sprague GF (يوليو 1989). "Bacterial conjugative plasmids mobilize DNA transfer between bacteria and yeast". Nature. ج. 340 ع. 6230: 205–9. DOI:10.1038/340205a0. PMID:2666856.
- ^ Kunik T, Tzfira T, Kapulnik Y, Gafni Y, Dingwall C, Citovsky V (فبراير 2001). "Genetic transformation of HeLa cells by Agrobacterium". Proc. Natl. Acad. Sci. U.S.A. ج. 98 ع. 4: 1871–6. DOI:10.1073/pnas.041327598. PMC:29349. PMID:11172043. مؤرشف من الأصل في 2019-12-10.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Waters VL (ديسمبر 2001). "Conjugation between bacterial and mammalian cells". Nat. Genet. ج. 29 ع. 4: 375–6. DOI:10.1038/ng779. PMID:11726922.
- ^ Yoon YG, Koob MD (2005). "Transformation of isolated mammalian mitochondria by bacterial conjugation". Nucleic Acids Res. ج. 33 ع. 16: e139. DOI:10.1093/nar/gni140. PMC:1201378. PMID:16157861. مؤرشف من الأصل في 2020-04-13.
وصلات خارجية
- الاقتران البكتيري (a Flash animation)
| اقتران بكتيري في المشاريع الشقيقة: | |