|
تضامنًا مع حق الشعب الفلسطيني |
جهاز مناعي تكيفي
الجهاز المناعي التكيفي ويُسمَّى أيضًا باسم الجهاز المناعي المكتسب أو مناعة مكتسبة[1] ونادرًا باسم الجهاز المناعي المتخصص، هو جهاز فرعيّ من الجهاز المناعي الكلي يضم خلايا مجموعيّة على درجة عالية من التخصص وعمليات تهدف إلى القضاء على العوامل الممرضة أو الحيلولة دون اختراقها خلايا الجسم. وانطلاقًا من اعتقاد أنه قد نشأ في أول الفقاريات ذوات الفك، يتم تنشيط الجهاز المناعي التكيفي أو «المتخصص» بواسطة الجهاز المناعي الفطري «غير المتخصص» الأقدم من حيث النشأة (والذي يعد آلية دفاع المضيف الأساسية ضد العوامل الممرضة في معظم الكائنات الحية الأخرى). ويزود هذا الجهاز الذاكرة المناعيّة بعد الاستجابة الأولى لعوامل ممرضة معينة لتوليد مناعة ولشن هجمات دفاعية أقوى في كل مرة تتم فيها مواجهة هذه العوامل الممرضة على وجه التحديد. عمل الجهاز المناعي التكيفي هو أساس. مثل الجهاز المناعي الفطري: يحتوي الجهاز المناعي التكيفي مكونات المناعة الخِلطيَّة ومكونات المناعة الخلويّة. ويشار إلى هذا النوع من المناعة باسم المناعة التكيفية نظرًا لأن الجهاز المناعي في الجسم يعد نفسه لمواجهة أي عوامل ممرضة أو كائنات غريبة في المستقبل.
على عكس الجهاز المناعي الفطري، الجهاز المناعي التكيفي مختص بدرجة عالية لعامل ممرض محدد. يستطيع تزويد الحماية لفترة طويلة، على سبيل المثال، شُفِيَ شخص ما من الحصبة بعدها سيكون محميًّا ضد الحصبة مدى حياته. في حالات أخرى، لا يمكنه توفير الحماية مدى الحياة، على سبيل المثال، الحُماق (جدري الماء). تدمر استجابة الجهاز المناعي التكيفي المُمْرِضات الغازِيَة وجزيئاتها السامة. في بعض الأحيان، لا يستطيع هذا الجهاز التمييز بين الجزيئات الغريبة المؤذية وغير المؤذية؛ لذا قد يسبب حمى الكلأ أو الربو أو أي أنواع أخرى من الحساسية. مولدات الضد هي مواد تستدعي استجابة الجهاز المناعي التكيفي. تمثل الخلايا الليمفاويّة -وهي أحد أنواع خلايا الدم البيضاء- استجابة الجهاز المناعي التكيفي. التصنيفان الرئيسيّان: استجابة الأجسام المضادة واستجابة المناعة الخلوية عن طريق الخلايا البائية والتائية، على الترتيب. استجابة الأجسام المضادة: تنشيط الخلايا البائية لإفراز الأجسام المضادة، وهي بروتينات تُعرَف أيضًا باسم غلوبولين مناعيّ. تتجول الأجسام المضادة خلال الدم المتدفق، وترتبط بمولدات الضد الغريبة لتثبيطها وعدم السماح لها بالارتباط بخلايا جسمنا.[2]
هذا الجهاز مكتسب؛ أي أنّ المستقبلات الخاصة بالمُمرض اُكتسِبت خلال حياة الكائن، بينما المستقبلات الخاصة بالمُمرض في الجهاز المناعي الفطري شُفِّرت مسبقًا في الخط الجنسي. الاستجابة المكتسبة تُسمَّى تكيفيّة؛ لأنها تحضر الجهاز المناعي في جسمنا للتحديات المستقبلية، ومع ذلك يمكنها أن تتكيف بطريقة خاطئة فتسبب المناعة الذاتية.[بحاجة لمصدر]|group= n}}
ويتميز هذا الجهاز بأنه قابل للتكيف بدرجة عالية بسبب فرط الطفرة الجسدية (حدوث مجموعة من الطفرات الجسدية المتلاحقة بشكل سريع) وعملية إعادة تشكيل V(D)J (عملية إعادة اتحاد جيني غير رجعيّة لأجزاء من جينات مستقبلات الأجسام المضادة). وتتيح هذه الآلية لعدد قليل من الجينات إنتاج عدد هائل من مستقبلات مولدات الضد المختلفة، والتي يتم حينئذٍ التعبير عنها بشكل مميز على كل خلية ليمفاوية منفردة. ونظرًا لأن عملية إعادة الاتحاد الجيني تحدث تغييرًا غير رجعيّ في الحمض النووي DNA الخاص بكل خلية، فإن كل ذرية (نسل) من تلك الخلية سترث الشفرة الجينيية الخاصة بنفس نوعية المستقبل، بما في ذلك خلايا الذاكرة البائية (Memory B cells) وخلايا الذاكرة التائية (Memory T cells) التي تعد المفاتيح الأساسية اللازمة للتمتع بمناعة متخصصة (نوعية) طويلة الأجل. وفي هذا الصدد، هناك نظرية تعرف باسم نظرية الشبكة المناعية، وهي نظرية توضح آلية عمل الجهاز المناعي التكيفي، والمعتمدة على تفاعلات بين المناطق المتغيرة لمستقبلات الخلايا التائية والخلايا البائية ومستقبلات الجزيئات التي تكونها الخلايا التائية والخلايا البائية التي لها مناطق متغيرة.
توضح نظرية الشبكة المناعية عمل الجهاز المناعي التكيفي، بُنيت هذه النظرية على أساس مفهوم الانتقاء النسيليّ، وتُطبَّق في البحث عن لقاح فيروس نقص المناعة البشري.
وظائف الجهاز المناعي التكيفي
يتم تنشيط المناعة التكيفية عند الفقاريات عندما يخترق أحد العوامل الممرضة الجهاز المناعي الفطري ويولد مستوًى عتبيًا للمستضدات.[3]
وتشمل الوظائف الرئيسية للجهاز المناعي التكيفي ما يلي:
- التعرف على المستضدات النوعية «غير الذاتية» في وجود المستضدات «الذاتية»، أثناء عملية عرض المستضد
- توليد مجموعة استجابات يتم تطويعها بشكل خاص للقضاء بالكامل على عوامل ممرضة معينة أو على خلايا مصابة بعوامل ممرضة
- توليد ذاكرة مناعية، والتي يتم من خلالها «تذكر» كل عامل ممرض بواسطة جسم مضاد للتوقيع الجيني ويمكن توجيه أوامر لخلايا الذاكرة المشار إليها لطرد عامل ممرض من الجسم بشكل سريع في حالة حدوث إصابات بعدوى لاحقًا.
الخلايا الفعالة (Effector cells)
تعد خلايا الجهاز المناعي التكيفي أحد أنواع الكريات البيضاء، المعروفة باسم الخلية الليمفاوية. وتعتبر الخلايا البائية والخلايا التائية نوعي الخلايا الليمفاوية الرئيسيين. ويتألف جسم الإنسان من نحو 2 تريليون خلية ليمفاوية، تشكل نسبة تتراوح ما بين %20 إلى %40 من خلايا الدم البيضاء (المعروفة بالاختصار WBCs)؛ غير أن حجمها الإجمالي يشكل نفس حجم المخ أو الكبد تقريبًا.[2] ويحتوي الدم المحيطي على نسبة %20 إلى %50 من الخلايا الليمفاوية الدوارة؛ أما النسبة المتبقية، فتنتقل من مكان لآخر داخل الجهاز الليمفاوي.[2]
وتنشأ الخلايا البائية والخلايا التائية من نفس الخلايا الجذعية متعددة القدرات المكونة للدم، والتي تظل غير مميزة في خصائصها عن بعضها البعض، إلى أن يتم تنشيطها.[4] تلعب الخلايا البائية دورًا كبيرًا في الاستجابة المناعية الخلطية، في حين تؤثر الخلايا التائية بشكل أساسي في الاستجابات المناعية الخلوية. وعلى الرغم من ذلك، فإنه في كل الفقاريات الأخرى تقريبًا، يتم إنتاج الخلايا البائية (والخلايا التائية) بواسطة الخلايا الجذعية في النخاع العظمي.[4] وتنتقل الخلايا التائية إلى الغدة التيموسية (Thymus)، التي اشتق اسمها منها نسبةً إلى الحرف T الذي تبدأ به، وتنمو فيها. وعند البشر، تعيد نسبة %1 إلى %2 من الخلايا الليمفاوية الدوران كل ساعة لزيادة فرص عثور الخلايا الليمفاوية نوعية المستضدات على هذه المستضدات النوعية داخل الأنسجة الليمفاوية الثانوية.[5]
في الحيوان البالغ، تضم الأعضاء الليمفاوية المحيطية الثانوية مزيجًا من الخلايا البائية والخلايا التائية فيما لا يقل عن ثلاث مراحل تمايز:
- الخلايا الساذجة التي قد نضجت وخرجت من النخاع العظمي أو الغدة التيموسية ودخلت إلى الجهاز الليمفاوي، والتي لا تزال في الوقت نفسه بحاجة إلى مواجهة مستضدها المناظر (النوعي)،
- الخلايا الفعالة التي قد تم تنشيطها بواسطة مستضدها المناظر، والتي تلعب دورًا مؤثرًا في القضاء على عامل ممرض، و
- خلايا الذاكرة - الخلايا التي بقت حيةً إلى أجل طويل بعد الإصابة بعدة أشكال من العدوى فيما مضى
عرض المستضد
تعتمد المناعة التكيفية على قدرة الخلايا المناعية على التمييز بين خلايا الجسم وبين أي أجسام أو كائنات غريبة غير مرغوب فيها تغزو الجهاز المناعي. وتعرض خلايا المضيف على سطحها مستضدات «ذاتية». وهذه المستضدات تختلف عن تلك الموجودة على سطح البكتيريا (المستضدات «غير الذاتية») أو على سطح الخلايا المضيفة المصابة بعدوى فيروسية (المستضدات «عديمة الذات»). وتتم استثارة الاستجابة التكيفية عن طريق التعرف على المستضدات غير الذاتية والمستضدات عديمة الذات.
وباستثناء الخلايا غير المنواة (بما فيها خلايا الدم الحمراء)، فإن جميع الخلايا لديها القدرة على عرض المستضد وتنشيط الاستجابة التكيفية.[4] وبعض الخلايا مجهز بشكل خاص لعرض المستضد وبرمجة الخلايا التائية الساذجة. وتجدر الإشارة هنا إلى أن الخلايا المتغصنة (Dendritic cells) والخلايا البائية (وبدرجة أقل الخلايا الملتهمة أو Macrophages) مزودة بمستقبلات خاصة محفزة للمناعة والتي تسمح بتنشيط الخلايا التائية بدرجة أكبر، وتعرف باصطلاح الخلايا العارضة للمستضد المتخصصة (APC).
ويمكن تنشيط عدة مجموعات فرعية من الخلايا التائية بواسطة خلايا عارضة للمستضد متخصصة، وكل نوع من الخلايا التائية مزود بشكل خاص من أجل التعامل مع كل عنصر سام أو عامل ممرض بكتيري أو فيروسي على حدة. ويعتمد نوع الخلية التائية التي تم تنشيطها ونوع الاستجابة المولدة، جزئيًا، على المحيط الذي حدثت فيه أول مواجهة بين الخلايا العارضة للمستضد المتخصصة والمستضد.[3]
المستضدات خارجية المنشأ
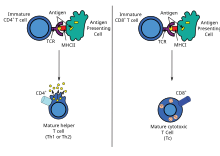
تبتلع الخلايا التغصنية العوامل الممرضة خارجية المنشأ، مثل البكتيريا أو الطفيليات أو السموم في الأنسجة، ثم تقوم بنقلها، عبر إشارات جذب كيميائي، إلى العقد الليمفاوية الغنية بالخلايا التائية. وفي أثناء عملية هجرة الخلايا، تمر الخلايا المتغصنة بعملية نضج تفقد فيها معظم قدرتها على ابتلاع العوامل الممرضة الأخرى وتكتسب قدرةً على الاتصال بالخلايا التائية. تستخدم الخلايا المتغصنة الإنزيمات لتقطيع العامل الممرض إلى أجزاء أصغر، تسمى مستضدات. وفي العقدة الليمفاوية، ستعرض الخلية المتغصنة هذه المستضدات «غير الذاتية» على سطحها عن طريق ربطها بمستقبل «ذاتي» يسمى معقد التوافق النسيجي الكبير، أو MHC (المعروف عند البشر أيضًا باسم مستضد الكريات البيضاء البشري أو HLA اختصارًا).[3] ويتم التعرف على مععقد التوافق النسيجي الكبير (MHC) هذا بواسطة الخلايا التائية المارة عبر العقدة الليمفاوية. وعادةً ما يتم عرض المستضدات خارجية المنشأ على جزيئات النوع الثاني من معقد التوافق النسيجي الكبير التي تقوم بتنشيط الخلايا التائية +CD4 المساعدة.[3]
المستضدات داخلية المنشأ
يتم إنتاج المستضادات داخلية المنشأ بواسطة الفيروسات التي تتكاثر داخل خلية مضيفة.[3] وتستخدم الخلية المضيفة إنزيمات لهضم البروتينات المرتبطة بعدوى فيروسية وعرض هذه الأجزاء على سطحها للخلايا التائية عن طريق ربطها بمعقد التوافق النسيجي الكبير. ويتم عرض المستضدات داخلية المنشأ في المعتاد على جزيئات النوع الأول من معقد التوافق النسيجي الكبير وتقوم بتنشيط الخلايا التائية +CD8 السامة للخلايا. وباستثناء الخلايا غير المنواة (بما في ذلك كريات الدم الحمراء)، يتم التعبير عن النوع الأول من معقد التوافق النسيجي الكبير بواسطة جميع الخلايا المضيفة.[3]
الخلايا الليمفاوية التائية
الخلايا الليمفاوية التائية +CD8 وسمية الخلايا
تعتبر الخلايا التائية السامة للخلايا أو Cytotoxic T cells (المعروفة اختصارًا أيضًا باسم TC أو الخلايا التائية القاتلة أو الخلايا الليمفاوية السامة للخلايا - CTL) مجموعة فرعية من الخلايا التائية التي تسبب موت الخلايا المصابة بالفيروسات (وغيرها من العوامل الممرضة الأخرى)، أو تكون تالفة أو عاطبة.[3]
ويتم تنشيط الخلايا التائية الساذجة السامة للخلايا عندما يتفاعل مستقبل الخلايا التائية (TCR) بقوة مع جزيء النوع الأول من معقد التوافق النسيجي الكبير المرتبط بببتيد. ويعتمد هذا على نوع معقد التوافق النسيجي الكبير وتوجيه معقد التوافق النسيجي الكبير/المستضد، وهو ما يجعل الخلية الليمفاوية التائية السامة للخلايا والخلية المصابة تبقيان مرتبطتين ببعضهما البعض.[3] وبمجرد تنشيطها، تمر الخلية الليمفاوية التائية السامة للخلايا بعملية تعرف باسم التوسع النسيلي، والتي تكتسب فيها إمكانات وظيفية وتنقسم بسرعة لإنتاج جيش من الخلايا الفعالة «المسلحة» ضد التهديدات. بعدها، ستنتقل الخلايا الليمفاوية التائية السامة للخلايا التي تم تنشيطها عبر أجزاء الجسم بحثا عن الخلايا التي تحمل ذلك المزيج الفريد من النوع الأول من معقد التوافق النسيجي الكبير والببتيد.
وعند تعرضها لهذه الخلايا الجسدية المصابة أو العاطبة، تفرز الخلايا الليمفاوية التائية الفعالة السامة للخلايا البرفورين والجرانوليسين: وهما نوعان من البروتينات السامة للخلايا، واللذان يكونان مسامًا في الغشاء البلازمي للخلية المستهدفة، على نحو يمكن الأيونات والماء من التدفق إلى الخلية المصابة والتسبب في انفجار أو انحلال الخلية.[3] تفرز الخلية الليمفاوية التائية السامة للخلايا الجرانزايم، وهو أحد أنواع بروتيز السيرين الذي ينفذ إلى الخلايا عبر المسام لتنشيط الاستماتة (الموت الذاتي للخلايا). وللحد من التلف الشامل للأنسجة أثناء فترة الإصابة بعدوى، تخضع عملية تنشيط الخلايا الليمفاوية التائية السامة للخلايا لمراقبة صارمة ويتطلب ذلك بشكل عام إشارة تنشيط قوية جدًا من معقد التوافق النسيجي الكبير/المستضد أو إشارات تنشيط إضافية من قبل الخلايا التائية «المساعدة» (انظر أدناه).[3]
وعند تلاشي العدوى، تموت غالبية الخلايا الفعالة وتتم إزالتها بواسطة الخلايا الملتهمة، غير أنه يتم الاحتفاظ بعدد محدود من هذه الخلايا لتعمل كخلايا ذاكرة.[4] ومع حدوث مواجهة لاحقة مع المستضد نفسه، تتمايز خلايا الذاكرة هذه بسرعة إلى خلايا فعالة، على نحو يقلل بدرجة هائلة من الفترة الزمنية اللازمة لتوجيه استجابة مناعية فعالة.
الخلايا التائية المساعدة
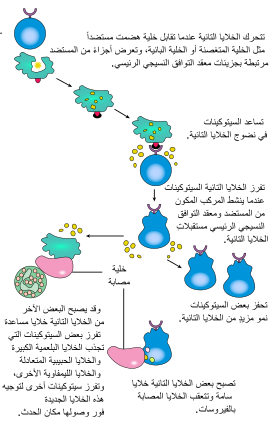
تمثل الخلايا الليمفاوية +CD4 أو الخلايا التائية المساعدة وسائط استجابة مناعية وتلعب دورًا مهمًا في تشكيل إمكانات الاستجابة المناعية التكيفية وزيادتها إلى أقصى درجة ممكنة.[3] غير أنه ليس لهذه الخلايا أي نشاط متعلق بتسميم الخلايا أو التهامها، فضلاً عن أنها لا يمكن أن تقتل الخلايا المصابة بعدوى أو تزيل العوامل الممرضة، لكنها في الأساس «تدير» الاستجابة المناعية، عن طريق توجيه الخلايا الأخرى لأداء مثل هذه المهام.
تعرض الخلايا التائية المساعدة على سطحها مستقبلات خلايا تائية (TCR) تتعرف على المستضد المرتبط بجزيئات النوع الثاني من معقد التوافق النسيجي الكبير. ونتيجة تنشيط خلية تائية مساعدة ساذجة، فإنها تقوم بإفراز مواد السيتوكين (مركبات بروتينية صغيرة) التي تحفز نشاط العديد من أنواع الخلايا، بما فيها الخلايا العارضة للمستضد التي نشطتها. وتتطلب الخلايا التائية المساعدة منبه تنشيط أخف في تأثيره بكثير من الخلايا التائية السامة للخلايا. ويمكن أن تطلق الخلايا التائية المساعدة مزيدًا من الإشارات التي «تساعد» في تنشيط الخلايا السامة للخلايا.[4]
الاستجابة Th1 والاستجابة Th2: استجابات الخلايا التائية المساعدة
هناك نوعان من استجابات الخلايا التائية المساعدة +CD4 الفعالة يمكن أن تحدثهما خلية عارضة للمستضد متخصصة، يشار إليهما بالرمزين Th1 وTh2، والمصممان من أجل إزالة أنواع مختلفة من العوامل الممرضة. ولم يتم التوصل إلى فهم كامل بشأن العوامل التي تحدد ما إذا كانت عدوى ما ستستثير نوع الاستجابة Th1 أم Th2، غير أن الاستجابة المولدة تلعب دورًا أساسيًا في إزالة عوامل ممرضة مختلفة.[3]
ويميز الاستجابة Th1 إفراز هرمون إنترفيرون جاما، الذي يحفز النشاط البكتيري للخلايا الملتهمة ويستحث الخلايا البائية على إنتاج أجسام مضادة طاهية (مغلفة)، ويؤدي إلى تكون «مناعة خلوية».[3] أما الاستجابة Th2، فيميزها إفراز هرمون إنترليوكين 4، الذي ينتج عنه تنشيط الخلايا البائية لإنتاج أجسام مضادة مبطلة لتأثير العوامل الممرضة وأشكال العدوى (قاتلة)، مما يؤدي إلى تكون «مناعة خلطية».[3] وفي العموم، تمتاز استجابات Th1 بأنها أكثر فاعليةً بدرجة أكبر ضد العوامل الممرضة داخل الخلوية (الفيروسات والبكتيريا الموجودة داخل الخلايا المضيفة)، في حين أن استجابات Th2 تعد أكثر فاعليةً ضد البكتيريا والفطريات والسموم خارج الخلوية.[3] وعلى غرار الخلايا التائية السامة للخلايا، فإن غالبية الخلايا المساعدة +CD4 تموت عند تلاشي العدوى، مع بقاء عدد محدود منها في صورة خلايا ذاكرة +CD4.
ويتمتع فيروس نقص المناعة البشرية (HIV) بالقدرة على تدمير الجهاز المناعي من خلال مهاجمة الخلايا التائية +CD4، وتحديدًا الخلايا التي يمكن أن تدفع عملية تدمير الفيروس، وأيضًا الخلايا التي تحفز تكوين المناعة ضد جميع العوامل الممرضة الأخرى التي تتم مواجهتها أثناء فترة حياة المتعضيات.[4]
وهناك نوع ثالث من الخلايا الليمفاوية التائية، وهو الخلايا التائية المنظمة (المعروفة أيضًا بالاختصار Treg)، وهي خلايا تقيد وتثبط الجهاز المناعي، وقد تضبط الاستجابات المناعية الشاذة تجاه المستضدات الذاتية؛ وهي آلية مهمة في مكافحة الإصابة بأمراض المناعة الذاتية.[4]
ولا تعمل الخلايا التائية مطلقًا عمل الخلايا العارضة لمستضد.
الخلايا التائية γδ
تمتلك الخلايا التائية γδ (خلايا جاما دلتا التائية) مستقبل خلايا تائية (TCR) بديلاً على عكس الخلايا التائية +CD4 و+CD8 وαβ وتجمع بين خصائص الخلايا التائية المساعدة والخلايا التائية السامة للخلايا والخلايا القاتلة الطبيعية. وعلى غرار مجموعات الخلايا التائية الفرعية «غير التقليدية» الأخرى التي تحمل مستقبلات خلايا تائية بديلة ثابتة، مثل الخلايا التائية القاتلة الطبيعية المقيدة بجزيء CD1d، فإن الخلايا التائية γδ تظهر بخصائص تجعلها واقعةً على الحد الفاصل بين المناعة الطبيعية والمناعة التكيفية. فمن ناحية، ربما ينظر إلى الخلايا التائية γδ على أنها أحد مكونات المناعة التكيفية من حيث إنها تعيد ترتيب جينات مستقبل الخلايا التائية عبر عملية إعادة تشكيل V(D)J، التي تولد بدورها ما يعرف باسم التنوع الوصلي، كما تنتج نمطًا ظاهريًا من الذاكرة. وعلى الرغم من ذلك، فإنه على الجانب الآخر ربما تعد مجموعات الخلايا التائية الفرعية المختلفة جزءًا من الجهاز المناعي الطبيعي، والذي قد يتم فيه استخدام مستقبل خلية تائية مقيد و/أو مستقبلات الخلايا القاتلة الطبيعية في صورة مستقبلات لتمييز أنماط الجزيئات المرتبطة بعوامل ممرضة. على سبيل المثال، وفقًا لهذا النموذج، توجه أعداد كبيرة من الخلايا التائية Vγ9/Vδ2 استجابة في خلال ساعات ضد جزيئات شائعة تنتجها الميكروبات، كما ستستجيب خلايا تائية Vδ1 داخل ظهارية مقيدة بدرجة عالية للخلايا الظهارية المشدودة.
الخلايا الليمفاوية البائية وإنتاج الأجسام المضادة

تعتبر الخلايا البائية هي الخلايا الرئيسية التي تدخل في عملية إنتاج الأجسام المضادة التي تنتشر في بلازما الدم والغدة الليمفاوية، المعروفة باسم مناعة خلطية. وتتمثل الأجسام المضادة (أو الجلوبيولين المناعي من النوع 1g) في بروتينات على شكل حرف Y يستخدمها الجهاز المناعي في التعرف على الأجسام الغريبة وإبطال تأثيرها. في الثدييات، توجد خمسة أنواع من الأجسام المضادة: IgA وIgD وIgE وIgG و IgM، التي تختلف في خصائصها البيولوجية، والتي قد نشأ كل منها بغرض التعامل مع أنواع مختلفة من المستضدات. وعند تنشيطها، تنتج الخلايا البائية أجسامًا مضادةً، يتعرف كل منها على مستضد واحد ويبطل تأثير عوامل ممرضة معينة.[3]
وعلى غرار مستقبل الخلية التائية، فإن الخلايا البائية تعرض مستقبل خلية بائية (BCR) مميزًا، وهو في هذه الحالة، جزيء جسم مضاد شلت حركته. ويتعرف مستقبل الخلية البائية على مستضد واحد معين فقط ويرتبط به. ويتمثل أحد أوجه الاختلاف المهمة بين الخلايا البائية والخلايا التائية في الطريقة التي «يتعرف» بها كل نوع من نوعي الخلايا على مستضد. فالخلايا التائية تتعرف على المستضد المطابق للجسم المضاد الموجود على سطحها في شكل معالج - في صورة ببتيد ضمن تركيب أحد جزيئات معقد التوافق النسيجي الكبير،[3] في حين تتعرف الخلايا البائية على المستضدات في شكلها الأصلي.[3] وبمجرد أن تلاقي إحدى الخلايا البائية المستضد المطابق للجسم المضاد الموجود على سطحها (أو مستضدها النوعي) (وتتلقى مزيدًا من الإشارات من خلية تائية مساعدة (غالبًا من نوع Th2)، فإنها تتمايز إلى خلية فعالة، تعرف باسم خلية بلازما.[3]
وخلايا البلازما هي خلايا قصيرة الأجل (يومان-3 أيام) تفرز أجسامًا مضادةً. وترتبط هذه الأجسام المضادة بالمستضدات، بحيث تجعلها أهدافًا سهلة بالنسبة للخلايا الملتهمة، وتنشط تتابع مجموعات المكمل (تعاقب تنشيط البروتينات الموجهة لتدمير الخلايا الدخيلة).[3] وستظل نحو %10 من خلايا البلازما حية لتصبح خلايا ذاكرة بائية طويلة الأجل نوعية المستضدات.[3] ونظرًا لأن هذه الخلايا مبرمجة بالفعل على إنتاج أجسام مضادة نوعية، فإنه يمكن توجيه أوامر لها للاستجابة بشكل سريع، في حالة ما إذا أصاب نفس العامل الممرض الخلية المضيفة مجددًا، في حين أن الخلية المضيفة تظهر عليها أعراض بسيطة، إن وجدت.
الجهاز المناعي التكيفي البديل
على الرغم من أن الجزيئات التقليدية للجهاز المناعي التكيفي (الأجسام المضادة ومستقبلات الخلايا التائية) لا توجد إلا لدى الفقاريات ذوات الفك، فإنه قد تم اكتشاف جزيء مشتق من خلية ليمفاوية في الفقاريات عديمة الفك البدائية، مثل اللامبري (الأنقليس) وسمك الهاج (الزيالون). وتمتلك هذه الحيوانات عددًا هائلاً من الجزيئات، تعرف باسم مستقبلات الخلايا الليمفاوية المتغيرة (VLRs اختصارًا) والتي، على شاكلة مستقبلات المستضدات في الفقاريات ذوات الفك، يتم إنتاجها فقط من عدد محدود من الجينات (جين واحد أو اثنين). ويعتقد أن هذه الجزيئات تربط مستضدات ممرضة بطريقة مماثلة للأجسام المضادة، وبالدرجة نفسها من النوعية.[7]
الذاكرة المناعية
عند تنشيط الخلايا البائية والخلايا التائية، سيعمل البعض منها عمل خلايا ذاكرة. وعلى مدار حياة الحيوان، تشكل خلايا الذاكرة هذه قاعدة بيانات من الخلايا الليمفاوية البائية والتائية الفعالة. ومع التفاعل مع مستضد تمت مواجهته من قبل، يتم انتقاء خلايا الذاكرة المناسبة وتنشيطها. وبهذا الأسلوب، يولد التعرض مرةً ثانيةً ومرات لاحقة لمستضد بعينه استجابةً مناعيةً أقوى وأسرع. وتعد هذه الاستجابة المناعية «تكيفية»، نظرًا لأن الجهاز المناعي يعد نفسه لمواجهة المخاطر المستقبلية. وقد تكون الذاكرة المناعية إما في صورة ذاكرة خاملة قصيرة الأجل أو ذاكرة نشطة طويلة الأجل.
الذاكرة الخاملة
عادةً ما تكون الذاكرة الخاملة قصيرة الأجل، تمتد لفترة تتراوح ما بين بضعة أيام وعدة أشهر. إذ إن الأطفال الرضع حديثي الولادة لا يكونون قد تعرضوا من قبل لميكروبات ويكونون عرضةً على وجه الخصوص للإصابة بأية عدوى. ويتم تزويدهم بطبقات متعددة من الحماية المناعية الخاملة بواسطة الأم. في الرحم، يتم نقل الأجسام المضادة من نوع IgG المستمد من الأم مباشرةً عبر المشيمة إلى جسم الطفل الرضيع، بحيث تكون لدى الأطفال الرضع عند ولادتهم مستويات عالية من الأجسام المضادة، وبنفس نطاق نوعيات المستضدات التي لدى أمهاتهم.[3] ويحتوي لبن الأم على أجسام مضادة تنتقل إلى أمعاء الطفل الرضيع حديث الولادة، مما يحميه من أشكال العدوى البكتيرية، إلى أن يصبح بإمكانه تكوين أجسام مضادة خاصة به.[3]
وتعد هذه مناعة خاملة نظرا لأن الرضيع لا ينتج فعليًا أي خلايا ذاكرة أو أجسام مضادة، فهو فقط يستعيرها من الأم. كذلك، يمكن أن تنتقل المناعة الخاملة قصيرة الأجل بشكل اصطناعي من فرد لآخر عبر المصل الغني بالأجسام المضادة.
الذاكرة النشطة
في العموم، تكون المناعة النشطة طويلة الأجل ويمكن اكتسابها بواسطة العدوى التي يتبعها تنشيط الخلايا البائية والخلايا التائية، أو يمكن اكتسابها اصطناعيًا بواسطة اللقاحات، في عملية تعرف باسم التحصين (immunization).
التحصين
منذ قديم الأزل، كانت الأمراض المعدية هي السبب الرئيسي للوفاة بين البشر. وعلى مدار القرن الماضي، تم تطوير عاملين مهمين لمقاومة انتشار هذه الأمراض: الإصحاح البيئي والتحصين.[4] ويعد التحصين (الذي يشار إليه في العموم باسم التطعيم) هو الاستثارة المتعمدة لاستجابة مناعية، ويمثل أكثر آليات توظيف الجهاز المناعي التي ابتكرها العلماء فاعليةً.[4] ويعتبر التحصين وسيلةً ناجحةً نظرًا لأنه يستغل النوعية الطبيعية للجهاز المناعي، وأيضًا قابليته للاستثارة.
وتتمثل القاعدة الأساسية التي يقوم عليها أسلوب التحصين في عرض مستضد مشتق من مرض يؤدي بالعضية التي تحفز الجهاز المناعي إلى تكوين مناعة وقائية ضد تلك العضية، والتي لا تسبب بنفسها التأثيرات الممرضة لتلك العضية. ويعرف مصطلح المستضد (antigen) (الذي يمثل اختصارًا لمصطلح anti body gen erator) على أنه أية مادة ترتبط بجسم مضاد معين وتحدثاستجابةً مناعيةً تكيفيةً.[2]
وتعتمد معظم اللقاحات الفيروسية على فيروسات ضعيفة حية، في حين تعتمد العديد من اللقاحات البكتيرية على مكونات لا خلوية لعضيات دقيقة، بما فيها المكونات السمية غير الضارة.[2] وتجدر الإشارة هنا إلى أن العديد من المستضدات المشتقة من لقاحات لا خلوية لا تستحث استجابةً مناعيةً تكيفيةً بقوة، كما أن غالبية اللقاحات البكتيرية تتطلب إضافة مواد مساعدة adjuvants تنشط الخلايا العارضة للمستضد في الجهاز المناعي الطبيعي لتعزيز قدرتها على توليد المناعة.[4]
التنوع المناعي
يمكن أن تعمل غالبية الجزيئات الضخمة، بما فيها فعليًا جميع البروتينات وكثير من المواد عديدة التسكر كمستضدات.[3] ويطلق على أجزاء المستضد التي تتفاعل مع جزيء أحد الأجسام المضادة أو أحد مستقبلات الخلية الليمفاوية اسم حاتمات (epitopes). وتضم غالبية المستضدات مجموعة حاتمات ويمكنها أن تحفز عملية إنتاج أجسام مضادة أو تستحث استجابات مناعية معينة من جانب الخلايا التائية، أو الأمرين معًا.[3]

وهناك نسبة ضئيلة جدًا (أقل من %0.01) من مجموع الخلايا الليمفاوية لديها القدرة على الارتباط بمستضد معين، مما يشير إلى أن عددًا محدودًا فقط من الخلايا هو الذي سيستجيب لكل مستضد.[4]
ولكي تتمكن الاستجابة المناعية (immune response) من «تذكر» عدد كبير من العوامل الممرضة والقضاء عليها، يجب أن تكون لدى الجهاز المناعي القدرة على التمييز بين عدة مستضدات مختلفة،[2] بالإضافة إلى أنه يتحتم إنتاج المستقبلات التي تتعرف على المستضدات في صورة مجموعة هائلة من الأشكال، مستقبل واحد في الأساس (على الأقل) لكل عامل ممرض يحتمل مواجهته. حتى في حالة غياب التنبيه من جانب مستضد، يكون باستطاعة الإنسان إنتاج ما يزيد عن 1 تريليون جزيء مختلف من جزيئات الأجسام المضادة.[4] وستكون هناك حاجة لملايين الجينات من أجل حفظ المعلومات الجينية المستخدمة في إنتاج هذه المستقبلات، غير أن الجينوم البشري بأكمله يضم جينات يقل عددها عن 25,000 جين.[8]
ويتم إنتاج هذا العدد الهائل من المستقبلات من خلال عملية تعرف باسم الانتقاء النسيلي.[2][3] ووفقًا لنظرية الانتقاء النسيلي، يقوم الحيوان، عند ولادته، بإنتاج مجموعة هائلة من الخلايا الليمفاوية بشكل عشوائي (والتي يحمل كل منها مستقبل مستضد معين) من المعلومات المشفرة في عائلة جينية صغيرة. من أجل توليد كل مستقبل خاص بمستضد معين، فإن هذه الجينات ستمر بعملية تعرف باسم إعادة تشكيل V(D)J ، أو التنوع الاندماجي والذي يعيد فيه أحد الأجزاء الجينية الاندماج مع أجزاء جينية أخرى لتشكيل جين واحد مميز. وعملية التجمع هذه هي التي تولد هذا الكم الهائل والمتنوع من المستقبلات والأجسام المضادة، قبل أن يواجه الجسم أي مستضدات، والتي تمكِّن الجهاز المناعي من الاستجابة لمجموعة متنوعة لا محدودة من المستضدات.[3] على مدار فترة حياة حيوان ما، سيتم انتقاء تلك الخلايا الليمفاوية التي يمكنها اتخاذ استجابة ضد المستضدات التي يواجهها الحيوان بالفعل، لاتخاذ فعل معين موجه ضد أي شيء يعبر عن ذلك المستضد.
ومن الجدير بالذكر أن الأجزاء الطبيعية والأجزاء التكيفية بالجهاز المناعي تعمل معًا وليس كبديل لبعضها البعض. ولن يكون في استطاعة السلاح المناعي التكيفي، الممثل في الخلايا البائية والخلايا التائية العمل دون دعم من الجهاز المناعي الطبيعي. وستكون الخلايا التائية عديمة الفائدة في حالة عدم وجود خلايا عارضة للمستضد لتنشيطها، كما سيتعطل عمل الخلايا البائية بدون مساعدة الخلايا التائية. على الجانب الآخر، من المرجح أن يمتلأ الجهاز المناعي الطبيعي بشكل مفرط بالعوامل الممرضة، في حالة عدم وجود تأثير متخصص للاستجابة المناعية التكيفية.
المناعة التكيفية أثناء الحمل
يتمثل محور العمل الأساسي للجهاز المناعي في التعرف على المستضدات «الذاتية» مقابل المستضدات «غير الذاتية». ومن ثم، فإن الآليات التي تحمي الجنين البشري (الذي يعتبر حاملاً لمستضدات خارجية المنشأ «غير ذاتية») من أي هجوم، والتي يوظفها الجهاز المناعي، مثيرة للاهتمام على وجه الخصوص. وعلى الرغم من عدم ظهور أي تفسير شامل لفك هذا اللغز، وعدم الإنكار، المتكرر في المعتاد، فإن هناك سببين تقليديين ربما يعزى إليهما كيفية تحمل الجنين. ويتمثل السبب الأول في أن الجنين يشغل جزءًا من الجسم محميًا بحاجز غير مناعي، الرحم، الذي لا يحميه الجهاز المناعي في المعتاد.[3] أما السبب الثاني، فيتمثل في أن الجنين نفسه ربما يعزز التثبيط المناعي في جسم الأم، وربما يكون ذلك من خلال عملية استنفاد المغذيات الفعالة.[3] وهناك تفسير أكثر حداثة لهذا الاستحثاث على التحمل، ألا وهو أن البروتينات السكرية المعبر عنها في الرحم أثناء الحمل تثبط الاستجابة المناعية في الرحم (انظر الجهاز الدفاعي للجنين في الحيوانات الثديية أو eu-FEDS).
أثناء فترة الحمل في الثدييات الولودة (جميع الثدييات باستثناء أحاديات الفتحة)، يتم تنشيط الفيروسات المنعكسة داخلية المنشأ وإنتاج أعداد هائلة منها أثناء مرحلة انغماس الجنين في جدار الرحم. ومن المعروف عنها في الوقت الحالي امتلاكها خصائص مثبطة للمناعة، مما يشير إلى أنها تحمي الجنين من الجهاز المناعي للأم. فضلاً عن ذلك، فإنه من الواضح أن بروتينات الالتحام الفيروسية تسبب تكون المدمج الخلوي المشيمي.[9] بهدف الحد من تبادل الخلايا المهاجرة بين الجنين المتكون في رحم الأم وبين جسم الأم (الأمر الذي لن تقوم به الأنسجة الطلائية على النحو الكافي، إذ إن أنواعا معينة من خلايا الدم متخصصةً بحيث تكون قادرة على دمج نفسها بين الخلايا الظاهرية المجاورة). وكان العمل المثبط للمناعة هو السلوك الطبيعي الأولى للفيروس، مثل HIV، وكانت بروتينات الالتحام وسيلة لنقل العدوى إلى الخلايا الأخرى عن طريق دمجها بالخلية المصابة (يقوم فيروس HIV بالعمل نفسه). ويعتقد أن سلالات الثدييات الولودة الحديثة قد نشأت بعد الإصابة بعدوى بهذا الفيروس، على نحو يتيح للجنين مقاومة الجهاز المناعي للأم.[10]
وقد اكتشف مشروع الجينوم البشري البحثي آلافًا من الفيروسات المنعكسة داخلية المنشأ والمصنفة إلى 24 عائلاً أو فصيلةً.[11]
التطور
نشأ جهاز المناعة المكتسبة أو التكيفي -الذي دُرس بشكل أفضل لدى الثدييات- لدى الأسماك الفكية منذ حوالي 500 مليون سنة مضت. توجد معظم الجزيئات والخلايا والأنسجة والآليات المرتبطة بهذا الجهاز الدفاعي في الأسماك الغضروفية.[12] تتواجد مستقبلات الخلايا اللمفاوية ومستقبلات الخلايا التائية لدى جميع الفقاريات الفكية. أقدم فئة من الغلوبولينات المناعية وهو الغلوبيولين المناعي م IgM هو غلوبولين مرتبط بالغشاء يتم إفرازه عقب تنشيط الخلايا البائية للأسماك الغضروفية. لنمطٍ إسوي آخر وهو الغلوبولين المناعي و (IgW) الخاص بالقروش صلة بالغلوبولين المناعي د (IgD) الخاص بالثدييات. المستقبلات التائية من كلا النوعين α/β وγ/δ موجودة لدى جميع الحيوانات من الفكيات إلى الثدييات. يختلف ترتيب القطع الجينية التي تخضع لإعادة ترتيب جيني لدى الأسماك الغضروفية التي تملك هيئة متكدسة مقارنة بهيئة التراسلوكون لدى الأسماك العظمية إلى الثدييات. على غرار المستقبلات التائية والغلوبولينات المناعية، لا يتواجد معقد التوافق النسيجي الكبير (مهس MHC) سوى لدى الفقاريات الفكية. للجينات التي تقوم بمعالجة المستضد وعرضه وكذلك جينات مهس القسم 1 ومهس القسم 2 [English] صلة وثيقة ببعضها في جميع جزيئات مهس الخاصة بالأنواع المدروسة تقريبا.
يمكن التعرف على وجود الخلايا اللمفانية (شبه لمفاوية) لدى بعض ثانويات الفم قبل الفقارية (مثل قنفذ البحر).[13] ترتبط هذه الخلايا بالمستضدات عبر مستقبلات التعرف على الأنماط الخاصة بجهاز المناعة الفطرية. لدى الأسماك اللافكية، تستخدم ثلاث أنواع فرعية من الخلايا اللمفاوية مستقبلات الخلية اللمفاوية المتغيرة للارتباط بالمستضد.[14] يتم توليد التنوع في هذه المستقبلات عبر إعادة ترتيب قطع دنا بها تكرارات غنية باليوسين يقوم بها نازعة أمين السايتوسين [English].[15] لا توجد دلائل على جينات منشطة للتأشيب (راغ RAG) تقوم بتأشيب قطع جينات المستقبلات التائية والغلوبولينات المناعية لدى الفقاريات الفكية.
يُعتقد أن تطور جهاز المناعة التكيفي المبني على جزيئات: معقد التوافق النسيجي الكبير والمستقبلات التائية (TCR) والغلوبولينات المناعية (Ig) نشأ من حادثتي تطور كبيرتين: اكتساب ينقول راغ (ربما من أصل فيروسي) وتضاعف كامل للجينوم [English] مرتين.[12] رغم أن جزيئات جهاز المناعة التكيفي محفوظة جيدا إلا أنها تتطور بسرعة كذلك، ومع ذلك وجد دراسات مقارنة أن العديد من الميزات متماثلة عبر الأصناف. نشأت معظم الميزات الرئيسية لجهاز المناعة التكيفي باكرا وسريعا، وتملك الأسماك اللافكية جهاز مناعة تكيفي مختلف يعتمد على التأشيب الجيني لتوليد مستقبلات مناعية وظيفتها مماثلة لوظائف الغلوبولينات المناعية المستقبلات التائية.[16] جهاز المناعة الفطرية - الذي له دور مهم في تنشيط جهاز المناعة التكيفي- هو أهم جهاز مناعي لدى اللافقاريات والنباتات.
انظر أيضًا
المراجع
- ^ Q114972534، ص. 11، QID:Q114972534
- ^ أ ب ت ث ج ح خ Alberts, B., Johnson, A., Lewis, J., Raff, M., Roberts, K., and Walters, P. (2002). Molecular Biology of the Cell (ط. 4th). New York and London: Garland Science. مؤرشف من الأصل في 2009-09-18.
{{استشهاد بكتاب}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ أ ب ت ث ج ح خ د ذ ر ز س ش ص ض ط ظ ع غ ف ق ك ل م ن هـ و ي أأ Janeway, C.A., Travers, P., Walport, M., and Shlomchik, M.J. (2001). Immunobiology (ط. 5th). New York and London: Garland Science. مؤرشف من الأصل في 2021-05-23.
{{استشهاد بكتاب}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link)[1]. - ^ أ ب ت ث ج ح خ د ذ ر ز س Janeway C.A., Travers, P., Walport, M., Shlomchik, M.J. (2005). Immunobiology (ط. 6th). Garland Science.
{{استشهاد بكتاب}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Microbiology and Immunology On-Line Textbook: مدرسة الطب بجامعة جنوب كاليفورنيا الأمريكية نسخة محفوظة 16 أكتوبر 2014 على موقع واي باك مشين.
- ^ أ ب ت ث الدليل المرجعي للمعهد القومي للحساسية والأمراض المعدية (NIAID) كتاب Understanding the immune System (بتنسيق pdf). المرجع.
- ^ M.N. Alder, I.B. Rogozin, L.M. Iyer, G.V. Glazko, M.D. Cooper, Z. Pancer (2005). "Diversity and Function of Adaptive Immune Receptors in a Jawless Vertebrate". Science. ج. 310 ع. 5756: 1970–1973. DOI:10.1126/science.1119420. PMID:16373579.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ International Human Genome Sequencing Consortium (2004). "Finishing the euchromatic sequence of the human genome". Nature. ج. 431 ع. 7011: 931–45. DOI:10.1038/nature03001. PMID:15496913. مؤرشف من الأصل في 2017-07-22.
- ^ Mi S, Lee X, Li X؛ وآخرون (فبراير 2000). "Syncytin is a captive retroviral envelope protein involved in human placental morphogenesis". Nature. ج. 403 ع. 6771: 785–9. DOI:10.1038/35001608. PMID:10693809.
{{استشهاد بدورية محكمة}}: Explicit use of et al. in:|مؤلف=(مساعدة)صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - ^ Luis P. Villarreal. "The Viruses That Make Us: A Role For Endogenous Retrovirus In The Evolution Of Placental Species". University of California, Irvine (lecture notes). مؤرشف من الأصل في 2012-04-02. اطلع عليه بتاريخ 2008-02-03.
- ^ Luis P. Villarreal (أكتوبر 2001). "Persisting Viruses Could Play Role in Driving Host Evolution". ASM News (American Society for Microbiology). مؤرشف من الأصل في 2012-03-06.
- ^ أ ب Flajnik MF، Kasahara M (يناير 2010). "Origin and evolution of the adaptive immune system: genetic events and selective pressures". Nature Reviews. Genetics. ج. 11 ع. 1: 47–59. DOI:10.1038/nrg2703. PMC:3805090. PMID:19997068.
- ^ Hibino T، Loza-Coll M، Messier C، Majeske AJ، Cohen AH، Terwilliger DP، Buckley KM، Brockton V، Nair SV، Berney K، Fugmann SD، Anderson MK، Pancer Z، Cameron RA، Smith LC، Rast JP (ديسمبر 2006). "The immune gene repertoire encoded in the purple sea urchin genome" (PDF). Developmental Biology. ج. 300 ع. 1: 349–65. DOI:10.1016/j.ydbio.2006.08.065. PMID:17027739. مؤرشف من الأصل (PDF) في 2022-12-10.
- ^ Pancer Z، Amemiya CT، Ehrhardt GR، Ceitlin J، Gartland GL، Cooper MD (يوليو 2004). "Somatic diversification of variable lymphocyte receptors in the agnathan sea lamprey" (PDF). Nature. ج. 430 ع. 6996: 174–80. Bibcode:2004Natur.430..174P. DOI:10.1038/nature02740. hdl:2027.42/62870. PMID:15241406. S2CID:876413. مؤرشف من الأصل (PDF) في 2023-02-16.
- ^ Rogozin IB، Iyer LM، Liang L، Glazko GV، Liston VG، Pavlov YI، Aravind L، Pancer Z (يونيو 2007). "Evolution and diversification of lamprey antigen receptors: evidence for involvement of an AID-APOBEC family cytosine deaminase". Nature Immunology. ج. 8 ع. 6: 647–56. DOI:10.1038/ni1463. PMID:17468760. S2CID:3658963.
- ^ Boehm T (مايو 2011). "Design principles of adaptive immune systems". Nature Reviews. Immunology. ج. 11 ع. 5: 307–17. DOI:10.1038/nri2944. PMID:21475308. S2CID:25989912.
| في كومنز صور وملفات عن: جهاز مناعي تكيفي |